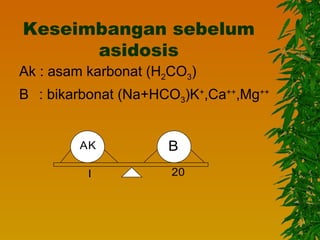
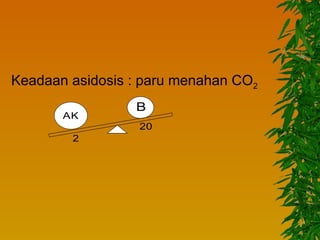
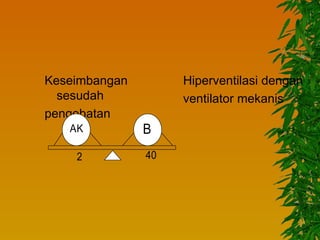
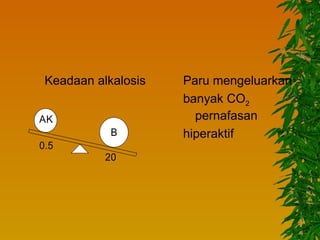
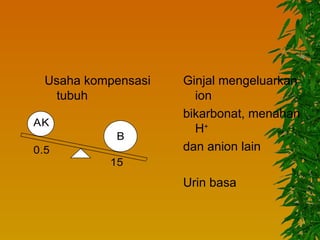
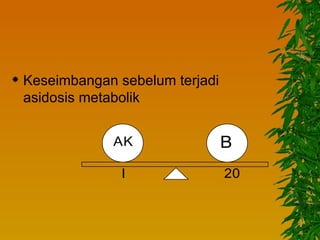
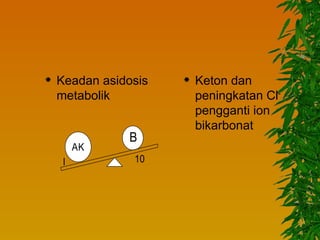
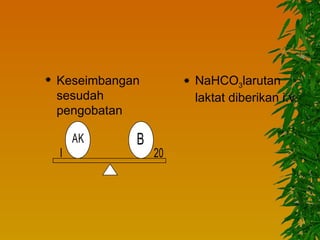
Dokumen ini membahas gangguan keseimbangan asam basa, termasuk pengertian asam dan basa, faktor-faktor yang mempengaruhi, serta berbagai jenis kelainan seperti asidosis dan alkalosis respiratorik maupun metabolik. Mekanisme kompensasi tubuh serta pengobatan yang sesuai untuk masing-masing kondisi juga dijelaskan. Akhirnya, bahaya dari gangguan asam basa terhadap kadar kalium dan fungsi tubuh diuraikan, termasuk potensi komplikasi kritis.