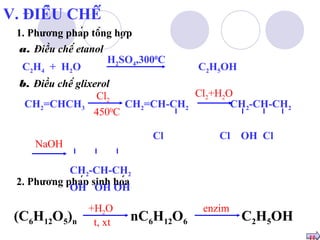
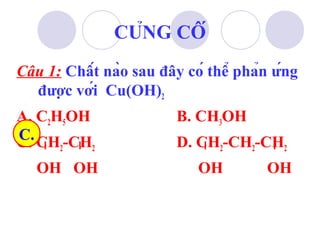
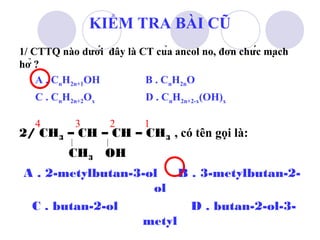
Tài liệu trình bày các tính chất hóa học của ancol no, đơn chức và phản ứng của chúng, bao gồm phản ứng thế nguyên tử H, phản ứng tách nước và phản ứng oxi hóa. Nó cũng đề cập đến phương pháp điều chế ancol và ứng dụng của etanol trong đời sống, đặc biệt là tác động của etanol đối với cơ thể con người. Cuối cùng, tài liệu nêu vấn đề an toàn liên quan đến việc pha chất phụ gia vào xăng, dẫn đến nguy cơ cháy nổ.



![IV. TÍNH CHẤT HÓA HỌC
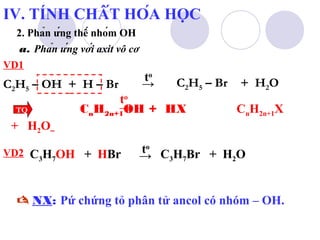
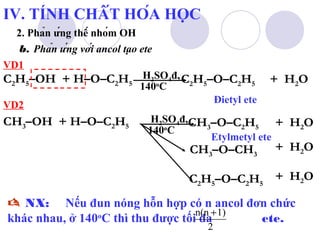
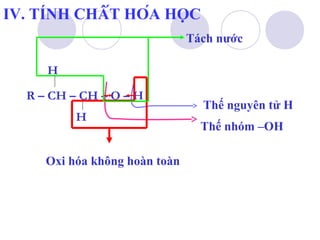
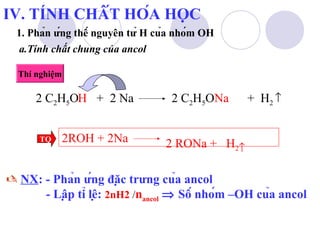
1. Phản ứng thế nguyên tử H của nhóm OH
b. Tính chất đặc trưng của ancol đa chức có nhóm OH cạnh nhau
- Cho vào 2 ống nghiệm dd CuSO4 và NaOH
- Cho C3H5(OH)3 vào 1 trong 2 ống nghiệm, quan sát.
Thí nghiệm
H2O
CH2 OH HO
CH O
CH2 OH HO
CH2
Cu O CH
H + HO Cu OH + H +2
CH2
HO CH2
CH
O
HO CH2
CH2 OH
CH O
CH2 OH
2C3H5(OH)3+Cu(OH)2 → [C3H5(OH)2O]2Cu + 2H2O
VD: 2C2H4(OH)2 + Cu(OH)2 →
Đồng (II) glixerat, màu xanh
[ C2H4(OH)O]2Cu +H2O
NX: Dùng Cu(OH)2 để phân biệt ancol đơn chức với ancol đa chức
có các nhóm –OH cạnh nhau trong phân tử](https://image.slidesharecdn.com/baigiangancol-141217014903-conversion-gate01/85/Ancol-nang-cao-ti-t-2-7-320.jpg)