يتناول النص مجموعة من المفاهيم الكيميائية المتعلقة بالتفاعلات الكيميائية المختلفة، بما في ذلك الصيغ الأولية والجزيئية والمركبات. يتضمن أيضًا أمثلة على التفاعلات بين الأحماض والقواعد وعوامل التفاعل الأخرى. يشرح النص كيفية تصنيف المحاليل الكيميائية والقوانين المتعلقة بها.

![يساجعت نهبئيت كيًيبء
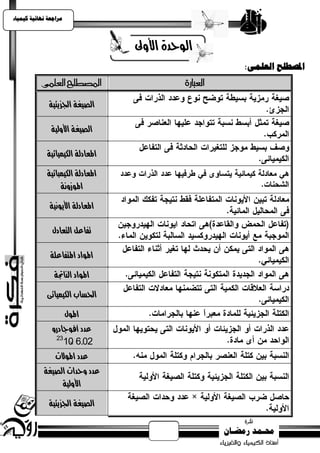
1] حضاب الصيغة األولية
[
]21 = [H = 1 , C
انحم:-
C H
4CH
2] حضاب الصيغة اجلشيئية
[
اىنخيت اىجزيئيت
عدد وحداث اىصيغت األوىيت =
مخيت اىصيغت األوىيت
2CH
انحم1:-
2CH](https://image.slidesharecdn.com/1-120515020920-phpapp01/85/1-3-320.jpg)
![يساجعت نهبئيت كيًيبء
8C4H 2CH
3] حضاب املول[
]1 = [O = 16 , H
انحم1:-
][H2O
]61 = [S = 32 , O )2(SO
انحم2:-
)2(SO](https://image.slidesharecdn.com/1-120515020920-phpapp01/85/1-4-320.jpg)
![يساجعت نهبئيت كيًيبء
]32 = [Na
)3(Na2CO
)702 = (Pb
[4] احلضاب اللينيائى
)2H2(g) + O2(g )2H2O(g
]61 = [H = 1 , O
انحم1:-
)2H2(g) + O2(g )2H2O(g
][H2O
]61 = [Mg = 24 , O
انحم2:-
)(Mg
)(MgO](https://image.slidesharecdn.com/1-120515020920-phpapp01/85/1-5-320.jpg)
![يساجعت نهبئيت كيًيبء
2Mg + O2 2MgO
CaCO3 CaO + CO2
[Ca = 40, C = 12, O = 16]
:3انحم
(CaCO3)
(CaO)
CaCO3 CaO + CO2
[Na =
23, Cl = 35.5]
(NaCl) -:4انحم
NaCl
NaCl Na+ + Cl-](https://image.slidesharecdn.com/1-120515020920-phpapp01/85/1-6-320.jpg)
![يساجعت نهبئيت كيًيبء
)-(Cl
= [Zn
]5.53 = 65, Cl
انحم5:
)2(ZnCl
Zn + 2HCl 2ZnCl2 + H
يسبئم عهً انىحدة األوىل
]21 = [H = 1 , C
]61 = [Na = 23, C = 12, O
2CH
]1 = [C = 12, H
]61 = [N = 14, O
]1 = [N = 14, H
2CH
]1 = [C = 12, H](https://image.slidesharecdn.com/1-120515020920-phpapp01/85/1-7-320.jpg)
![يساجعت نهبئيت كيًيبء
[Mg = 24, S = 32, O = 16, H = 1]
[Zn = 65, S = 32, O = 16, H = 1]
2H2(g) + O2(g) 2H2O(g)
[S = 32 , O = 16] (SO2)
[Na = 23]
(Na2CO3)
[Na = 23, C = 12, O =16]
(Pb = 207)
[Mg = 24, H = 1, Cl = 35.5]
CH4 + 2O2 CO2 + 2H2O
[C = 12, H = 1, O = 16]
2H2 + O2 2H2O
وضح ببملعبدالث انسيصيت املىشونت](https://image.slidesharecdn.com/1-120515020920-phpapp01/85/1-8-320.jpg)




![يساجعت نهبئيت كيًيبء
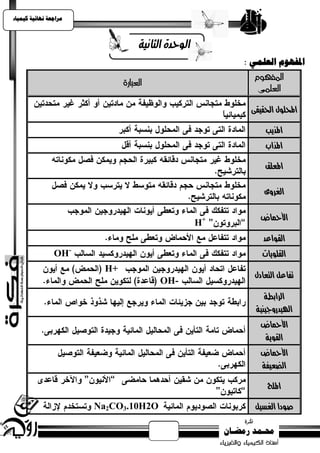
تصييف األمحاض
1] تقسيه األمحاض طبقاً لطبيعة ميشأها:-
[
أمحاض عضوية أمحاض معدىية املقارىة
ميشأها
HCl
CH3COOH
3HNO أمجلة
6C4H6O
4H2SO
7C6H8O
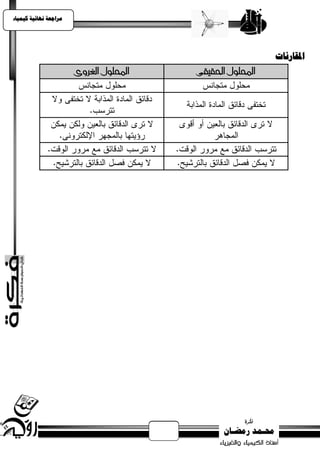
2] تقسيه األمحاض تبعاً لقوتها:-[
أمحاض ضعيفة أمحاض قوية املقارىة
التأيً
التوصيل
للكهرباء
CH3COOH HCl
3HNO أمجلة
3C3H6O 4H2SO](https://image.slidesharecdn.com/1-120515020920-phpapp01/85/1-15-320.jpg)
![يساجعت نهبئيت كيًيبء
3] تقسيه األمحاض تبعاً لعدد قاعديتها:-[
أمحاض ثالثية أمحاض ثيائية أمحاض أحادية
املقارىة
القاعدية القاعدة القاعدة
عدد الربوتوىات
)+(H
HCl
4H3PO 4H2SO
أمجلة
CH3COOH
7C6H8O 4H2C2O
3HNO](https://image.slidesharecdn.com/1-120515020920-phpapp01/85/1-16-320.jpg)
















![يساجعت نهبئيت كيًيبء
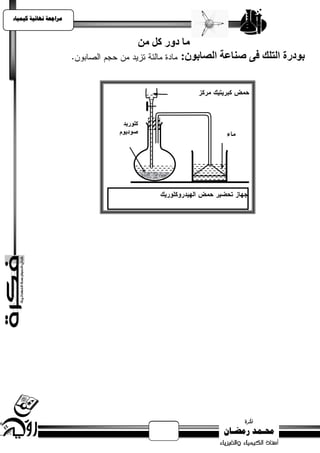
مسائل
]61 = [H = 1, S = 32, O
4H2SO
وصٌ انًزاة ثبنجشاو
انكزهخ انجضيئيخ انجشاييخ نهًزاة × حجى انزشكيض =
انًحهىل ثبنهزش
H
2N2 + 3H 32NH
.N N = 946 K. J., N – H = 390 K. J., H – H = 435 K.J
اىحو
H
|
N N + 3H – H 2 N–H
|
H
طبقخ كسش انشاثطخ
طبقخ ركىيٍ انشاثطخ
H
H
2CI2 + 2H2O 24HCl + O](https://image.slidesharecdn.com/1-120515020920-phpapp01/85/1-39-320.jpg)
![يساجعت نهبئيت كيًيبء
حشاسح ركىيٍ انًزفبعالد حشاسح ركىيٍ انُىارج
– H
Al2Cl6 + 6 Na .2Al + 6 NaCl, H = - 1074.6 K.J
اىحو
Al2Cl6 + 6 Na .2Al + 6 NaCl, H = - 1074.6 K.J
حشاسح ركىيٍ انًزفبعالد حشاسح ركىيٍ انُىارج
– H
–
]1 = [S = 32, O = 16, H
اىحو
]4[H2SO](https://image.slidesharecdn.com/1-120515020920-phpapp01/85/1-41-320.jpg)
![يساجعت نهبئيت كيًيبء
]32 = [H = 1, O = 16, Na
اىحو:-
][NaOH
)(KOH
)93 = (H = 1, O = 16, K
)Ag+NO3-(aq) + Na+Cl-(aq )Na+NO3-(aq) + AgCl(s
H = -35.6 kJ/mol
(أ) رشسيت 1.0 يىل يٍ كهىسيذ انفضخ. (ة) رشسيت 53.41 جى يٍ كهىسيذ انفضخ.
إرا عهًذ أٌ انكزم انزسيخ كبآلرً: }801 = {Cl = 35.5, Ag
اىحو
][AgCl](https://image.slidesharecdn.com/1-120515020920-phpapp01/85/1-42-320.jpg)

![يساجعت نهبئيت كيًيبء
C + O2 CO2, H = - 393.3 KJ
CO + ½ O2 CO2, H = - 283.7 KJ
N2O2, NO, NO2
N2 + 3H2 2NH3, Δ H = - 89 K.J.
H H
N H
ΔH
H2 + Br2 2HBr
H H
Br Br
H - Br
[H2SO4]
[H = 1, S = 32, O = 16]
Cl Cl
CH4 + Cl2 CH3Cl + HCl, Δ H = - 25 K.cal
CH3 - H
CH3 - Cl
H - Cl
N2 + O2 2NO, Δ H = + 180 K.J.](https://image.slidesharecdn.com/1-120515020920-phpapp01/85/1-44-320.jpg)
![يساجعت نهبئيت كيًيبء
C + O2 CO2, Δ H = - 393.5 K.J.
1
N2 + 3 H2 NH3, H = - 46.19 K J
2 2
2C + 2H2 C2H4, H = +52.3 K.J.
[Na = 23, H = 1, O = 16]
[Na = 23, H = 1, O = 16]
C3H8
C3H8 + 5 O2 3CO2 + 4H2O Δ H - 2228.5 K.J.
2C2H6 + 7O2 4CO2 + 6H2O Δ H - 2400 K.J.](https://image.slidesharecdn.com/1-120515020920-phpapp01/85/1-45-320.jpg)







![يساجعت نهبئيت كيًيبء
وضح اندوز انري يقىو به كم ين:
1] البلرتيا فى صياعة البيوداس:
[
2] رابع أيجيل الزصاص 4)5 Pb(C2Hعيد إضافتُ للذاسولني:
[
3] أىشيه األىفزتاس أثياء التخنز اللحوىل:[
4] األصطح الشدادية وتلويً غاس ثالح أكضيد اللربيت:
[
5] أكضيد امليذييش أو أكضيد األلومييوو أو الطفل فى التلضري احلفشى:[
6] أىشيه الشمياس أثياء التخنز اللحوىل:[
يب املقصىد بكم ين:
1] رقه أوكتاٌ لوقود 9
0 [
2] غاس البوتاداس:
[
3] الفزض العطوى ليشأة البرتول:[
انذالئم عهً صحخ انفشض انعضىي:
](https://image.slidesharecdn.com/1-120515020920-phpapp01/85/1-54-320.jpg)



