аром амінокислоти
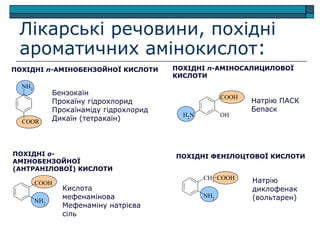
- 1. ПОХІДНІ ФЕНІЛОЦТОВОЇ КИСЛОТИ ПОХІДНІ п-АМІНОБЕНЗОЙНОЇ КИСЛОТИ ПОХІДНІ п-АМІНОСАЛИЦИЛОВОЇ КИСЛОТИ ПОХІДНІ о- АМІНОБЕНЗОЙНОЇ (АНТРАНІЛОВОЇ) КИСЛОТИ OHNH2 COOH NH2 COOR NH2 COOH NH2 CH2 COOH Бензокаїн Прокаїну гідрохлорид Прокаїнаміду гідрохлорид Дикаїн (тетракаїн) Натрію ПАСК Бепаск Кислота мефенамінова Мефенаміну натрієва сіль Натрію диклофенак (вольтарен) Лікарські речовини, похідні ароматичних амінокислот:
- 2. Бензокаїн етил 4-аминобензоат етиловий ефір n-амінобензойної кислоти 2 NH2 COOC2H5 Опис. Кристалічний порошок білого кольору. Викликає на язиці почуття заніміння. Розчинність. Дуже мало розчинний у воді, легко розчинний в спирті. NH2 C O O C2H5 Хімічні властивості Реакції на первинну ароматичну аміногрупу (діазотування та азосполучення; конденсація з ароматичними альдегідами) Реакції на бензольне кільце: бромування, йодування, нітрування та інш. Реакції на залишок етанолу: окиснення до ацетальдегіду, йодоформна проба, утворення етилацетату
- 3. Бензокаїн 3 NH2 COOC2H5 Здобування. Вихідною речовиною є толуол: NH2 C O O C2H5 CH3 CH3 NO2 NO2 COOH NO2 COOC2 H5 HNO3 H2SO4 K2Cr2O7 H2SO4 H2SO4 C2H5OH Fe CH3 COOH [H] ; толуол п-нітротолуол п-нітробензойна кислота етиловий ефір п-нітробензойної кислоти
- 4. 21 NH2 COOC2H5 1. Температура плавлення = 89 ... 92; 2. ІЧ-спектроскопія. C2 H5 OH [O] CH3 C O H Na2 [Fe(CN)5 NO] CH3 C O H Na2 [Fe(CN)5 CH2 COH]+ пиперазина гидрат Бензокаїн ІДЕНТИФІКАЦІЯ 3. Реакція на залишок етанолу: cубстанцію окислюють хрому (VI) оксидом та накривають пробірку папером, змоченим піперазина гідратом і натрію нитропруссидом. Спостерігається блакитне забарвлення:
- 5. 21 NH2 COOC2H5 Бензокаїн ІДЕНТИФІКАЦІЯ 4. Реакція на первинну ароматичну аміногрупу – утворення азобарвнику : N + N COOC2 H5 OH N N NaO COOC2H5 NH2 COOC2 H5 NaNO2 HCl Cl- NaOH
- 6. 21 NH2 COOC2H5 Бензокаїн ІДЕНТИФІКАЦІЯ 5. Реакція на первинну ароматичну аміногрупу – з ароматичними альдегідами утворення основи Шиффу: NH2 COOC2H5 C N CH3 CH3O H N COOC2H5 CH N CH3 CH3 H 2O + - основание Шиффа
- 7. 21 NH2 COOC2H5 Бензокаїн ІДЕНТИФІКАЦІЯ 6. Реакція на залишок етанолу, який можна виявити за йодоформною пробою (після гідролізу): + C2H5OH NH2 COONa NaOH NH2 COOC2H5 tº, C2H5OH + 4I2 + 6NaOH → CHI3↓ + 5NaI + HCOONa + 5H2O 7. При окисненні лікарської речовини розчином хлораміну в присутності кислоти хлористоводневої та ефіру – ефірний шар забарвлюється в оранжевий колір.
- 8. Кількісне визначення 1. Нітритометрія, пряме титрування В разі використання зовнішнього індикатору: 2KIO3 + 5NaNO2 + 2HCl → I2 + 5NaNO3 + 2KCl + H2O %вол.)-(100*н 100100*( % *22 .)... m TKVV дкNaNOдрNaNO ⋅⋅ = − Бензокаїн NH2 COOC2H5 індикатори: зовнішний-йодкрохмальний папір, внутрішні – тропеолін 00 або його суміш з метиленовим синім, або нейтральний червоний, s=1 N + N COOC2 H5 NH2 COOC2 H5 NaNO2 изб. HCl Cl-KBr ) мл г( 1000 Msc T у)(бензокаїн)(NaNO2 ⋅⋅ = Паралельно проводять контрольний дослід.
- 9. 9 Застосування в медицині Місцевоанестезуючий засіб Гастралгія, знеболювання слизових оболонок при спазмах та болях в шлунку, в т.ч. при виразковій хворобі та підвищеній чутливості стравоходу, біль при поверхневих ураженнях шкіри та слизових оболонок, міозити, захворювання поверхневих вен, геморой, тріщини заднього проходу, гостре запалення середнього вуха, біль в області зовнішнього слухового проходу; при діагностичних маніпуляціях на слизових оболонках (гастроскопія, ректоскопія, отоскопія, уретроскопія, гінекологічні процедури)
- 10. ПОХІДНІ ФЕНІЛОЦТОВОЇ КИСЛОТИ ПОХІДНІ п-АМІНОБЕНЗОЙНОЇ КИСЛОТИ ПОХІДНІ п-АМІНОСАЛИЦИЛОВОЇ КИСЛОТИ ПОХІДНІ о- АМІНОБЕНЗОЙНОЇ (АНТРАНІЛОВОЇ) КИСЛОТИ OHNH2 COOH NH2 COOR NH2 COOH NH2 CH2 COOH Бензокаїн Прокаїну гідрохлорид Прокаїнаміду гідрохлорид Дикаїн (тетракаїн) Натрію ПАСК Бепаск Кислота мефенамінова Мефенаміну натрієва сіль Натрію диклофенак (вольтарен) Лікарські речовини, похідні ароматичних амінокислот:
- 11. Прокаїну гідрохлорид (Procaini hydrochloridum) 2-Діетиламіноетил-4-амінобензоату гідрохлорид Властивості. Кристалічний порошок білого кольору або безбарвні кристали. На язиці викликає почуття заніміння. Дуже легко розчинний у воді, розчинний у 96% спирті, практично не розчинний в ефірі. Добування: з бензокаїну реакцією переетерификації β ди‑ етиламіноетанолом в присутності натрію алкоголяту: H2N COOCH2CH2N(C2H5)2H2N COOC2H5 HO-CH2-CH2-N C2H5 C2H5 àí åñòåçèí î ñí î âàí èå ï ðî êàèí à HCl H2N COOCH2CH2N(C2H5)2 HCl NH2 C O O CH2 CH2 N C2 H5 C2 H5 H Cl.
- 12. 12 NH2 C O O CH2 CH2 N C2 H5 C2H5 * HCl Прокаїну гідрохлорид (Procaini hydrochloridum) ІДЕНТИФІКАЦІЯ Фізико-хімічні методи: 1. Визначення Тпл, яка має бути від 154С до 158С. 2. Інфрачервоний спектр субстанції має відповідати спектру ФСЗ прокаїну.
- 13. Хімічні методи: 3. Реакція нітрування та утворення солі ортохіноїдної будови. Спостерігається коричневато-червоне забарвлення: ONH2 O R HNO3, t Co ONH2 O R O2 N O2 N KOH (спиртовой раствор) ONH O R N O2 N OK O _ + 4. Реакція знебарвлення розчину калію перманганату (відмінність від інших анестетиків). 5. Субстанція дає реакції на хлоріди: ІДЕНТИФІКАЦІЯ Cl- + AgNO3 → AgCl↓ + NO3 - AgCl + 2NH4 OH → [Ag(NH3 ) 2 ]Cl + 2H2 O
- 14. 14 6. Субстанція дає реакції на первинну ароматичну аміногрупу: 6.1 . Утворення азобарвника ІДЕНТИФІКАЦІЯ NH2 C O O CH2 CH2 N C2 H5 C2 H5 H Cl C O O CH2 CH2 N C2 H5 C2 H5 N + N H Cl OH NN NaO C O O CH2 CH2 N C2 H5 C2 H5 . NaNO2 HCl Cl- NaOH . 6.2 . Утворення основи Шиффу NH2 C O O CH2 CH2 N C2H5 C2 H5 C N CH3 CH3O H NCH C O O CH2 CH2 N C2 H5 C2 H5 N CH3 CH3 H 2 O + - основа Шиффа HCl
- 15. Кількісне визначення 1. Нітритометрія, пряме титрування, s=1 Можливі методи: 2. Алкаліметрія, пряме титрування у присутності хлороформу за фенолфталеїном. 3. Аргентометрія, пряме титрування у присутності кислоти оцтової розв., індикатор – бромфеноловий синій, s=1. 4. Ацидиметрія в неводному середовищі (CH3COOH, HCOOH), у присутності ртуті (ІІ) хлориду. Застосування. Місцевоанестезуючий засіб. При всмоктуванні і при безпосередньому введенні в кров впливає на весь організм у цілому. Зменшує утворення ацетилхоліну і знижує збудливість периферичних холінореактивних систем. Блокує вегетативні ганглії. Зменшує спазми гладкої мускулатури, знижує збудливість м'яза серця. NH2 C O O CH2 CH2 N C2H5 C2 H5 * HCl 6. Фізико-хімічні методи. 5. Зворотня броматометрія, зворотня йодхлорметрія.
