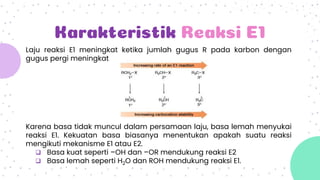
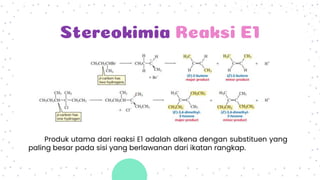
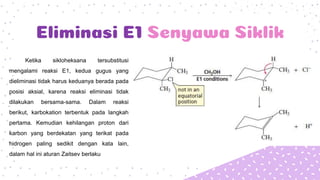
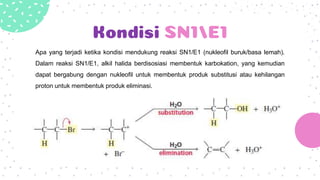
Reaksi eliminasi unimolekuler (E1) melibatkan pembentukan karbokation sebagai tahap penentu laju. Reaksi E1 memiliki dua tahap, pelepasan gugus pergi dan kemudian pembentukan ikatan rangkap. Karakteristik reaksi E1 adalah laju yang meningkat dengan bertambahnya gugus R dan basa lemah seperti air. Produk utama adalah alkena yang lebih tersubstitusi.

![Pendahuluan
Jenis reaksi eliminasi yang dapat dialami alkil halida adalah
eliminasi E1.
"E" adalah singkatan dari eliminasi dan "1" adalah singkatan dari
unimolekuler.
Tahap penentu laju pada reaksi E1 adalah tahap pertama, yaitu
tahap pembentukan karbokation. Karena tahap ini hanya
melibatkan satu molekul substrat saja, maka mekanisme reaksinya
disebut eliminasi unimolecular (E1)
rate = k [alkyl halide]](https://image.slidesharecdn.com/mekanismereaksie1-221218024637-624a2362/85/Mekanisme-Reaksi-E1-pptx-2-320.jpg)