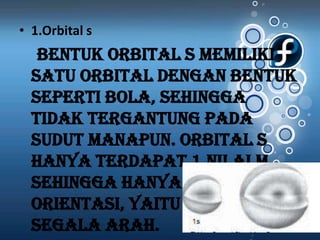
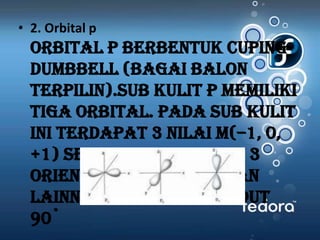
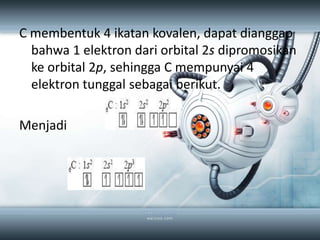
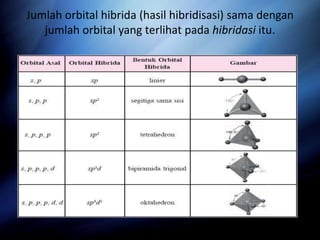
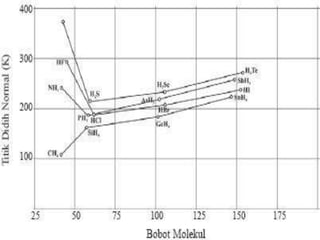
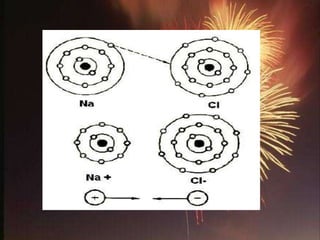
Dokumen tersebut membahas tentang struktur atom, sistem periodik unsur, ikatan kimia, dan konfigurasi elektron berdasarkan konsep bilangan kuantum seperti aturan Aufbau, aturan Pauli, dan aturan Hund. Secara khusus membahas tentang teori atom mekanika kuantum, diagram orbital, letak unsur dalam tabel periodik, bentuk geometri molekul, teori ikatan seperti VSEPR dan hibridisasi, serta jenis ikatan seperti ion, kovalen, hid