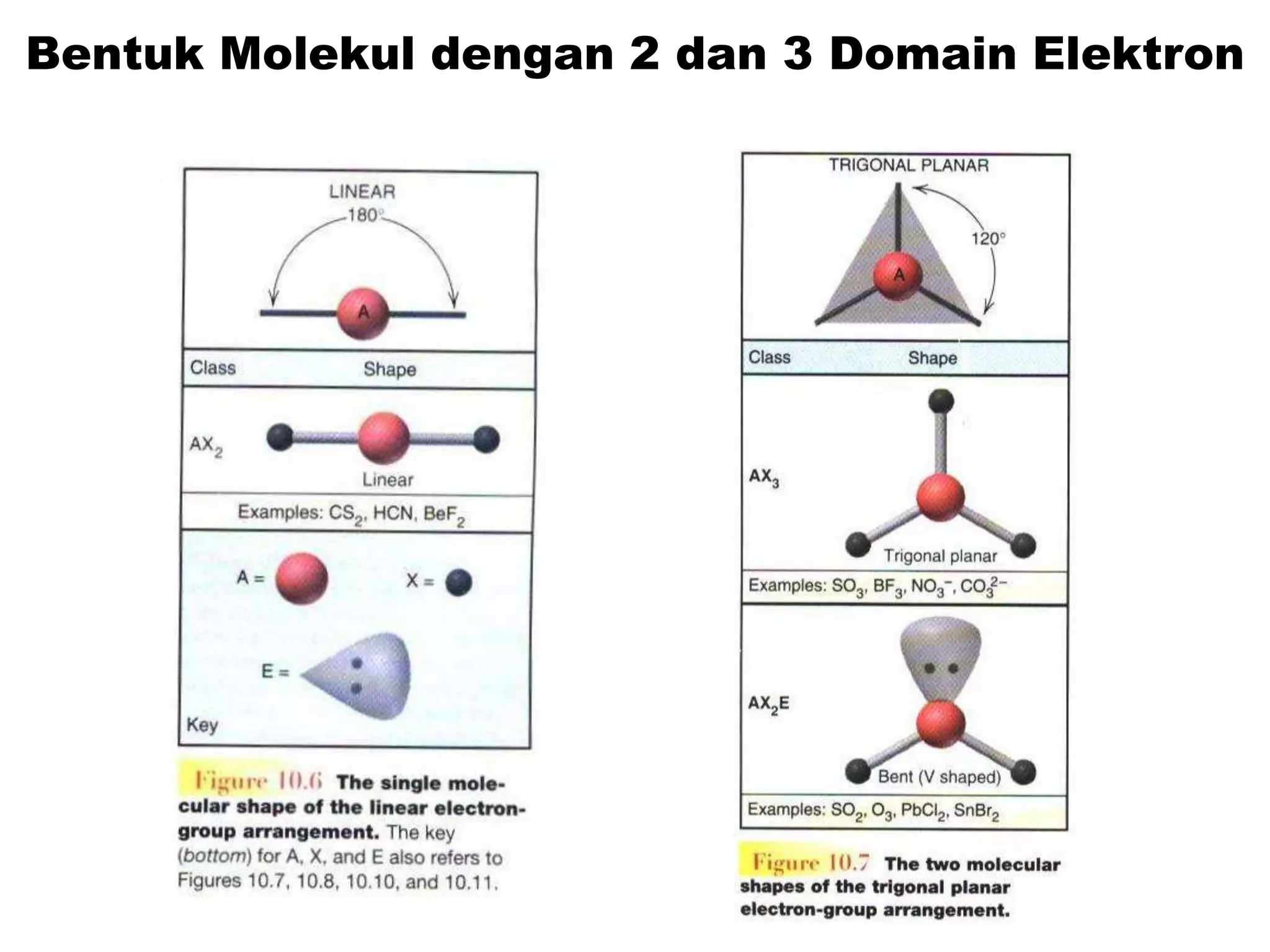
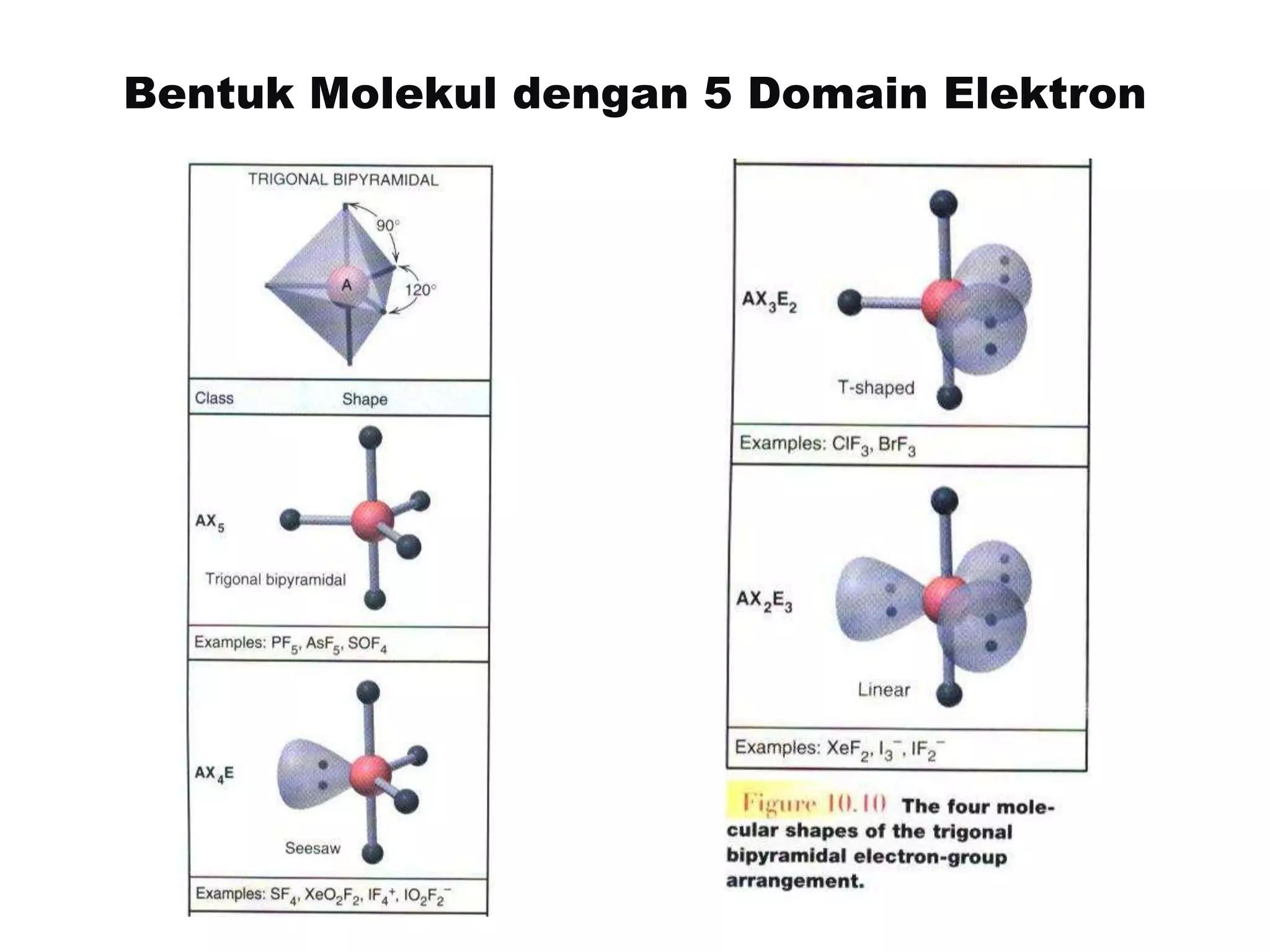
Ikatan kimia membentuk zat melalui berbagai jenis ikatan seperti ion, kovalen, dan logam untuk mencapai kestabilan. Teori domain elektron menjelaskan struktur molekul berdasarkan jumlah dan tipe elektron yang membentuk ikatan dan bebas. Rumusan tipe molekul dan geometri domain elektron digunakan untuk meramalkan bentuk molekul.