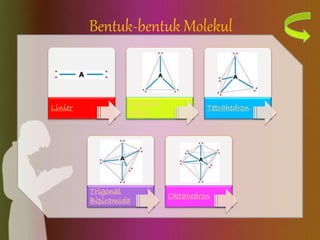
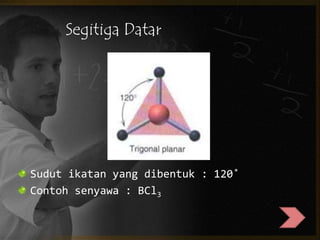
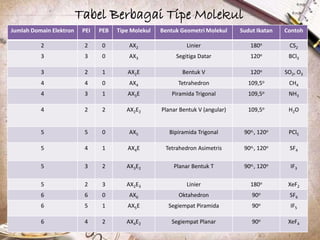
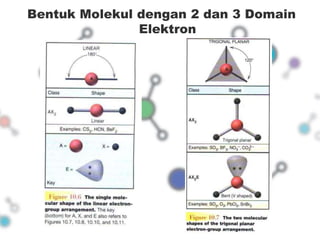
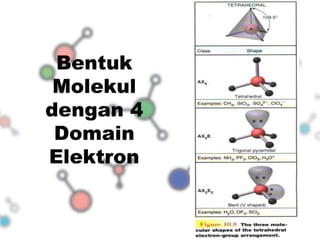
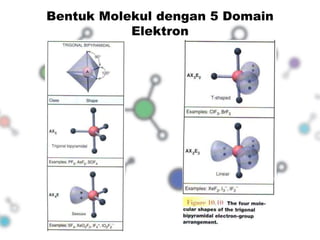
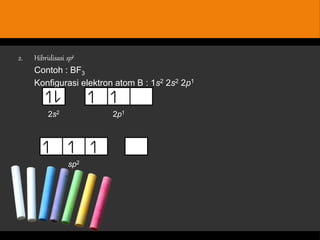
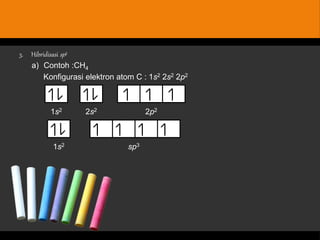
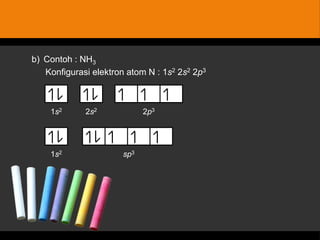
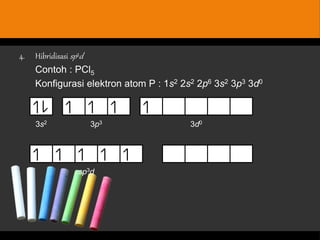
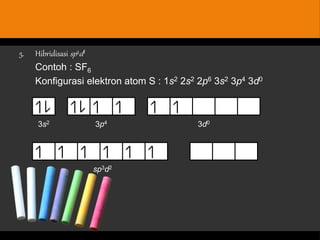
Dokumen tersebut membahas tentang bentuk struktur molekul, yang mencakup penjelasan tentang berbagai bentuk geometri molekul seperti linier, segitiga, tetrahedron, dan lainnya yang ditentukan oleh sudut ikatan antaratom dan jenis ikatan elektronnya. Dokumen ini juga menjelaskan teori domain elektron dan hibridisasi orbital yang dapat digunakan untuk memprediksi bentuk molekul.