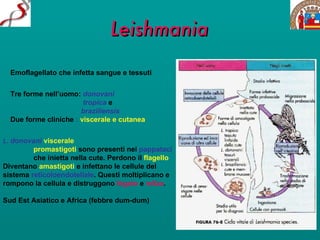
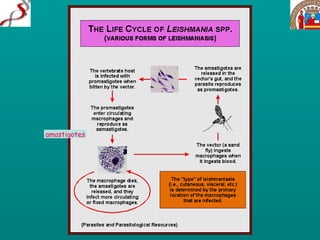
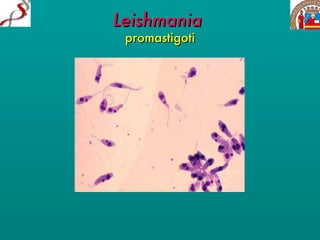
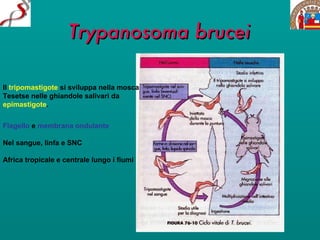
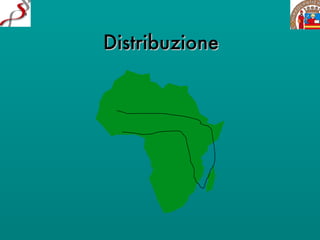
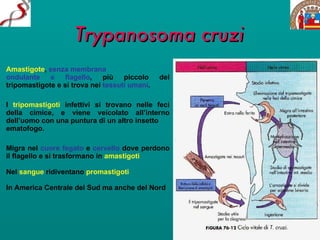
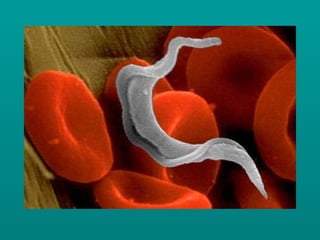
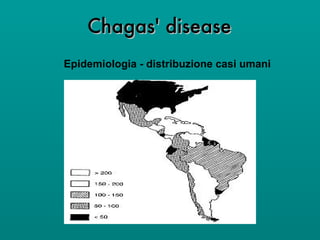
Il documento discute il ciclo di vita e l'epidemiologia di diverse specie di protozoi patogeni come Leishmania e Trypanosoma, evidenziando i vettori coinvolti e le manifestazioni cliniche delle malattie da essi causate, come leishmaniosi e malattia di Chagas. Si menzionano le forme cliniche della leishmaniosi, inclusa quella viscerale e cutanea, che colpiscono milioni di persone in tutto il mondo. Inoltre, vengono descritti i sintomi e le complicanze associate alle infezioni, così come le modalità di trasmissione delle malattie.