تناقش الوثيقة موضوع تصنيف العناصر في الجدول الدوري، حيث تبرز مستويات الطاقة الرئيسية والفرعية، وتوضح كيفية ترتيب العناصر بناءً على الأعداد الذرية. تتناول أيضًا الفئات الأربعة لعناصر الجدول الدوري وهي العناصر الممثلة، النبيلة، الانتقالية، والداخلية، مع شرح خصائصها وتوزيعاتها الإلكترونية. يقدم النص أمثلة متنوعة ليوضح تركيب الإلكترونات في العناصر المختلفة.

![فى احلسام سلسلةالكيمياءMr. Hossam Sewify
الثانىالباب:العناصروتصنيف الدورىاجلدولالثانوىالثانىالصف
1
•وجودللطاقة مستويات سبعةالريئسيةهى(K. L. M. N. O. P. Q)
•اكتشافللطاقة الحقيقية المستوياتوالفرعية المستويات هى)مستوى (تحت(s. p. d. f).
•إلى التوصلالبن مبدأالتصاعدى اءبحيثوجدك يزيدبإلكترون يسبقه الذى العنصر عن عنصر ل.واحد
فإن ولذلكاجلدول بناء أساس:
[1]الذرية أعدادها حسب تصاعديا العناصر ترتيب.
[2التصاعدى البناء مبدأ الجدول فى العناصر ترتيب ويوافق ].
:الفرعية املستويات ترتيب تذكر
الثانىالبابالدورى اجلدولوتالعناصر صنيف
1s 2s < 2p 3s < 3p 4s < 3d < 4p
5s < 4d < 5p 6s < 4f < 5d < 6p 7s < 5f < 6d
الدورى اجلدول بناءالطويل
2
8
8
18
18
32
32
عدد
العناصر
1
2
3
4
5
6
7
رقم
الدورة
الرئيسية اإلنتقالية العناصر
الداخلية اإلنتقالية العناصر
الاملمثلة عناصر النبيلة العناصراملمثلة العناصر
اللنثانيدات
األكتينيدات](https://image.slidesharecdn.com/2018-171013000838/75/2018-2-2048.jpg)
![فى احلسام سلسلةالكيمياءMr. Hossam Sewify
الثانىالباب:العناصروتصنيف الدورىاجلدولالثانوىالثانىالصف
2
العناصر فئاتالعناصر أنواع
fdpsممثلةنبيلة
انتقالية
رئيسية
انتقالية
داخلية
•ينمعينة خبواص تتميز )(مناطق فئات أربع إىل اجلدول قسم.
[1]الفئة عناصر(s):
•الجدول يسار فى تقع.
•الفرعى المستوى فى الخارجية إلكتروناتها تقع التى العناصر على تحتوى(s)
•المجموعتين فى توجد1A . 2A
المجموعة 1A 2A
اإللكترونى تركيبها (ns1
) (ns2
)
حيث(n)الوقت نفس فى الدورة ورقم األخير المستوى رقم.
الصوديوم :مثالNa11اإللكترونى التوزيع1s2
2s2
2p6
3s1
[2الفئة عناصر ](p):
•الجدول من اليمنى المنطقة تشغل.
•ال فى الخارجية إلكتروناتها تقع التى العناصر على تحتوىالفرعى مستوى(p)
•ستة من تتكونمجموعاتالمستوى (ألن رأسية(p))إلكترونات لست يتسع
•:المجموعات فى توجد
المجموعة 3A 4A 5A 6A 7A المجموعة(0)
اإللكترونى تركيبها (np1
) (np2
) (np3
) (np4
) (np5
) (np6
)
العناصر فئات
العناصر ترتيبالدورى اجلدولالطويل
f1
f2
f3
f4 5
f 6
f 7
f 8
f 9
f 10
f 11
f 12
f 13
f 14
f
6
7
s1
2s1
2
3
4
5
6
7
d1
d2
d3
d4
d5
d6
d7
d8
d9
d10
s2
P6P5P4P3P2P1
d
p
f
s](https://image.slidesharecdn.com/2018-171013000838/75/2018-3-2048.jpg)
:
•الجدول من الوسطى المنطقة تشغل.
•على تحتوىالفرعى المستوى فى الخارجية إلكتروناتها تقع التى العناصر(d)
•للمجموعات (سبعة رأسية مجموعات عشرة من تتكون(B)وثالثةصفوفالثام المجموعة لعناصرن)ة
•اإلنتقالية العناصر تسمىالرئيسيةإلى وتنقسمسالسل ثالثهى:
األوىل االنتقالية السلسلةالثانية االنتقالية السلسلةالثالثة االنتقالية السلسلة
3d4d5d
الرابعة الدورة فى تقعالخامسة الدورة فى تقعالسادسة الدورة فى تقع
اإلسكانديوم من العناصر تشمل
(Sc)الخارصين حتى(Zn)
اليوتريوم من العناصر تشمل
(Y)الكادميوم حتى(Cd)
اللنثانيوم من العناصر تشمل
(La)الزئبق حتى(Hg)
[4الفئة عناصر ](f):
•.السادسة الدورة من تبدأ
•ًالطوي يكون ال لكى الجدول تحت تفصل ًاغالب.
•الفرعى المستوى فى الخارجية إلكتروناتها تقع التى العناصر على تحتوى(f)يستوعب الذى14ًاإلكترون.
•:هما سلسلتين من تتكون
لنثينيداتاكتينيدات
•السادسة الدورة فى توجد
•ويتتابعالفرعى المستوى امتالء فيها(4f)من تتكون لذلك
(14ًاعنصر )
•هتتو الختتارجى تكافاهتتا مستتتوى)2
s6(ةتتديدة فهتتى ولتتذا
بعناصتتتر ستتتميت ولتتتذلك فصتتتلها يصتتتعب ولتتتذلك التشتتتابه
خاطئة تسمية وهى النادرة األكاسيد.
•السابعة الدورة فى توجد
•الفرعتى المستوى امتالء فيها ويتتابع
(5f)تتكون لذلك( من14ًاعنصر )
•غيتر وأنويتهتا مشتعة عناصتر جميعها
مستقرة.
:هى العناصر من أنواع أربعة إىل اجلدول فى العناصر تقسم-
[1النبيلة العناصر ]:
•عناصرالمجموعةاألخيرةالفئة عناصر من(p)أو الصفرية (المجموعة18).
•اإللكترونى تركيبها)6
(npالهيليوم ماعدا)2
s1(.
•تتميزباإللكترونات الطاقة مستويات جميع بإمتالء.
•الصعوبة بغاية مركبات وتكون ًاتمام مستقرة عناصر.
النيون :مثالNe10اإللكترونى التوزيع1s2
.2s2
.2p6
[2املمثلة العناصر ]:
•الفئة عناصر وهى(s) . (p)الصفرية المجموعة عناصر ماعدا.
•باإل الطاقة مستويات جميع بامتالء تتميزاألخير الطاقة مستوى ماعدا لكترونات.
•الفرعى المستوى إمتالء فيها يتتابع(s. p)
العناصر أنواع](https://image.slidesharecdn.com/2018-171013000838/75/2018-4-2048.jpg)
![فى احلسام سلسلةالكيمياءMr. Hossam Sewify
الثانىالباب:العناصروتصنيف الدورىاجلدولالثانوىالثانىالصف
4
•الوصول إلى تميلاإللكترونى التركيب إلى)6
np2
(nsالخارجية لمستويتهااكتساب أو بفقد وذلكاإللكترونتاتأو
بالمشاركة.
الصوديوم :مثالNa11:اإللكترونى التوزيع1s2
. 2s2
. 2p6
. 3s1
مثالاأللومنيوم :Al13:اإللكترونى التوزيع1s2
. 2s2
. 2p6
. 3s2
. 3p1
الكلور :مثالCl17:اإللكترونى التوزيع1s2
. 2s2
. 2p6
. 3s2
. 3p5
[3الرئيسية االنتقالية العناصر ]:
•الفئة عناصر هى(d)حيثالفرعى المستوى امتالء فيها يتتابع(d)
•با الطاقة مستويات جميع بامتالء تتميزللطاقة رئيسيين مستويين آخر ماعدا إللكترونات.
:مثالالحديدFe261s2
. 2s2
. 2p6
. 3s2
. 3p6
. 4s2
. 3d6
K L M N
2 8 14 2
مكتمل مكتمل مكتمل غير مكتمل غير
[4الداخلية االنتقالية العناصر ]:
•الفرعى المستوى امتالء فيها يتتابع(f)
•الطاقة مستويات جميع بامتالء تتميزرئيسية مستويات ثالثة آخر ماعدا باإللكترونات.
العناصر وأنواع فئات يوضح جدول
الفئةالنوعالفئة عناصر خواصالدورة فى عددها
الفئة
s
ممثلة عناصرالفرعى المستوى تشغل الخارجية إلكتروناتها(s)
عنصران
ns1
. ns2
الفئة
p
ممثلة عناصر
المست تشغل الخارجية إلكتروناتهاالفرعى وى(p)
5عناصر
np1
: np5
نبيلة عناصر
واحد عنصر
6
np
الفئة
d
انتقالية عناصر
رئيسية
الفرعى المستوى تشغل الخارجية إلكتروناتها(d)
10عناصر
nd1
: nd10
الفئة
f
انتقالية عناصر
داخلية
الفرعى المستوى تشغل الخارجية إلكتروناتها(f)
14ًاعنصر
nf1
: nf14](https://image.slidesharecdn.com/2018-171013000838/75/2018-5-2048.jpg)
![فى احلسام سلسلةالكيمياءMr. Hossam Sewify
الثانىالباب:العناصروتصنيف الدورىاجلدولالثانوىالثانىالصف
5
( مثال1:)-التعليل مع العنصر نوع ًامبين التالية العناصر لذرات اإللكرتونى التوزيع اكتب
11Na. 18Ar. 25Mn. 40Zr. 35Br. 58Ce. 64Gd
:احلل-
العنصراإللكرتونى التوزيعالتعليل مع العنصر نوع
11Na[10Ne] 3s1تتةتفئ تتلتممث تترتعنص(s)تتتوىتالمس تتىتف تتلتمكتم تترتغي تتهتألنتتىتالفرع(s)
مكتمل غير األخير الرئيسى والمستوى.
18Ar[10Ne] 3s2
. 3p6األ المستوى ألن نبيل عنصرباإللكترونات مكتمل )(الثالث خير
إلكترونات {عددs + p=8}
25Mn[18Ar] 4s2
. 3d5( )األولى االنتقالية السلسلة (من رئيسى انتقالى عنصر3d)مكتمل غير
الرئيسي والمستويين)والرابع (الثالث مكتملين غير األخيرين ين
35Br[18Ar] 4s2
. 3d10
. 4p5
فئة ممثل عنصر(p)مكتمل غير األخير الرئيسى الطاقة ومستوى.
58Ce[54Xe] 6s2
. 4f1
. 5d1اللنثينيتدات من داخلى انتقالى عنصر(4f)الرئيستية مستتويات والثالثتة
والخام الرابع وهى مكتملة غير األخيرةوالسادس س.
64Gd[54Xe] 6s2
. 4f7
. 5d1اللنثينيتدات من داخلى انتقالى عنصر(4f)الرئيستية مستتويات والثالثتة
والسادس والخامس الرابع وهى مكتملة غير األخيرة
:من اجلدول يتكون-
:أفقية دورات-
•)الرئيسية المستويات عدد مع (يتفق دورات سبع عددها
•الع عن عنصر كل فيزيدواحد بإلكترون الدورة نفس فى يسبقه الذى نصر.
•.جديد رئيسى بمستوى دورة كل تبدأ
•الخامل الغاز وهو األخير العنصر إلى نصل حتى الفرعية المستويات ملء الواحدة الدورة فى ويتتابع.
•.الرئيسية المستويات عدد فى الواحدة الدورة عناصر تتفق
الدورةالرئيسية املستويات عدداملستالرئيسية وياتالعناصر عدد
األولى1K2
الثانية2K. L8
الثالثة3K. L. M.8
الرابعة4K. L. M. N18
الخامسة5K. L. M. N. O18
السادسة6K. L. M. N. O. P32
السابعة7K. L. M. N. O. P. Q32
:األفقية الدورة-
أفقي مرتبة اخلواص متشابه غري عناصر عدةالذرى العدد فى الزيادة حسب ًا
جمموعات:رأسية-
•عددها18.مجموعة
وصفالدورى اجلدولالطويل](https://image.slidesharecdn.com/2018-171013000838/75/2018-6-2048.jpg)
![فى احلسام سلسلةالكيمياءMr. Hossam Sewify
الثانىالباب:العناصروتصنيف الدورىاجلدولالثانوىالثانىالصف
6
•تىتاألساس تمتالك تددتع تىتف تتتختل تنتولك ترتاألخي تىتالفرع تةتالطاق تتوىتمس تىتف تدةتالواح تةتالمجموع ترتعناص تقتتتف
.)(الرئيسى
اإللكرتونى التوزيعالرمزالعنصر
[2He] 2s1
3Liالليثيوم
[10Ne] 3s1
11Naالصوديوم
[18Ar] 4s1
19Kالبوتاسيوم
[36Kr] 5s1
37Rbالروبيديوم
•.ًاغالب الكيميائية الخواص فى الواحدة المجموعة عناصر تتفق
:الرأسية اجملموعة-
األخري الطاقة مستوى إلكرتونات عدد فى متشابهة ألنها اخلواص فى متشابهة عناصر عدة
(س1:)-:اآلتية للعبارات العلمى املفهوم اكتب-
1-عدةواحد آخربمقدار عن عنصر كل يزيد بحيث الذرية أعدادها فى الزيادة حسب تصاعدية مرتبة عناصر.
2-اآلخيرين المستويين ماعدا باإللكترونات الرئيسية المستويات جميع فيها يكتمل التى العناصر مجموعة.
3-الفرعى المستوى امتالء فيها يتتابع العناصر من سلسلة(4f)باإللكترونات(04/)ثان
4-الفئة عناصر(f)الفرعى المستوى امتالء فيها يتتابع حيث(4f)باإللكترونات(07/)أول
(س2: )-:)العلمى السبب (اذكر يأتى ملا علل-
1-الكيميائية الخواص فى متشابهة الالنثانيدات عناصر.
2-عناصر ثمانية على الثانية الدورة تشمل.
3-عنص عشر ثمانية على الرابعة الدورة تشتملًار.
4-على السادسة الدورة تشتمل32ًاعنصر.
5-الفئة عناصر(s)الفئة عناصر بينما مجموعتين تشمل(p)مجموعات ست تشمل.
6-الرابعة الدورة من بداية الرئيسية االنتقالية العناصر ظهور يبدأالثالثة وليس.
(س3:)-:املناسب لالختيار األجبدى احلرف اكتب-
(1)الو المجموعة عناصر تتشابهعدد فى الدورى الجدول فى احدة....
التكافا إلكترونات )(أالبروتونات )(بالطاقة مستويات )(جالنيوترونات )(د.
(2)عدد فى الواحدة الدورة عناصر تتشابه...
التكافا إلكترونات )(أالبروتونات )(بالطاقة مستويات )(جالنيوترونات )(د.
(3)الفئة عناصر تسمى(d)…… :(97/)أول
الممثلة العناصر )(أاالنتقالية العناصر )(بالنبيلة العناصر )(جاألكتينيدات )(د
(4)الفرعى المستوى امتالء يبدأ التى العناصر(d)عناصر عليها يطلق لها……(02/)ثان
رئيسية انتقالية )(أممثلة )(بنبيلة )(جداخلية انتقالية )(د
(5)لمستوي اإللكترونى التوزيع عنصرالخارجية طاقته ات2
s61
d57
f4عناصر من يكون…(08/)س
األولى االنتقالية السلسلة )(أ.االكتينيدات سلسلة )(ب
الالنثانيدات سلسلة )(ج.الثالثة االنتقالية السلسلة )(د.
(6)اإللكترونى تركيبه عنصر14
f43
d52
s6Xe54من يكون…(08/)أول
ا االنتقالية السلسلة )(أألولى.االكتينيدات سلسلة )(ب
الالنثانيدات سلسلة )(ج.الثالثة االنتقالية السلسلة )(د.
(7)العنصرX86هو الخارجية الطاقة مستويات فى اإللكترونات توزيع يكون……
األسئلة](https://image.slidesharecdn.com/2018-171013000838/75/2018-7-2048.jpg)


![فى احلسام سلسلةالكيمياءMr. Hossam Sewify
الثانىالباب:العناصروتصنيف الدورىاجلدولالثانوىالثانىالصف
9
من املسافة بأنه الذرة قطر نصف تعريف اخلطأ من وبالتاىل النواة حول اإللكرتون موقع حتديد ميكن ال أنه أظهرت املوجية النظرية
إلكرتون أبعد إىل النواة.
قطر نصف تعريف:الذرة-
:الرابطة طول-
األنجستروم بوحدة الرابطة طول وتقدرǺ
:األيونية الرابطة طول-
أو
•األيونى القطر بنص المقاس القطر نص ويسمى.
•المكتسبة أو المفقودة اإللكترونات عدد على األيونى القطر نصف يعتمد.
الراب وطول القطر نصف بني العالقةطة
[1:الذرتني متاثل حالة فى ]-
= الرابطة طول2×القطر نص
= القطر نص
[2:التماثل عدم حالة فى ]-
الثانية للذرة نق + األولى للذرة نق = الرابطة طول
نق1الرابطة طول =–نق2
نق2الرابطة طول =–نق1
( مثال1:)-الك جزئ فى الرابطة طول أن علمت إذالور[Cl - Cl]يساوى1.98أجنسرتوم
الكلور وذرة الكربون ذرة بني الرابطة وطول[C - Cl]يساوى1.76أجنسرتوم–الكربون ذرة قطر نصف أحسب
:الحل-
ن= الكلور ذرة قطر ص==0.99أنجستروم
الكربون ذرة قطر نصوالكلور الكربون رابطة طول =–ا ذرة قطر نصلكلور
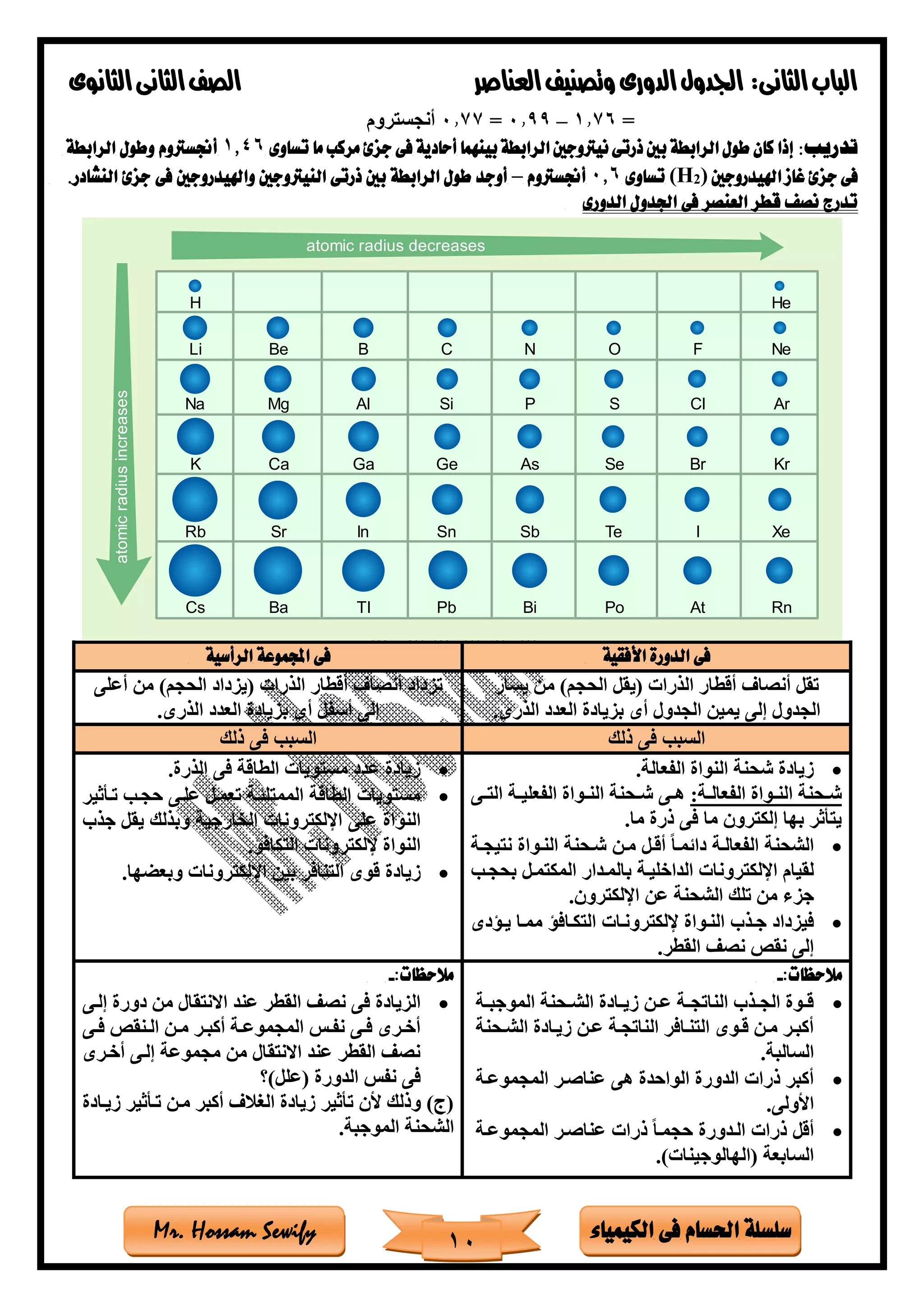
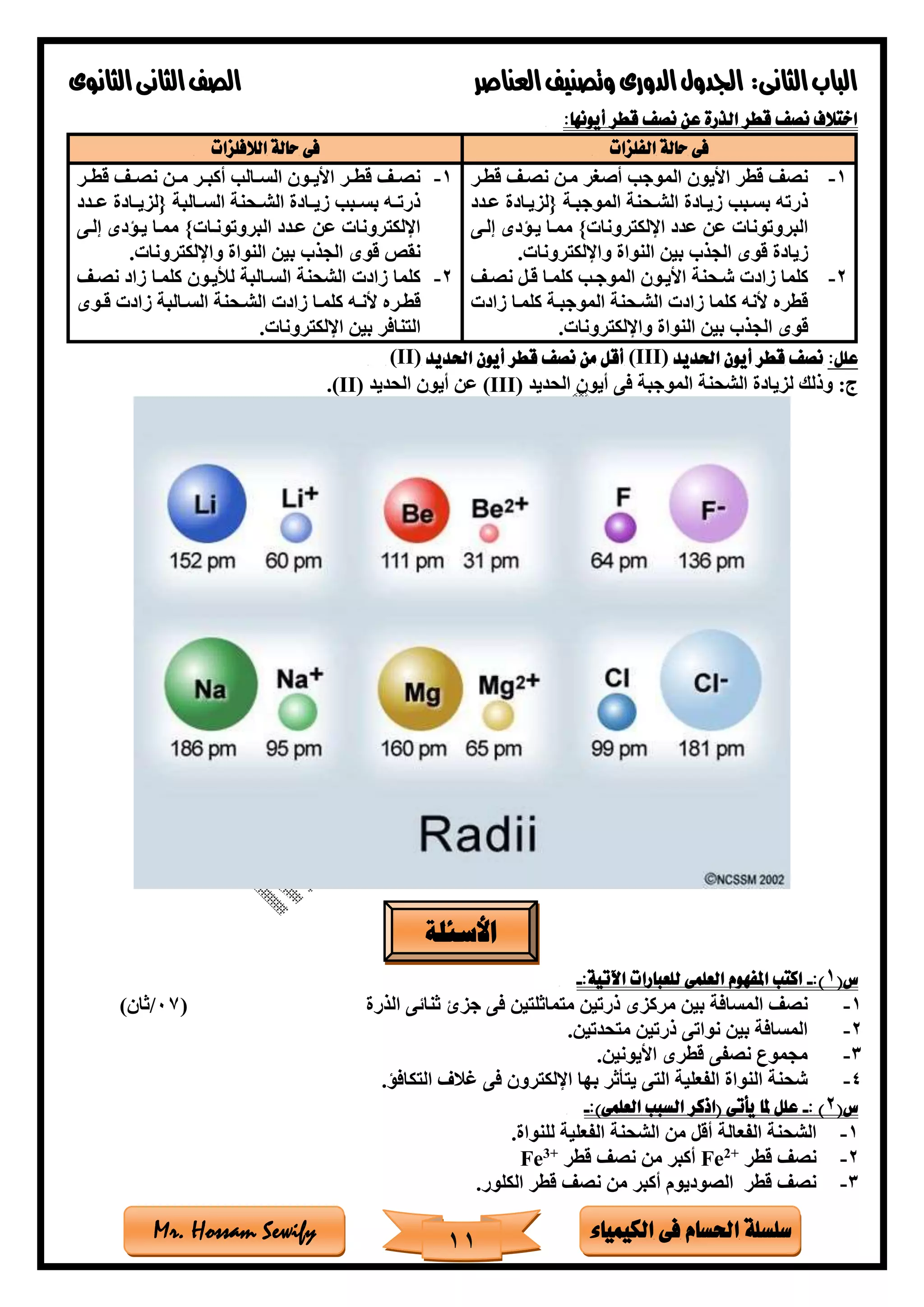
الدورى اجلدول فى اخلواص تدرج
الذرة قطر نصف :ًالأو
الرابطة طول
ب
نق
سص
ص نق س نق
الرابطة طول
2
1.98
2
الذرة ثنائى جزئ فى متماثلتني ذرتني مركزى بني املسافة نصف
هىمتحدتني ذرتني نواتى بني املسافة
متحدين أيونني مركزى بني املسافة هىاأليونني قطرى نصفى جمموع تساوى](https://image.slidesharecdn.com/2018-171013000838/75/2018-10-2048.jpg)

![فى احلسام سلسلةالكيمياءMr. Hossam Sewify
الثانىالباب:العناصروتصنيف الدورىاجلدولالثانوىالثانىالصف
13
6-الماء جزئ فى الرابطة طول كان إذا الهيدروجين لذرة التساهمى القطر نص احسب1.96وطول أنجستروم
األكسجين جزئ فى الرابطة1.36أنجستروم.(10/)أول
=======================================================
7-الكلور جزئ فى الرابطة طول كانت إذا1.98ا وطول أنجستروموالكربون الكلور بين لرابطةC - Cl
يساوى1.76الكربون ذرة قطر نص احسب أنجستروم
=======================================================
8-النيتريك أكسيد جزئ فى الرابطة طول كان إذا(NO)1.36األكسجين جزئ فى الرابطة وطول أنجستروم
1.32ذرة قطر نص احسب أنجسترومالنيتروجين جزئ فى الرابطة طول استنتج ثم النيتروجين.
(11/)أول
=======================================================
9-= النشادر جزئ فى الرابطة طول كان إذا1الماء جزئ وفى أنجستروم0.96Aالهيدروجين جزئ وفى0.6
Aالنيتريك أكسيد جزئ فى الرابطة طول يكون فكم(NO)
========================================================
10-تساوى ما مركب جزئ فى أحادية بينهما الرابطة نيتروجين ذرتى بين الرابطة طول كان إذا1.46Aوطول
تساوى الهيدروجين جزئ فى الرابطة0.6Aفى والهيدروجين النيتروجين ذرتى بين الرابطة طول أوجد
النشادر جزئ.
========================================================
11-أيونى قطر نص أن علمت إذا++
Mg.++
Crيساوى72.0،84.0Aالرابطة طول وأن الترتيب على
يساوى الماغنسيوم أكسيد جزئ فى األيونية2.12:أنجستروم
][أالكروم أكسيد جزئ فى األيونية الرابطة طول احسب.
][بأجزئ فى الرابطة ًالطو أكثر يهماCrOأم3O2Cr
======================================================
12-تونتالكرب تىتذرت تينتب تةتالرابط تولتط تبتاحسC)-(Cتةتالرابط تولتط تذلكتوكH)-(Cتانتاإليث تزئتج تىتف6H2Cإذا
يساوى الهيدروجين جزئ فى الرابطة طول :أن علمت0.6الرابط وطول أنجستروميستاوى الكلتور جزئ فى ة
98.1انجستروم.الكربون كلوريد رابع جزئ فى الرابطة وطول4CClيساوى1انجستروم.
======================================================
13-يساوى الهيدروجين فلوريد جزئ فى الرابطة طول بأن ًاعلم الفلور جزئ فى الرابطة طول احسب0.94
أنجستروم.وطيساوى الهيدروجين جزئ فى الرابطة ول0.6انجستروم
=========================================================
14-أيون قطر نص أن علمت إذا+
Liيساوى68.0يساوى الطعام ملح جزئ فى الرابطة وطول أنجستروم
76.2الصوديوم أيون قطر نص وأن أنجستروم+
Naيساوى95.0أنجسترومفى الرابطة طول احسب
الليثيوم كلوريد جزئ.
(س6:اآلتية العبارات أكمل :)
(1)الموجب األيون قطر نص……السالب األيون قطر نص بينما ،المتعادلة ذرته قطر نص من……من
المتعادلة ذرته قطر نص.
(2)فى ًاحجم الذرات أكبر تقع……فى ًاحجم وأصغرها الجدول……الجدول.
(س7العنصر )وهو اإللكرتونى الرتكيب نفس هلا التالية واأليونات6
p32
s36
p22
s22
s1:احلجم حسب ًاتصاعدي فرتبها
Ar. K+
. Cl-
. S2-
. Ca2+
(س8حسب السبب ذكر مع ًاتصاعدي اآلتية واأليونات العناصر رتب :):قطرها نصف-
(1)Ca20.Al13.Mg12(2)+3
Fe.Fe.+2
Fe
(س19( عالمة ضع :)عال أو )( مة:اخلطأ تصويب مع )
(1)منها إلكترون وأبعد النواة بين المسافة هو الذرة قطر نص.
(2)المتعادلة ذرته قطر نص من أصغر الصوديوم أيون قطر نص.](https://image.slidesharecdn.com/2018-171013000838/75/2018-14-2048.jpg)




![فى احلسام سلسلةالكيمياءMr. Hossam Sewify
الثانىالباب:العناصروتصنيف الدورىاجلدولالثانوىالثانىالصف
19
:أمثلة-
البورونالسليكوناجلرمانيومالزرنيخأنتيمونتيلوريوم
BSiGeAsSbTe
والال الفلزية الصفة تدرجالدورى اجلدول فى فلزية
األفقية الدورة فىالرأسية اجملموعة فى
اليمين إلى اليسار من اتجهنا كلما الفلزية الصفة تقل
تظهر حتى القطر نص ونقص الذرى العدد بزيادة أى
وتنتهى الالفلزية الصفة تزداد ثم الفلزات أةباه
)الالفلزات (أقوى السابعة بالمجموعة
الفلز الصفة تزيداتجهنا كلما الالفلزية الصفة وتقل ية
نص وكبر الذرى العدد بزيادة أى أسفل إلى أعلى من
القطر
:مالحظات-
•السيزيوم وهو الجدول يسار أسفل يقع الدورى الجدول فى الفلزات أقوى.
•الفلور وهو الجدول يمين أعلى يقع الجدول فى الالفلزات أقوى.
األكاسيد أنواع:-[1حامضية ].[2قاعدية ].[3مترددة ].
:احلامضية األكاسيد-
•:مثل الالفلزات أكاسيد هى-5O2P.3SO.2SO.2CO
•:ًاأحماض وتعطى الماء فى تذوب-)الحامضية األكاسيد الالفلزات أكاسيد تسمى (لذلك
CO2 + H2O H2CO3 )الكربونيك (حمض
SO2 + H2O H2SO3 )الكبريتوز (حمض
SO3 + H2O H2SO4 )الكبريتيك (حمض
P2O5 + 3H2O 2H3PO4 )األرثوفسفوريك (حمض
•:ًءوما ًاملح وتعطى القلويات مع تتفاعل-
CO2 + NaOH Na2CO3 + H2O
SO2 + 2NaOH Na2SO3 + H2O
:القاعدية األكاسيد-
•:مثل الفلزات أكاسيد هى-CuO.O2K.O2Na.MgO
•:قلويات ويكون الماء فى يذوب بعضها-)قلوية (أكاسيد
والقاعدية احلامضية اخلاصية :ًاسادس
الالفلزية الصفة تزيد
الفلزية الصفة تقل
الالفلزيةالصفةتقل
الفلزيةالصفةتزيد
الفلزات أقوى
الالفلزات أقوى](https://image.slidesharecdn.com/2018-171013000838/75/2018-20-2048.jpg)
![فى احلسام سلسلةالكيمياءMr. Hossam Sewify
الثانىالباب:العناصروتصنيف الدورىاجلدولالثانوىالثانىالصف
20
Na2O + H2O 2NaOH
K2O + H2O 2KOH
CaO + H2O Ca(OH)2
MgO + H2O Mg(OH)2
•:مثل الماء فى يذوب ال بعضها-PbO.O2Ag.3O2Fe.CuO
•:ًءوما ًاملح منتجة األحماض مع القاعدية األكاسيد تتفاعل-
Na2O + 2HCl 2NaCl + H2O
MgO + H2SO4 MgSO4 + H2O
:املرتددة األكاسيد-
وماء ملح احلالتني فى وينتج حامضية كأكاسيد القلويات مع وتتفاعل قاعدية كأكاسيد األمحاض مع تتفاعل التى األكاسيد هى
SnO3O2SbZnO3O2Al
قصدير أكسيدأنتيمون أكسيد ثالثزنك أكسيدألومنيوم أكسيد
ZnO(s) + H2SO4(aq) ZnSO4(aq) + H2O(l)
ZnO(s) + 2NaOH(aq) Na2ZnO2(aq) + H2O(l)
الصوديوم خارصينات
الدورى اجلدول فى والقاعدية احلامضية اخلواص تدرج
[1:األفقية الدورة فى ]-
ليك القاعدية الصفة تقل الذرى العدد بزيادة)الجتدول يمتين إلى يسار (من ليكاسيد الحامضية الصفة تزداد بينما اسيد
)القطر نص (لنقص الالفلزية الصفة وزيادة الفلزية الصفة لضع وذلك
[2:الرأسية اجملموعة فى ]-
األوىل اجملموعةالسابعة اجملموعة
وذلك الذرى العدد بزيادة القاعدية الخاصية تزداد
الق نص زيادة بسببقوى وضع الذرى طر
مما الهيدروكسيد ومجموعة العنصر بين الترابط
الهيدروكسيد أيون انفصال سهولة إلى يادى
السالب
وذلك الذرى العدد بزيادة الحامضية الخاصية تزداد
قوى وضع الذرى القطر نص زيادة بسبب
يادى مما الهيدروجين وأيون العنصر بين الترابط
أيون انفصال سهولة إلىالموجب الهيدروجين
ضعي قلوىLiOH
اخلاصية تزداد
القاعدية
ضعي حمضHF
اخلاصية تزداد
احلامضية
قوى قلوىNaOHمتوسط حمضHCl
قوة أكثر قلوىKOHقوى حمضHBr
قوة أكثر قلوىRbOHأقوى حمضHI
القلويات أقوىCsOH
مركبا والقواعد األكسجينية األمحاضهيدروكسيلية ت
العامة بالصيغة تمثيلها يمكن(MOH)
حيث(M)العنصر ذرة هى
:يلى كما تأينها فيمكن
[1:قاعدة وتعترب هيدروكسيد أيونات تعطى ]
MOH M+
+ OH-
بتين الجتذب قتوة كانتت إذا)-
O.+
(Hبتين الجتذب قتوة متن أكبتر)-
O.+
(M
ا تتأينكقاعدة لمادة.
M +
O -
H +](https://image.slidesharecdn.com/2018-171013000838/75/2018-21-2048.jpg)
![فى احلسام سلسلةالكيمياءMr. Hossam Sewify
الثانىالباب:العناصروتصنيف الدورىاجلدولالثانوىالثانىالصف
21
:مثال-قتوة فتضتع موجبتة واحتدة ةتحنة إال تحمتل وال كبيتر التذرة حجتم يكتون الصتوديوم مثتل القلويتة الفلتزات فتى
وبين بينها الرابطة)-
(Oأيون تعطى وبذلك الهيدروجين أليون أكثر تنجذب والتى)-
(OHكقاعدة تتأين أى
NaOH Na+
+ OH-
[2وتع هيدروجني أيونات تعطى ]:ًاحامض ترب
MOH MO-
+ H+
بين الجذب قوة كانت إذا)-
O.+
(Mبين الجذب قوة من أكبر)-
O.+
(Hكحمض المادة تتأين.
:مثال-ةتحنتها وتتزداد يقتل حجمهتا الكلتور مثتل الالفلزات ذرات أن نجد الدورى الجدول فى اليمين ناحية اتجهنا كلما
إلى انجذابها يزداد وبذلك)-
(Oأيون تعطى وبذلك)+
(Hكحامض تتأين أى.
ClOH ClO-
+ H+
[3:تتأين املادة فإن اجلذب قوتا تساوت إذا ]-
:احلمضى الوسط فى ][أ-كقاعدة.
:القلوى الوسط فى ][ب-كحامض.
)(متردد األلومنيوم هيدروكسيد :مثال3(OH)2Al
العن ذرة على السابقة الجذب قوى تعتمد:حيث من صر-
•الحجم.
•الكهربية الشحنة مقدار.
:األكسجينية األمحاض قوة-
اهليدروجني بذرات املرتبطة غري األكسجني ذرات عدد على األكسجينية األمحاض قوة تعتمد
:األكسجينية لألمحاض العامة الصيغة-
MOn(OH)m
:حيث-(M):العنصر ذرة هى)n(Oاألكسجين ذرات عدد :
األق الحمضبالهيدروجين المرتبطة غير األكسجين ذرات من أكبر عدد على يحتوى الذى هو :وى.
احلمضصيغتهاألكسجينية صيغتة
ذرات عددOغري
بذ املرتبطةH
قوةاحلمض
األرثوسليكونيكH4SiO4Si(OH)4--ضعي حمض
األرثوفسفوريكH3PO4PO(OH)31متوسط حمض
الكبريتيكH2SO4SO2(OH)22حمقوى ض
البيروكلوريكHClO4ClO3(OH)3ًاجد قوى حمض
(س1:)-:اآلتية للعبارات العلمى املفهوم اكتب-
1-الالفلزات خواص ومعظم الفلزات مظهر لها عناصر
2-باإللكترونات سعته نص من بأقل تكافاها غالف يمتل التى العناصر مجموعة
3-تكافاها غالف يمتل التى العناصر مجموعةباإللكترونات سعته نص من بأكثر(06/)أول
4-موجبتين ةحنتين يحمل أيون لتكوين موجب أيون من إلكترون لنزع الالزمة الطاقة مقدار
(س2: )-:)العلمى السبب (اذكر يأتى ملا علل-
1-كهروموجبة وعناصر للكهرباء التوصيل جيدة الفلزات
2-الالفلزات أقوى والفلور الفلزات أقوى السيزيوم
3-أكاأللومنيوم سيد3O2Alمتردد أكسيد
األسئلة](https://image.slidesharecdn.com/2018-171013000838/75/2018-22-2048.jpg)

![فى احلسام سلسلةالكيمياءMr. Hossam Sewify
الثانىالباب:العناصروتصنيف الدورىاجلدولالثانوىالثانىالصف
24
:أمثلة-
المركبNaClMgO3O2Al
األيونات-
Cl+
Na2–
O+2
Mg2–
O+3
Al
التأكسد عدد-1+1-2+2-2+3
املوجبة األيوناتالسالبة األيونات
الفلزات جميع أيونات.
األمونيوم مجموعة+
4NH
الهيدروجين أيون+
H
الالفلزات جميع أيونات.
الذرية المجموعات باقى.
•الموجب التأكسد عددالذرة فقدتها التى اإللكترونات عدد على يدل.
•عددالسالب التأكسدالذرة اكتسبتها التى اإللكترونات عدد على يدل.
:التساهمية املركبات فى :ًاثاني-
:الرابطة فى اإللكترونية اإلزاحة تبين الذرة تحملها التى الشحنة فإن سالبة أو موجبة أيونات يوجد ال-
سالبة ةحنة تحمل كهربية سالبية األكثر الذرة ][أ.
سا األقل الذرة ][بموجبة ةحنة تحمل لبية.
[1:المتماثل الجزىء حالة فى ]-
صفر = ذرة لكل التأكسد عدد
ألن متستاوية التذرات بتين الروابط فى اإللكترونية اإلزاحة تكونالستالبية فتى متستاوية واحتد لعنصتر جتزئ أى ذرات
:الكهربية
الهيدروجين جزئ فى الهيدروجين تأكسد عددصفر =
تأكسد عددالكلور جزئ فى الكلورصفر =
األكسجين جزئ فى األكسجين تأكسد عددصفر =
[2:مختلفتان الذرتان كانت إذا ]-
:بحيث كهربية سالبية األكثر الذرة مع المشاركة اإللكترونات تحسب-
•سالبة جزئية ةحنة عليها يتكون سالبية األكثر الذرة.
•ةحنة عليها يتكون سالبية األقل الذرةموجبة جزئية.
الكربون أكسيد ثانى جزئ2COالماء جزئO2H
OCO
242
•
•
HOH
11
2
تأكسد عدد(O)=-2
تأكسد عدد(C)+ =4
تأكسد عدد(O)=-2
تأكسد عدد(H)+ =1
H H
Cl Cl
O
O
](https://image.slidesharecdn.com/2018-171013000838/75/2018-25-2048.jpg)
![فى احلسام سلسلةالكيمياءMr. Hossam Sewify
الثانىالباب:العناصروتصنيف الدورىاجلدولالثانوىالثانىالصف
25
النشادر جزئ3NHالهيدروجين أكسيد فوق جزئ2O2H
1H
HNH
11
3
•
•
•
•
•
HOOH
11
11
تأكسد عدد(N)=-3
تأكسد عدد(H)+ =1
تأكسد عدد(O)=-1
تأكسد عدد(H)+ =1
:مالحظات-
[1( :مركباته معظم فى األكسجين تأكسد عدد ]-2:اآلتية الحاالت ماعدا )-
( = تأكسده عدد يكون األكسيد فوق حالة فى )(أ-1)
:مثال-الهيدروجي أكسيد فوقن)2O2(Hالصوديوم أكسيد فوق)2O2(Na
= أكسيد السوبر حالة فى )(ب(−
𝟏
𝟐
)
:مثالالبوتاسيوم أكسيد سوبر)2(KO
األكسجين فلوريد حالة فى )(ج)2(OF+( = تأكسده عدد يكون2)
ليكسجين الكهربية السالبية من أكبر للفلور الكهربية السالبية ألن.
[2الهيدرو تأكسد عدد ]+( :مركباته معظم فى جين1)
( = الهيدروجين تأكسد عدد يكون الفلزات هيدريدات ماعدا-1)
للفلز الكهربية السالبية من أكبر تكون الحالة هذه فى للهيدروجين الكهربية السالبية ألن وذلك.
:مثل-الصوديوم هيدريد(NaH)الكالسيوم هيدريد)2(CaH
•تحت أيونية مركبات الهيدريداتوىالسالب الهيدروجين أيون على.
•المصعد عند الهيدروجين يتصاعد ًاكهربي وتحليلها صهرها عند.
HNa
11
•
HCaH
121
•
•
[3صفر = ذراته عدد كان مهما )(المنفردة الذرية الحالة فى عنصر ألى التأكسد عدد ]
(S8. P4. O3. Cl2. H2. Fe)
[4صفر = المتعادل المركب جزئ تأكسد عداد ]
[5تىتاألول تةتالمجموع ترتعناص تدتتأكس تددتع ](A)+( ًاتتدائم تاتمركباته تىتف1تةتالثاني تةتالمجموع ترتوعناص )(A)+(2)
الثالثة المجموعة وعناصر(A)+(3)
[6موج بإةارة عليه التى الشحنات عدد = عنصر أى أليون التأكسد عدد ]سالبة أو بة
[7:سالبة أو موجبة بإةارة المجموعة تحملها التى الشحنة = الذرية للمجموعات التأكسد عدد ]-
اجملموعةاألمونيومالكربيتاتالكربوناتالنيرتات
صيغتهاNH4
+
SO4
- 2
CO3
- 2
NO3
-
تأكسدها عدد+1-2-2-1
[8]ف فقط ًاواحد أيونا أو واحدة ذرة يخص التأكسد عددالجزئ ى.](https://image.slidesharecdn.com/2018-171013000838/75/2018-26-2048.jpg)
![فى احلسام سلسلةالكيمياءMr. Hossam Sewify
الثانىالباب:العناصروتصنيف الدورىاجلدولالثانوىالثانىالصف
26
التأكسد أعداد حساب طريقة
مثال(1:)-البوتاسيوم كرومات ثانى فى الكروم تأكسد عدد احسب)7O2Cr2(K
:الحل-
متعادل المركبصفر = تأكسده عدد
7O2Cr2Kصفر =
({7×-2+ )2( + س2+ ×1صفر = })
-14+2+ س2صفر =-12+2صفر = س+ = س6
+ = البوتاسيوم كرومات ثانى فى الكروم تأكسد عدد6
مثال(2:)-فى الكربيت تأكسد عدد احسب2-
3SO
:الحل-
المتأينة مجموعة= تأكسدها عدد-2
({3×-2= }س + )-2-6= س +-2
= س6–2+ =4
+ = الكبريتيت مجموعة فى الكبريت تأكسد عدد4
:ملحوظة:املركب نفس فى تأكسد حالة من أكثر الواحد للعنصر يكون قد
األمونيوم نيترات فى النيتروجين :مثال3NO4NH
[NO3]-
[NH4]+
3×-2= س +-1
+ =س6–1
+ = س5
4×1+ = س +1
= س-4+1
= س-3
∴النيتروج تأكسد عدد+( يكون األمونيوم نيترات فى ين5،-3)
:التأكسد عدد استخدام مميزات-
الكيميائية التفاعالت أثناء واالختزال التأكسد حيث من للعنصر حيدث الذى التغري معرفة
التأكسداالختزال
فى زيادة عنها ينتج إلكترونات فقد عملية هو
الموجبة الشحنة
ينتج إلكترونات اكتساب عملية هوفى نقص عنها
الموجبة الشحنة
مثال1:-:التاىل التفاعل فى واحلديد الكروم من لكل واختزال أكسدة من احلادث التغري نوع بني-
K2Cr2O7 + 6FeCl2 + 14 HCl 2KCl + 2CrCl3 + 6FeCl3 + 7H2O
:احلل-
(1:للكروم بالنسبة )-
:فى الكروم تأكسد عدد حساب7O2Cr2K
({7×-2+ )2( + س2+ ×1صفر = })-14+2+ س2صفر =
-12+2صفر = س+ = س6
+ = البوتاسيوم كرومات ثانى فى الكروم تأكسد عدد6
:فى الكروم تأكسد عدد حساب3CrCl
({3×-1صفر = }س + )+ = س3
K2Cr2O7 CrCl3
Cr + 6
Cr +3
+( من نقص الكروم تأكسد عدد6إ )+( لى3اختزال عملية له حدث أى )
(2:للحديد بالنسبة )-
FeCl2 FeCl3
Fe+2
Fe+3](https://image.slidesharecdn.com/2018-171013000838/75/2018-27-2048.jpg)
![فى احلسام سلسلةالكيمياءMr. Hossam Sewify
الثانىالباب:العناصروتصنيف الدورىاجلدولالثانوىالثانىالصف
27
+( من زاد الحديد تأكسد عدد2+( إلى )3أكسدة عملية له حدث أى ).
مثال2::واملختزل املؤكسد العامل ًامبين التاىل التفاعل فى واختزال أكسدة من حدث ما بني
CH4 + 2O2 → CO2 + 2 H2O
احلل:
[ :الكربون تأكسد عدد1( المتفاعالت فى ]-4)[2+( النواتج فى ]4)
للكربون أكسدة حدث)مختزل عامل (الكربون
[ األكسجين تأكسد عدد1)(صفر المتفاعالت فى ][2( النواتج فى ]-2)
ليكسجين اختزال حدث)ماكسد عامل (األكسجين
والمتفاعال النواتج فى الهيدروجين تأكسد عدد+( يتغير لم ت1).
مثال3::التاىل التفاعل فى واختزال أكسدة من ماحدث بني
[NH4]+
[NO3]-
N2O + 2H2O
مثال4:واملختزل املؤكسد العامل حتديد مع التالية التفاعالت فى واختزال أكسدة من حدث ما بني
[1] 3H2S + 2NO3
–
+ 2H+
3S + 2NO + 4H2O
[2] MnO2 + 4 HBr MnBr2 + Br2 + 2 H2O
:ملحوظة
والرتسيب التعادل تفاعالت مثل إختزال أو أكسدة تفاعالت تعترب ال التفاعالت أنواع بعض
:التعادل تفاعل
قاعدة + محض+ ماء + ملح……
NaOH + HCl NaCl + H2O
Na2CO3 + 2HCl 2NaCl + H2O + CO2
:الرتسيب تفاعل
مصحوب يكون تفاعلراسب بتكوين
NaCl + AgNO3 NaNO3 + AgCl
(س1:)-:اآلتية للعبارات العلمى املفهوم اكتب-
1-الموجب الشحنة فى زيادة عنها ينشأ إلكترونات فقد عملية.(96/)ثان
2-الموجبة الشحنة فى نقص عنها ينتج إلكترونات اكتساب عملية.
3-تب التى الكهربية الشحنة يمثل الذى العددالمركب أو الذرة على دو
4-األيونى أو التساهمى المركب فى الذرة على تبدو التى )سالبة أو (موجبة الكهربية الشحنة يمثل عدد.
(11/)س
(س2: )-:)العلمى السبب (اذكر يأتى ملا علل-
1-فى سالب الكلور تأكسد عدد(HCl)فى وموجب)7O2(Cl
2-للماغن مركبات على الحصول يصعب+( بها تأكسده عدد سيوم3).
3-اسكانديوم أيون على الحصول الصعب من+4
ScSc)21((08/)س
األسئلة](https://image.slidesharecdn.com/2018-171013000838/75/2018-28-2048.jpg)