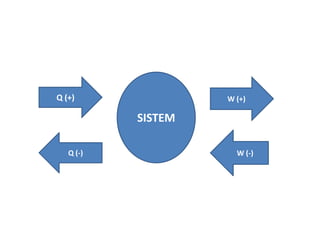
Dokumen tersebut membahas hukum pertama termodinamika, termasuk definisi hukum tersebut, perubahan energi dalam sistem, dan penerapannya pada berbagai proses termodinamika seperti isotermal, isokorik, isobarik, dan adiabatik. Juga dibahas kapasitas kalor dan besaran-besarannya untuk gas.