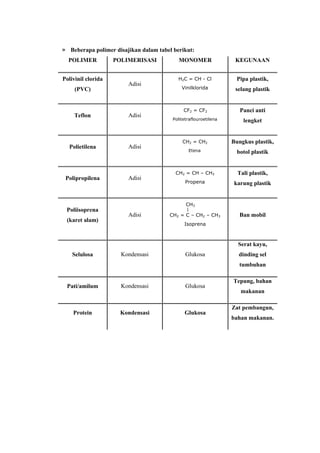
Dokumen ini membahas makromolekul, terutama polimer, yang terdiri dari monomer terkait melalui reaksi polimerisasi adisi dan kondensasi. Polimer diklasifikasikan berdasarkan asal, jenis monomer, kegunaan, dan sifat termal, dan contohnya meliputi karet, plastik, dan protein. Penulis juga mengeksplorasi faktor yang mempengaruhi sifat polimer, termasuk panjang rantai, susunan, dan penambahan zat aditif.















![Glutamina (Gln, Q)
] Asam amino basa
Lisina (Lys, K)
Arginina (Arg, R)
Histidina (His, H) (memiliki gugus siklik)
Asam amino dengan sulfur
Sisteina (Cys, C)
Metionina (Met, M)
Prolin
Prolina (Pro, P) (memiliki gugus siklik)
Asam amino aromatik
Fenilalanina (Phe, F)
Tirosina (Tyr, Y)
Triptofan (Trp, W)
Kelompok ini memiliki cincin benzena dan menjadi bahan baku metabolit sekunder
aromatik.
Fungsi biologi asam amino
1. Penyusun protein, termasuk enzim.
2. Kerangka dasar sejumlah senyawa penting dalam metabolisme (terutama vitamin,
hormon dan asam nukleat).
3. Pengikat ion logam penting yang diperlukan dalam dalam reaksi enzimatik
(kofaktor).
Asam amino esensial](https://image.slidesharecdn.com/makalahkimia-120618000941-phpapp01/85/Makalah-kimia-17-320.jpg)

![penghubugn lainnya
- Bersama dengan Vitamin C membentuk L-Carnitine
- Membantu dalam pembentukan kolagen maupun jaringan penghubung tubuh lainnya
(cartilage dan persendian)
5. Tyyptophan
- Pemicu serotonin (hormon yang memiliki efek relaksasi)
- Merangsang pelepasan hormon pertumbuhan
6. Methionine
Protein (asal kata protos dari bahasa Yunani yang berarti "yang paling utama") adalah
senyawa organik kompleks berbobot molekul tinggi yang merupakan polimer dari
monomer-monomer asam amino yang dihubungkan satu sama lain dengan ikatan peptida.
Molekul protein mengandung karbon, hidrogen, oksigen, nitrogen dan kadang kala sulfur
serta fosfor. Protein berperan penting dalam struktur dan fungsi semua sel makhluk hidup
dan virus.
Kebanyakan protein merupakan enzim atau subunit enzim. Jenis protein lain berperan
dalam fungsi struktural atau mekanis, seperti misalnya protein yang membentuk batang
dan sendi sitoskeleton. Protein terlibat dalam sistem kekebalan (imun) sebagai antibodi,
sistem kendali dalam bentuk hormon, sebagai komponen penyimpanan (dalam biji) dan
juga dalam transportasi hara. Sebagai salah satu sumber gizi, protein berperan sebagai
sumber asam amino bagi organisme yang tidak mampu membentuk asam amino tersebut
(heterotrof).
Protein merupakan salah satu dari biomolekul raksasa, selain polisakarida, lipid, dan
polinukleotida, yang merupakan penyusun utama makhluk hidup. Selain itu, protein
merupakan salah satu molekul yang paling banyak diteliti dalam biokimia. Protein
ditemukan oleh Jöns Jakob Berzelius pada tahun 1838.
Biosintesis protein alami sama dengan ekspresi genetik. Kode genetik yang dibawa DNA
ditranskripsi menjadi RNA, yang berperan sebagai cetakan bagi translasi yang dilakukan
ribosom.[1] Sampai tahap ini, protein masih "mentah", hanya tersusun dari asam amino](https://image.slidesharecdn.com/makalahkimia-120618000941-phpapp01/85/Makalah-kimia-19-320.jpg)
![proteinogenik. Melalui mekanisme pascatranslasi, terbentuklah protein yang memiliki
fungsi penuh secara biologi.[2][3]
Struktur
Struktur tersier protein. Protein ini memiliki banyak struktur sekunder beta-sheet dan
alpha-helix yang sangat pendek. Model dibuat dengan menggunakan koordinat dari Bank
Data Protein (nomor 1EDH).
Struktur protein dapat dilihat sebagai hirarki, yaitu berupa struktur primer (tingkat satu),
sekunder (tingkat dua), tersier (tingkat tiga), dan kuartener (tingkat empat): [4][5]
struktur primer protein merupakan urutan asam amino penyusun protein yang
dihubungkan melalui ikatan peptida (amida). Frederick Sanger merupakan
ilmuwan yang berjasa dengan temuan metode penentuan deret asam amino pada
protein, dengan penggunaan beberapa enzim protease yang mengiris ikatan antara
asam amino tertentu, menjadi fragmen peptida yang lebih pendek untuk
dipisahkan lebih lanjut dengan bantuan kertas kromatografik. Urutan asam amino
menentukan fungsi protein, pada tahun 1957, Vernon Ingram menemukan bahwa
translokasi asam amino akan mengubah fungsi protein, dan lebih lanjut memicu
mutasi genetik.](https://image.slidesharecdn.com/makalahkimia-120618000941-phpapp01/85/Makalah-kimia-20-320.jpg)
![struktur sekunder protein adalah struktur tiga dimensi lokal dari berbagai
rangkaian asam amino pada protein yang distabilkan oleh ikatan hidrogen.
Berbagai bentuk struktur sekunder misalnya ialah sebagai berikut:
o alpha helix (α-helix, "puntiran-alfa"), berupa pilinan rantai asam-asam
amino berbentuk seperti spiral;
o beta-sheet (β-sheet, "lempeng-beta"), berupa lembaran-lembaran lebar
yang tersusun dari sejumlah rantai asam amino yang saling terikat
melalui ikatan hidrogen atau ikatan tiol (S-H);
o beta-turn, (β-turn, "lekukan-beta"); dan
o gamma-turn, (γ-turn, "lekukan-gamma").[4]
struktur tersier yang merupakan gabungan dari aneka ragam dari struktur
sekunder. Struktur tersier biasanya berupa gumpalan. Beberapa molekul protein
dapat berinteraksi secara fisik tanpa ikatan kovalen membentuk oligomer yang
stabil (misalnya dimer, trimer, atau kuartomer) dan membentuk struktur
kuartener.
contoh struktur kuartener yang terkenal adalah enzim Rubisco dan insulin.
Struktur primer protein bisa ditentukan dengan beberapa metode: (1) hidrolisis protein
dengan asam kuat (misalnya, 6N HCl) dan kemudian komposisi asam amino ditentukan
dengan instrumen amino acid analyzer, (2) analisis sekuens dari ujung-N dengan
menggunakan degradasi Edman, (3) kombinasi dari digesti dengan tripsin dan
spektrometri massa, dan (4) penentuan massa molekular dengan spektrometri massa.
Struktur sekunder bisa ditentukan dengan menggunakan spektroskopi circular dichroism
(CD) dan Fourier Transform Infra Red (FTIR).[6] Spektrum CD dari puntiran-alfa
menunjukkan dua absorbans negatif pada 208 dan 220 nm dan lempeng-beta
menunjukkan satu puncak negatif sekitar 210-216 nm. Estimasi dari komposisi struktur
sekunder dari protein bisa dikalkulasi dari spektrum CD. Pada spektrum FTIR, pita
amida-I dari puntiran-alfa berbeda dibandingkan dengan pita amida-I dari lempeng-beta.
Jadi, komposisi struktur sekunder dari protein juga bisa diestimasi dari spektrum
inframerah.
Struktur protein lainnya yang juga dikenal adalah domain. Struktur ini terdiri dari 40-350
asam amino. Protein sederhana umumnya hanya memiliki satu domain. Pada protein yang
lebih kompleks, ada beberapa domain yang terlibat di dalamnya. Hubungan rantai](https://image.slidesharecdn.com/makalahkimia-120618000941-phpapp01/85/Makalah-kimia-21-320.jpg)
![polipeptida yang berperan di dalamnya akan menimbulkan sebuah fungsi baru berbeda
dengan komponen penyusunnya. Bila struktur domain pada struktur kompleks ini
berpisah, maka fungsi biologis masing-masing komponen domain penyusunnya tidak
hilang. Inilah yang membedakan struktur domain dengan struktur kuartener. Pada struktur
kuartener, setelah struktur kompleksnya berpisah, protein tersebut tidak fungsional.
Kekurangan Protein
Protein sendiri mempunyai banyak sekali fungsi di tubuh kita. Pada dasarnya protein
menunjang keberadaan setiap sel tubuh, proses kekebalan tubuh. Setiap orang dewasa
harus sedikitnya mengonsumsi 1 g protein per kg berat tubuhnya. Kebutuhan akan protein
bertambah pada perempuan yang mengandung dan atlet-atlet.
Kekurangan Protein bisa berakibat fatal:
Kerontokan rambut (Rambut terdiri dari 97-100% dari Protein -Keratin)
Yang paling buruk ada yang disebut dengan Kwasiorkor, penyakit kekurangan
protein.[7] Biasanya pada anak-anak kecil yang menderitanya, dapat dilihat dari
yang namanya busung lapar, yang disebabkan oleh filtrasi air di dalam pembuluh
darah sehingga menimbulkan odem.Simptom yang lain dapat dikenali adalah:
o hipotonus
o gangguan pertumbuhan
o hati lemak
Kekurangan yang terus menerus menyebabkan marasmus dan berkibat kematian.
Manfaat Protein
Manfaat protein bagi tubuh kita sangatlah banyak. Protein sangat mempengaruhi proses
pertumbuhan tubuh kita. Diantara manfaat protein tersebut adalah sebagai berikut:
Sebagai enzim. Protein memiliki peranan yang besar untuk mempercepat reaksi
biologis.](https://image.slidesharecdn.com/makalahkimia-120618000941-phpapp01/85/Makalah-kimia-22-320.jpg)



![adipokina, antara lain kemerin, interleukin-6, plasminogen activator inhibitor-1, retinol
binding protein 4 (RBP4), tumor necrosis factor-alpha (TNFα), visfatin, dan hormon
metabolik seperti adiponektin dan hormon adipokinetik (Akh).
Sifat dan Ciri ciri
Karena struktur molekulnya yang kaya akan rantai unsur karbon(-CH2-CH2-CH2-)maka
lemak mempunyai sifat hydrophob. Ini menjadi alasan yang menjelaskan sulitnya lemak
untuk larut di dalam air. Lemak dapat larut hanya di larutan yang apolar atau organik
seperti: eter, Chloroform, atau benzol.
Fungsi
Secara umum dapat dikatakan bahwa lemak memenuhi fungsi dasar bagi manusia, yaitu:
[1]
1. Menjadi cadangan energi dalam bentuk sel lemak. 1 gram lemak menghasilkan
39.06 kjoule atau 9,3 kcal.
2. Lemak mempunyai fungsi selular dan komponen struktural pada membran sel
yang berkaitan dengan karbohidrat dan protein demi menjalankan aliran air, ion
dan molekul lain, keluar dan masuk ke dalam sel.
3. Menopang fungsi senyawa organik sebagai penghantar sinyal, seperti pada
prostaglandin dan steroid hormon dan kelenjar empedu.
4. Menjadi suspensi bagi vitamin A, D, E dan K yang berguna untuk proses biologis
5. Berfungsi sebagai penahan goncangan demi melindungi organ vital dan
melindungi tubuh dari suhu luar yang kurang bersahabat.
Lemak juga merupakan sarana sirkulasi energi di dalam tubuh dan komponen utama yang
membentuk membran semua jenis sel.
Sifat-Sifat Lemak
1.Sifat Fisis Lemak](https://image.slidesharecdn.com/makalahkimia-120618000941-phpapp01/85/Makalah-kimia-26-320.jpg)



![ikatan ester fosfat. Sementara gliserofosfolipid adalah komponen utama membran
biologis, komponen lipid non-gliserida lainnya seperti sfingomielin dan sterol (terutama
kolesterol di dalam membran sel hewani) juga ditemukan di dalam membran biologis.[2]
Di dalam tumbuhan dan alga, galaktosildiasilgliserol,[3] dan sulfokinovosildiasilgliserol,[4]
yang kekurangan gugus fosfat, adalah komponen penting dari membran kloroplas dan
organel yang berhubungan dan merupakan lipid yang paling melimpah di dalam jaringan
fotosintesis, termasuk tumbuhan tinggi, alga, dan bakteri tertentu.
Dwilapis telah ditemukan untuk memamerkan tingkat-tingkat tinggi dari keterbiasan
ganda yang dapat digunakan untuk memeriksa derajat keterurutan (atau kekacauan) di
dalam dwilapis menggunakan teknik seperti interferometri polarisasi ganda.
Organisasi-mandiri fosfolipid: liposom bulat, misel, dan dwilapis lipid.
Cadangan energi](https://image.slidesharecdn.com/makalahkimia-120618000941-phpapp01/85/Makalah-kimia-30-320.jpg)
![Triasilgliserol, tersimpan di dalam jaringan adiposa, adalah bentuk utama dari cadangan
energi di tubuh hewan. Adiposit, atau sel lemak, dirancang untuk sintesis dan pemecahan
sinambung dari triasilgliserol, dengan pemecahan terutama dikendalikan oleh aktivasi
enzim yang peka-hormon, lipase.[5] Oksidasi lengkap asam lemak memberikan materi
yang tinggi kalori, kira-kira 9 kkal/g, dibandingkan dengan 4 kkal/g untuk pemecahan
karbohidrat dan protein. Burung pehijrah yang harus terbang pada jarak jauh tanpa makan
menggunakan cadangan energi triasilgliserol untuk membahanbakari perjalanan
mereka.[6]
Pensinyalan
Di beberapa tahun terakhir, bukti telah mengemuka menunjukkan bahwa pensinyalan
lipid adalah bagian penting dari pensinyalan sel.[7] Pensinyalan lipid dapat muncul
melalui aktivasi reseptor protein G berpasangan atau reseptor nuklir, dan anggota-anggota
beberapa kategori lipid yang berbeda telah dikenali sebagai molekul-molekul pensinyalan
dan sistem kurir kedua.[8] Semua ini meliputi sfingosina-1-fosfat, sfingolipid yang
diturunkan dari seramida yaitu molekul kurir potensial yang terlibat di dalam pengaturan
pergerakan kalsium,[9] pertumbuhan sel, dan apoptosis;[10] diasilgliserol (DAG) dan
fosfatidilinositol fosfat (PIPs), yang terlibat di dalam aktivasi protein kinase C yang
dimediasi kalsium;[11] prostaglandin, yang merupakan satu jenis asam lemak yang
diturunkan dari eikosanoid yang terlibat di dalam radang and kekebalan;[12] hormon
steroid seperti estrogen, testosteron, dan kortisol, yang memodulasi fungsi reproduksi,
metabolisme, dan tekanan darah; dan oksisterol seperti 25-hidroksi-kolesterol yakni
agonis reseptor X hati.[13]
Fungsi lainnya
Vitamin-vitamin yang "larut di dalam lemak" (A, D, E, dan K1) – yang merupakan lipid
berbasis isoprena – gizi esensial yang tersimpan di dalam jaringan lemak dan hati, dengan
rentang fungsi yang berbeda-beda. Asil-karnitina terlibat di dalam pengangkutan dan
metabolisme asam lemak di dalam dan di luar mitokondria, di mana mereka mengalami
oksidasi beta.[14] Poliprenol dan turunan terfosforilasi juga memainkan peran
pengangkutan yang penting, di dalam kasus ini pengangkutan oligosakarida melalui
membran. Fungsi gula fosfat poliprenol dan gula difosfat poliprenol di dalam reaksi](https://image.slidesharecdn.com/makalahkimia-120618000941-phpapp01/85/Makalah-kimia-31-320.jpg)
![glikosilasi ekstra-sitoplasmik, di dalam biosintesis polisakarida ekstraselular (misalnya,
polimerisasi peptidoglikan di dalam bakteri), dan di dalam protein eukariotik N-
glikosilasi.[15][16] Kardiolipin adalah sub-kelas gliserofosfolipid yang mengandung empat
rantai asil dan tiga gugus gliserol yang tersedia melimpah khususnya pada membran
mitokondria bagian dalam.[17] Mereka diyakini mengaktivasi enzim-enzim yang terlibat
dengan fosforilasi oksidatif.[18]
Metabolisme
Lemak yang menjadi makanan bagi manusia dan hewan lain adalah trigliserida, sterol,
dan fosfolipid membran yang ada pada hewan dan tumbuhan. Proses metabolisme lipid
menyintesis dan mengurangi cadangan lipid dan menghasilkan karakteristik lipid
fungsional dan struktural pada jaringan individu.
Biosintesis
Karena irama laju asupan karbohidrat yang cukup tinggi bagi makhluk hidup, maka
asupan tersebut harus segera diolah oleh tubuh, menjadi energi maupun disimpan sebagai
glikogen. Asupan yang baik terjadi pada saat energi yang terkandung dalam karbohidrat
setara dengan energi yang diperlukan oleh tubuh, dan sangat sulit untuk menggapai
keseimbangan ini. Ketika asupan karbohidrat menjadi berlebih, maka kelebihan itu akan
diubah menjadi lemak. Metabolisme yang terjadi dimulai dari:
Asupan karbohidrat, antara lain berupa sakarida, fruktosa, galaktosa pada saluran
pencernaan diserap masuk ke dalam sirkulasi darah menjadi glukosa/gula darah.
Konsentrasi glukosa pada plasma darah diatur oleh tiga hormon, yaitu glukagon,
insulin dan adrenalin.
Insulin akan menaikkan laju sirkulasi glukosa ke seluruh jaringan tubuh. Pada
jaringan adiposa, adiposit akan mengubah glukosa menjadi glukosa 6-fosfat dan
gliserol fosfat, masing-masing dengan bantuan satu molekul ATP.
o Jaringan adiposit ini yang sering dikonsumsi kita sebagai lemak.
Glukosa 6-fosfat kemudian dikonversi oleh hati dan jaringan otot menjadi
glikogen. Proses ini dikenal sebagai glikogenesis, dalam kewenangan insulin.](https://image.slidesharecdn.com/makalahkimia-120618000941-phpapp01/85/Makalah-kimia-32-320.jpg)

![o Proses ini terjadi di dalam hati dan disebut lipolisis. Sejumlah hormon
yang antagonis dengan insulin disekresi pada proses ini menuju ke dalam
hati, antara lain:
Glukagon, sekresi dari kelenjar pankreas
ACTH, GH, sekresi dari kelenjar hipofisis
Adrenalin, sekresi dari kelenjar adrenal
TH, sekresi dari kelenjar tiroid
o Lemak di dalam darah yang berlebih akan disimpan di dalam jaringan
adiposa.
Lebih lanjut gliserol dikonversi menjadi dihidroksiaketon, kemudian menjadi
dihidroksiaketon fosfat dan masuk ke dalam proses glikolisis.
Sedangkan asam lemak akan dikonversi di dalam mitokondria dengan proses
oksidasi, dengan bantuan asetil-KoA menjadi adenosin trifosfat, karbondioksida
dan air.
Kejadian ini melibatkan sintesis asam lemak dari asetil-KoA dan esterifikasi asam lemak
pada saat pembuatan triasilgliserol, suatu proses yang disebut lipogenesis atau sintesis
asam lemak.[19] Asam lemak dibuat oleh sintasa asam lemak yang mempolimerisasi dan
kemudian mereduksi satuan-satuan asetil-KoA. Rantai asil pada asam lemak diperluas
oleh suatu daur reaksi yang menambahkan gugus asetil, mereduksinya menjadi alkohol,
mendehidrasinya menjadi gugus alkena dan kemudian mereduksinya kembali menjadi
gugus alkana. Enzim-enzim biosintesis asam lemak dibagi ke dalam dua gugus, di dalam
hewan dan fungi, semua reaksi sintasa asam lemak ini ditangani oleh protein tunggal
multifungsi,[20] sedangkan di dalam tumbuhan, plastid dan bakteri memisahkan kinerja
enzim tiap-tiap langkah di dalam lintasannya.[21][22] Asam lemak dapat diubah menjadi
triasilgliserol yang terbungkus di dalam lipoprotein dan disekresi dari hati.
Sintesis asam lemak tak jenuh melibatkan reaksi desaturasa, di mana ikatan ganda
diintroduksi ke dalam rantai asil lemak. Misalnya, pada manusia, desaturasi asam stearat
oleh stearoil-KoA desaturasa-1 menghasilkan asam oleat. Asam lemak tak jenuh ganda-
dua (asam linoleat) juga asam lemak tak jenuh ganda-tiga (asam linolenat) tidak dapat
disintesis di dalam jaringan mamalia, dan oleh karena itu asam lemak esensial dan harus
diperoleh dari makanan.[23]](https://image.slidesharecdn.com/makalahkimia-120618000941-phpapp01/85/Makalah-kimia-34-320.jpg)
![Sintesis triasilgliserol terjadi di dalam retikulum endoplasma oleh lintasan metabolisme di
mana gugus asil di dalam asil lemak-KoA dipindahkan ke gugus hidroksil dari gliserol-3-
fosfat dan diasilgliserol.[24]
Terpena dan terpenoid, termasuk karotenoid, dibuat oleh perakitan dan modifikasi satuan-
satuan isoprena yang disumbangkan dari prekursor reaktif isopentenil pirofosfat dan
dimetilalil pirofosfat.[25] Prekursor ini dapat dibuat dengan cara yang berbeda-beda. Pada
hewan dan archaea, lintasan mevalonat menghasilkan senyawa ini dari asetil-KoA,[26]
sedangkan pada tumbuhan dan bakteri lintasan non-mevalonat menggunakan piruvat dan
gliseraldehida 3-fosfat sebagai substratnya.[25][27] Satu reaksi penting yang menggunakan
donor isoprena aktif ini adalah biosintesis steroid. Di sini, satuan-satuan isoprena
digabungkan untuk membuat skualena dan kemudian dilipat dan dibentuk menjadi
sehimpunan cincin untuk membuat lanosterol.[28] Lanosterol kemudian dapat diubah
menjadi steroid, seperti kolesterol dan ergosterol.[28][29]
Degradasi
Oksidasi beta adalah proses metabolisme di mana asam lemak dipecah di dalam
mitokondria dan/atau di dalam peroksisoma untuk menghasilkan asetil-KoA. Sebagian
besar, asam lemak dioksidasi oleh suatu mekanisme yang sama, tetapi tidak serupa
dengan, kebalikan proses sintesis asam lemak. Yaitu, pecahan berkarbon dua dihilangkan
berturut-turut dari ujung karboksil dari asam itu setelah langkah-langkah dehidrogenasi,
hidrasi, dan oksidasi untuk membentuk asam keto-beta, yang dipecah dengan tiolisis.
Asetil-KoA kemudian diubah menjadi Adenosina trifosfat, CO2, dan H2O menggunakan
daur asam sitrat dan rantai pengangkutan elektron. Energi yang diperoleh dari oksidasi
sempurna asam lemak palmitat adalah 106 ATP.[30] Asam lemak rantai-ganjil dan tak
jenuh memerlukan langkah enzimatik tambahan untuk degradasi.
Gizi dan kesehatan
Sebagian besar lipid yang ditemukan di dalam makanan adalah berbentuk triasilgliserol,
kolesterol dan fosfolipid. Kadar rendah lemak makanan adalah penting untuk
memfasilitasi penyerapan vitamin-vitamin yang larut di dalam lemak (A, D, E, dan K)
dan karotenoid.[31] Manusia dan mamalia lainnya memerlukan makanan untuk memenuhi](https://image.slidesharecdn.com/makalahkimia-120618000941-phpapp01/85/Makalah-kimia-35-320.jpg)
![kebutuhan asam lemak esensial tertentu, misalnya asam linoleat (asam lemak omega-6)
dan asam alfa-linolenat (sejenis asam lemak omega-3) karena mereka tidak dapat
disintesis dari prekursor sederhana di dalam makanan.[32] Kedua-dua asam lemak ini
memiliki 18 karbon per molekulnya, lemak majemuk tak jenuh berbeda di dalam jumlah
dan kedudukan ikatan gandanya. Sebagian besar minyak nabati adalah kaya akan asam
linoleat (safflower, bunga matahari, dan jagung). Asam alfa-linolenat ditemukan di dalam
daun hijau tumbuhan, dan di beberapa biji-bijian, kacang-kacangan, dan leguma
(khususnya flax, brassica napus, walnut, dan kedelai).[33] Minyak ikan kaya akan asam
lemak omega-3 berantai panjang asam eikosapentaenoat dan asam dokosaheksaenoat.[34]
Banyak pengkajian telah menunjukkan manfaat kesehatan yang baik yang berhubungan
dengan asupan asam lemak omega-3 pada perkembangan bayi, kanker, penyakit
kardiovaskular (gangguan jantung), dan berbagai penyakit kejiwaan, seperti depresi,
kelainan hiperaktif/kurang memperhatikan, dan demensia.[35][36] Sebaliknya, kini
dinyatakan bahwa asupan lemak trans, yaitu yang ada pada minyak nabati yang
dihidrogenasi sebagian, adalah faktor risiko bagi penyakit jantung.[37][38][39]
Beberapa pengkajian menunjukkan bahwa total asupan lemak yang dikonsumsi
berhubungan dengan menaiknya risiko kegemukan[40][41] and diabetes.[42][43] Tetapi,
pengkajian lain yang cukup banyak, termasuk Women's Health Initiative Dietary
Modification Trial (Percobaan Modifikasi Makanan Inisiatif Kesehatan Perempuan),
sebuah pengkajian selama delapan tahun terhadap 49.000 perempuan, Nurses' Health
Study (Pengkajian Kesehatan Perawat dan Health Professionals Follow-up Study
(Pengkajian Tindak-lanjut Profesional Kesehatan), mengungkapkan ketiadaan hubungan
itu.[44][45][46] Kedua-dua pengkajian ini tidak menunjukkan adanya hubungan antara
persentase kalori dari lemak dan risiko kanker, penyakit jantung, atau kelebihan bobot
badan. Nutrition Source, sebuah situs web yang dipelihara oleh Departemen Gizi di
Sekolah Kesehatan Masyarakat Harvard, mengikhtisarkan bukti-bukti terkini pada
dampak lemak makanan: "Sebagian besar rincian penelitian yang dilakukan di Harvard
ini menunjukkan bahwa jumlah keseluruhan lemak di dalam makanan tidak berhubungan
dengan bobot badan atau penyakit tertentu."[47]](https://image.slidesharecdn.com/makalahkimia-120618000941-phpapp01/85/Makalah-kimia-36-320.jpg)

