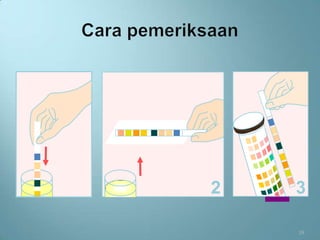
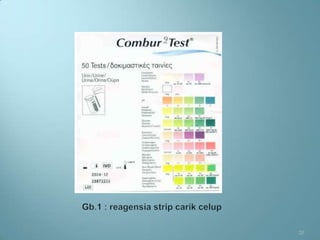
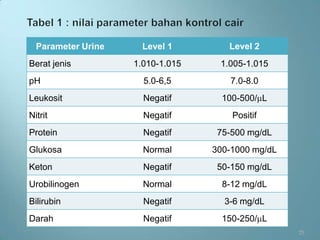
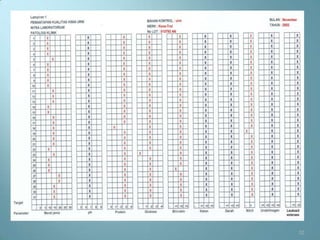
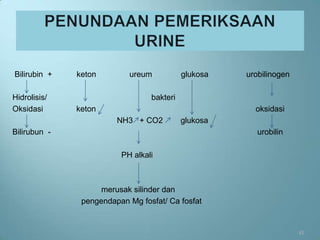
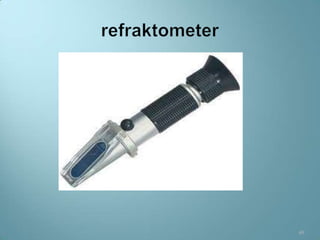
Dokumen ini menjelaskan prosedur dan prinsip pemeriksaan laboratorium urine, termasuk jenis pemeriksaan, alat, reagensia, serta teknik penyimpanan dan analisis yang benar. Beberapa pemeriksaan yang dibahas mencakup pemeriksaan makroskopis, kimia, dan mikroskopis serta faktor yang dapat mempengaruhi hasil seperti kontaminasi dan penyimpanan yang tidak tepat. Selain itu, pemantapan mutu laboratorium dijelaskan untuk memastikan akurasi hasil pemeriksaan.