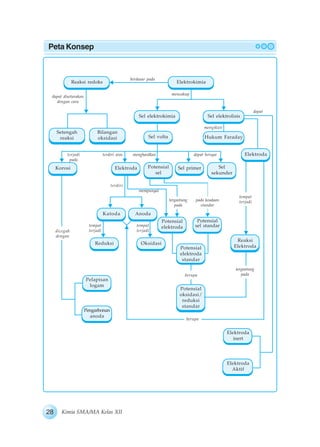
Reaksi redoks dan elektrokimia merupakan bab yang membahas reaksi redoks, sel volta, dan sel elektrolisis. Reaksi redoks adalah reaksi yang melibatkan perubahan bilangan oksidasi dan terdiri atas reaksi reduksi dan oksidasi. Sel elektrokimia terdiri atas sel volta yang menghasilkan arus listrik dari reaksi redoks dan sel elektrolisis yang menggunakan arus listrik untuk menghasilkan reaksi redoks. Sel volta dan sel