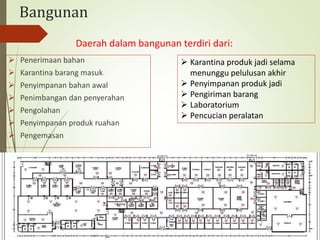
Dokumen tersebut membahas pedoman cara pembuatan kosmetik yang baik (CPKB) yang mencakup 12 aspek utama mulai dari sistem manajemen mutu, personalia, fasilitas produksi, peralatan, sanitasi, produksi, pengawasan mutu, dokumentasi, audit internal, penyimpanan, kontrak produksi dan pengujian, serta penanganan keluhan produk. Penerapan CPKB merupakan persyaratan untuk memperoleh sertifikat pembuatan kosmetik yang baik."