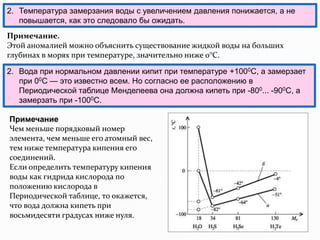
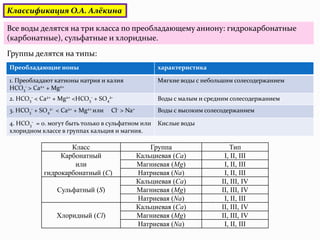
Лекция доцента Петровой Е.А. охватывает структуру и свойства воды, ее аномальные физико-химические характеристики и гидрологический цикл. Также рассматриваются классификации природных вод по происхождению, минерализации и химическому составу. Документ подчеркивает важность воды как универсального растворителя и регулятора температуры на планете.