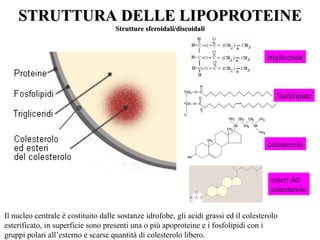
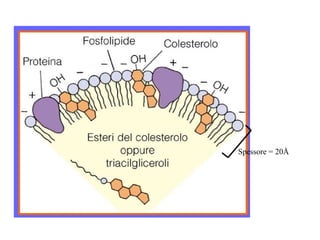
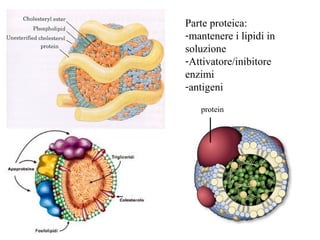
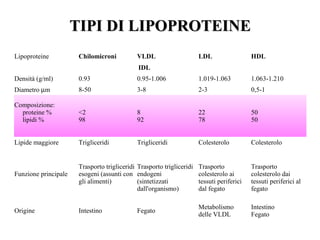
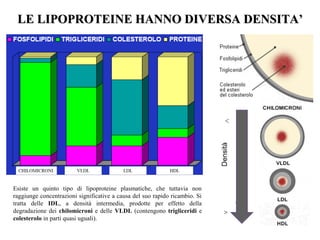
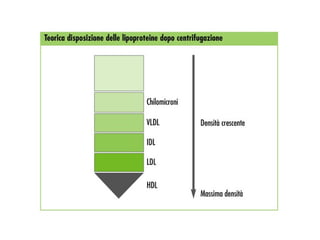
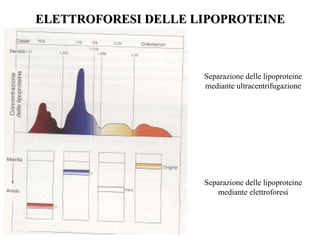
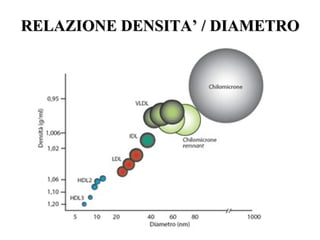
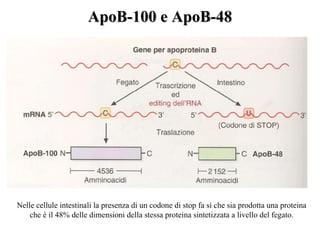
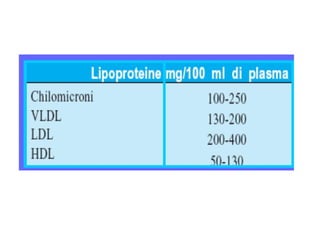
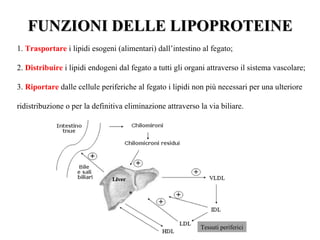
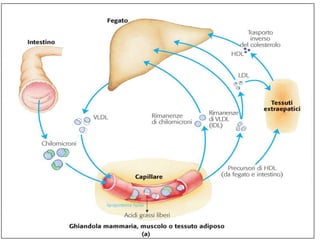
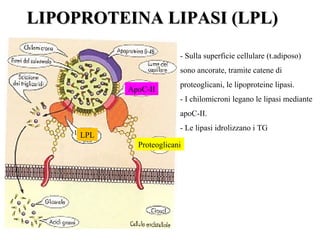
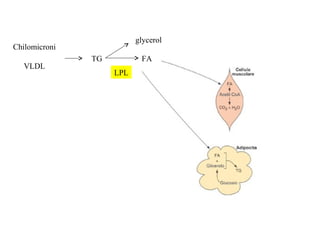
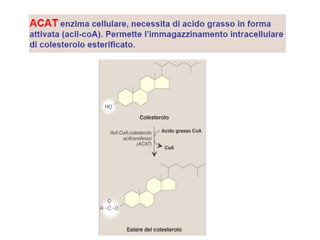
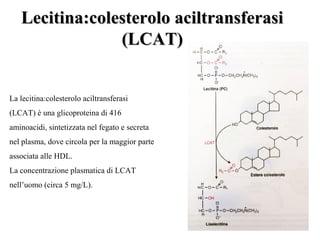
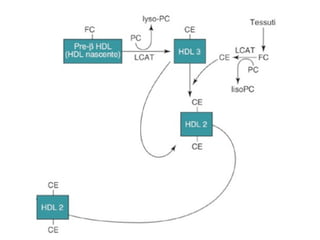
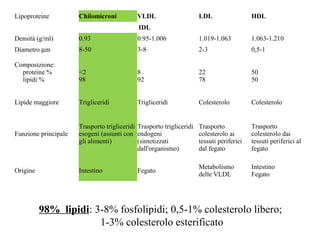
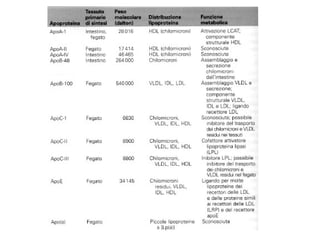
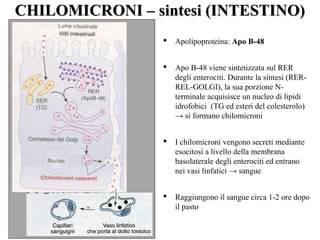
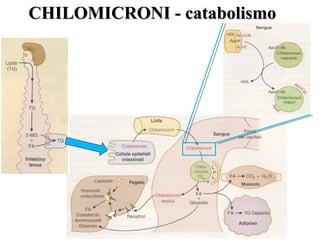
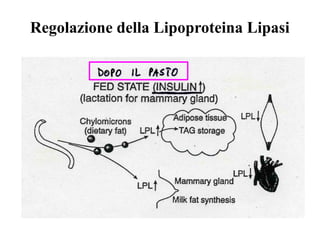
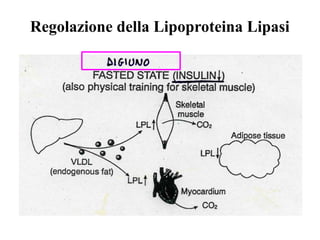
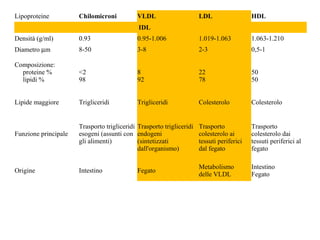
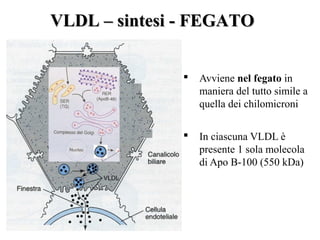
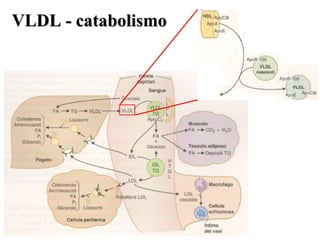
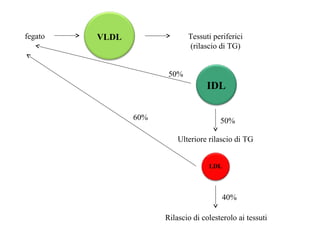
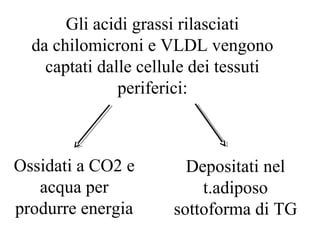
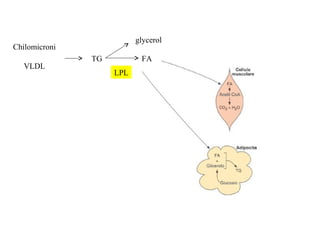
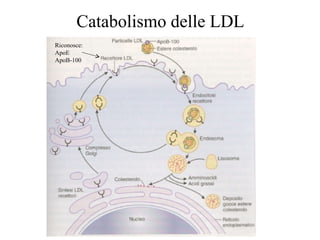
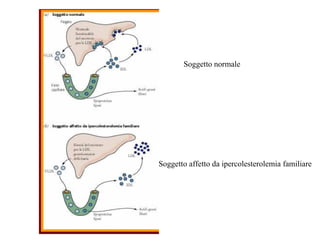
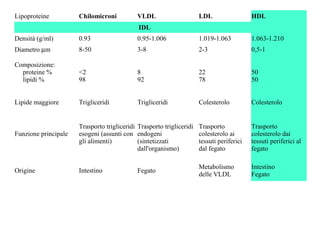
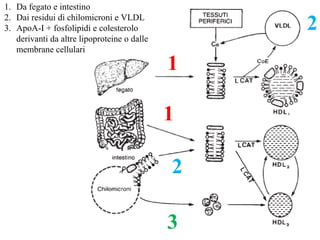
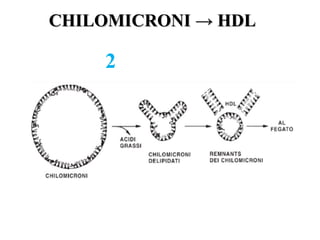
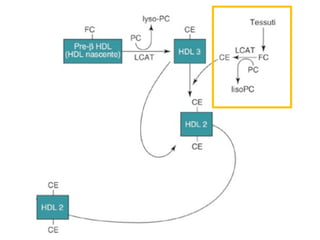
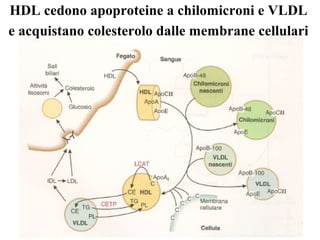
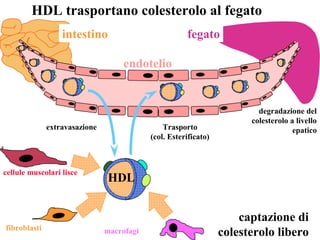
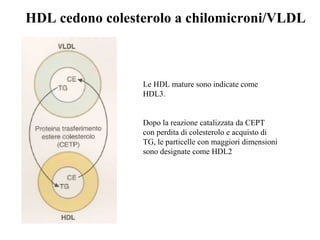
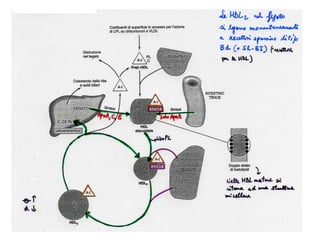
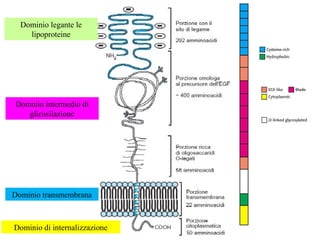
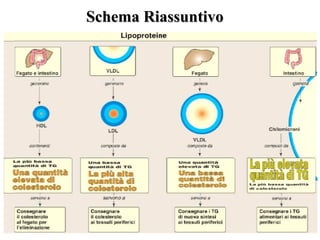
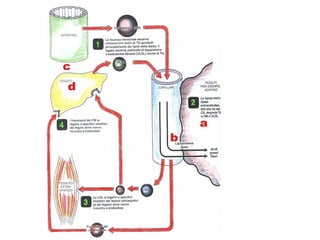
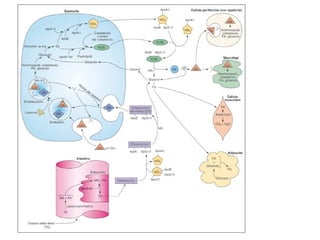
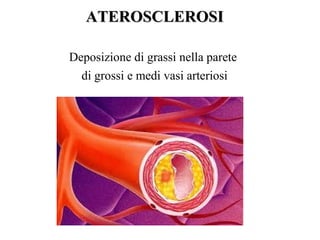
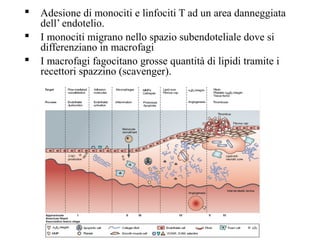
Le lipoproteine sono macromolecole che trasportano lipidi nel corpo, include classi come chilomicroni, VLDL, LDL e HDL. Esse svolgono funzioni cruciali come il trasporto di lipidi esogeni ed endogeni e il riassorbimento del colesterolo dai tessuti. La loro struttura e composizione varia, influenzando anche il metabolismo e le condizioni patologiche come l'ipercolesterolemia familiare.