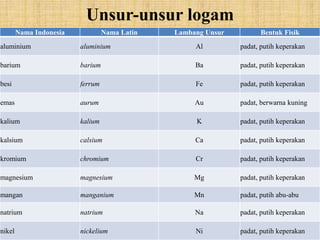
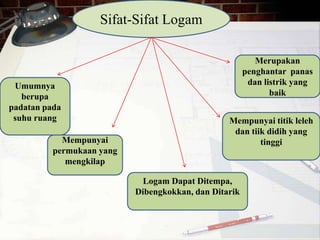
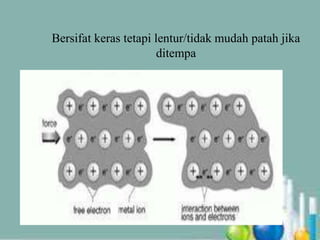
Dokumen tersebut membahas tentang ikatan logam dan sifat-sifat logam. Ikatan logam terbentuk antara atom logam akibat gaya tarik antara muatan positif ion logam dengan elektron bebas. Sifat logam meliputi berupa padatan pada suhu ruang, menghantarkan panas dan listrik, titik leleh dan didih tinggi, serta permukaan yang mengkilap.