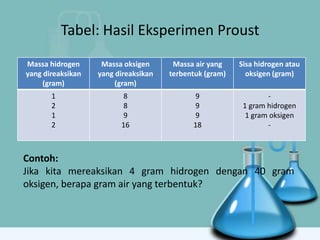
Hukum Proust menyatakan bahwa perbandingan massa unsur-unsur penyusun suatu senyawa adalah tetap dan tidak bergantung pada jumlah atau asal bahan awal. Eksperimen Proust menunjukkan bahwa perbandingan massa hidrogen dan oksigen yang membentuk air adalah 1:8.