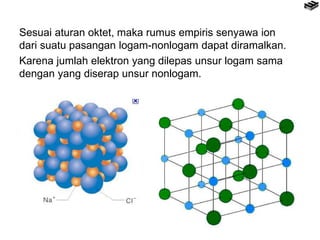
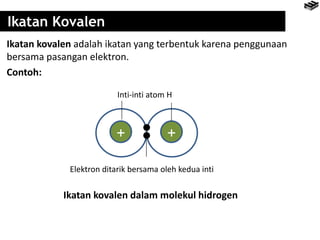
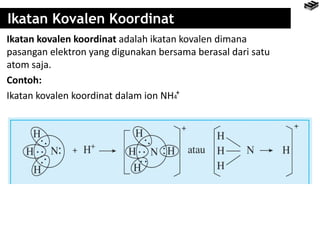
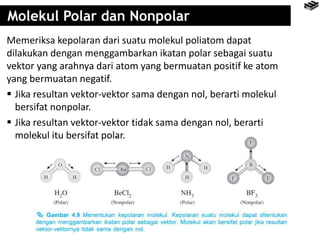
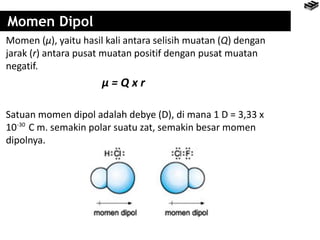
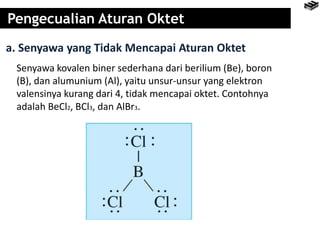
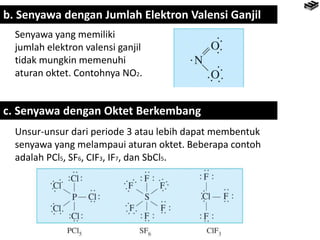
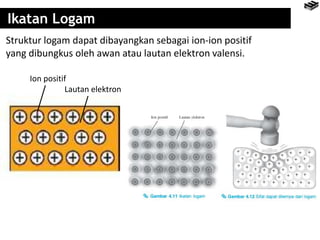
Bab 4 membahas berbagai jenis ikatan kimia seperti ikatan ion, kovalen, logam, serta pengecualian aturan oktet. Ikatan ion terbentuk melalui pertukaran elektron antara unsur logam dan nonlogam, sedangkan ikatan kovalen terbentuk dari berbagi elektron. Aturan oktet menjelaskan kecenderungan unsur untuk memiliki konfigurasi elektron seperti gas mulia terdekat.