Πολυατομικά Ιόντα και αριθμός οξείδωσης
•Download as PPT, PDF•
0 likes•1,623 views
Χημεία Α΄Λυκείου
Report
Share
Report
Share
Recommended
More Related Content
What's hot
What's hot (20)
χημεια α Ppt05 (3.3 3.5 3.6 χημικές αντιδράσεις) (1)

χημεια α Ppt05 (3.3 3.5 3.6 χημικές αντιδράσεις) (1)
Χημεία Α' Λυκείου - Βασικές έννοιες (Inter learning)

Χημεία Α' Λυκείου - Βασικές έννοιες (Inter learning)
More from Fotis Fotiades
More from Fotis Fotiades (20)
Ταξινόμηση των μορφών άνθρακα (φυσικοί & τεχνητοί)

Ταξινόμηση των μορφών άνθρακα (φυσικοί & τεχνητοί)
Εύρεση μοριακού τύπου από τον αριθμό οξείδωσης - Αντιδράσεις Εξουδετέρωσης

Εύρεση μοριακού τύπου από τον αριθμό οξείδωσης - Αντιδράσεις Εξουδετέρωσης
Recently uploaded
Recently uploaded (13)
Γιορτή της μητέρας-Φύλλα εργασιών για όλες τις τάξεις

Γιορτή της μητέρας-Φύλλα εργασιών για όλες τις τάξεις
RODOPI CHALLENGE (ROC 50 MILES) 2024 ΤΕΧΝΙΚΗ ΕΝΗΜΕΡΩΣH

RODOPI CHALLENGE (ROC 50 MILES) 2024 ΤΕΧΝΙΚΗ ΕΝΗΜΕΡΩΣH
Οδηγίες για τη δημιουργία Flashcard με το Quizlet.pdf

Οδηγίες για τη δημιουργία Flashcard με το Quizlet.pdf
EKSETASTEA KAI DIDAKTEA YLH G TAKSHS GENIKOY LYKEIOY

EKSETASTEA KAI DIDAKTEA YLH G TAKSHS GENIKOY LYKEIOY
Οδηγίες για τη δημιουργία διαδραστικών δραστηριοτήτων με την εφαρμογή Wordwal...

Οδηγίες για τη δημιουργία διαδραστικών δραστηριοτήτων με την εφαρμογή Wordwal...
2η Διεθνική Συνάντηση μαθητών και καθηγητών στο Σαλέρνο της Ιταλίας

2η Διεθνική Συνάντηση μαθητών και καθηγητών στο Σαλέρνο της Ιταλίας
ΠΑΝΕΛΛΗΝΙΕΣ 2024 ΠΡΟΤΕΙΝΟΜΕΝΑ ΘΕΜΑΤΑ ΝΕΟΕΛΛΗΝΙΚΗ ΓΛΩΣΣΑ ΚΑΙ ΛΟΓΟΤΕΧΝΙΑ.pdf

ΠΑΝΕΛΛΗΝΙΕΣ 2024 ΠΡΟΤΕΙΝΟΜΕΝΑ ΘΕΜΑΤΑ ΝΕΟΕΛΛΗΝΙΚΗ ΓΛΩΣΣΑ ΚΑΙ ΛΟΓΟΤΕΧΝΙΑ.pdf
Η Δυναστεία των Παλαιολόγων - Βυζαντινή Αυτοκρατορία

Η Δυναστεία των Παλαιολόγων - Βυζαντινή Αυτοκρατορία
Πολυατομικά Ιόντα και αριθμός οξείδωσης
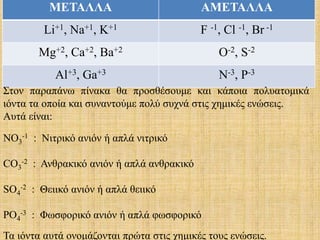
- 1. ΜΕΤΑΛΛΑ ΑΜΕΤΑΛΛΑ Li+1, Na+1, K+1 F -1, Cl -1, Br -1 Mg+2, Ca+2, Ba+2 Ο-2, S-2 Al+3, Ga+3 Ν-3, P-3 Στον παραπάνω πίνακα θα προσθέσουμε και κάποια πολυατομικά ιόντα τα οποία και συναντούμε πολύ συχνά στις χημικές ενώσεις. Αυτά είναι: ΝΟ3 -1 : Νιτρικό ανιόν ή απλά νιτρικό CΟ3 -2 : Ανθρακικό ανιόν ή απλά ανθρακικό SO4 -2 : Θειικό ανιόν ή απλά θειικό PO4 -3 : Φωσφορικό ανιόν ή απλά φωσφορικό Τα ιόντα αυτά ονομάζονται πρώτα στις χημικές τους ενώσεις.
- 2. Π.χ. ας ενώσουμε το Na+1 με καθένα από αυτά Na+1 ΝΟ3 -1 Na+1 CΟ3 -2 Na+1 SO4 -2 Na+1 PO4 -3 NaΝΟ3 Na2 CΟ3 Na2SO4 Na3PO4 Νιτρικό νάτριο Ανθρακικό νάτριο Θειικό νάτριο Φωσφορικό νάτριο
- 3. Π.χ. ας ενώσουμε το Ca+2 με καθένα από αυτά Ca+2 ΝΟ3 -1 Ca+2 CΟ3 -2 Ca+2 SO4 -2 Ca+2 PO4 -3 Ca(ΝΟ3)2 Ca2 (CΟ3)2 Ca2(SO4)2 Ca3(PO4)2 Νιτρικό ασβέστιο Ανθρακικό ασβέστιο Θειικό ασβέστιο Φωσφορικό ασβέστιο CaCΟ3 CaSO4
- 4. Π.χ. ας ενώσουμε το Al+3 με καθένα από αυτά Al+3 ΝΟ3 -1 Al+3 CΟ3 -2 Al+3 SO4 -2 Al+3 PO4 -3 Al(ΝΟ3)3 Al2 (CΟ3)3 Al2(SO4)3 Al3(PO4)3 Νιτρικό αργίλιο Ανθρακικό αργίλιο Θειικό αργίλιο Φωσφορικό αργίλιο AlPO4
- 5. Ως γνωστό, οι ετεροπολικές ενώσεις είναι στερεές στις συνθήκες που είμαστε π.χ. το κοινό αλάτι NaCl. Όταν πρόκειται να πραγματοποιήσουμε αντιδράσεις μεταξύ αλάτων στο εργαστήριο, πρώτα τα άλατα τα διαλύουμε στο νερό και έπειτα τα αναμιγνύουμε. Φτιάχνουμε δηλαδή ένα υδατικό διάλυμα άλατος και το συμβολίζουμε με (aq) Δηλ. NaCl(aq) σημαίνει υδατικό διάλυμα χλωριούχου νατρίου ενώ NaCl(s) σημαίνει στερεό χλωριούχο νάτριο
- 6. Ας προσπαθήσουμε να συμπληρώσουμε μια τέτοια αντίδραση που πραγματοποιείται: LiF Li2S AgF Ag2S + + → Li+1 S-2 Ag+1 F -1 Όμως κάτι δεν πάει καλά… Μπορούμε να το διορθώσουμε; 2 2 Σχηματίζεται αέριο ή ίζημα; Ναι ! ↓
- 7. Και κάνα δύσκολο για εσάς: Na2CO3 + BaCl2 → ΠΡΟΣΟΧΗ!!! Το CΟ3 είναι ένα πολυατομικό ιόν και το 3 δεν είναι ο Α.Ο. του νατρίου BaCO3 + NaCl 2 Na+1 CΟ3 -2 Ba+2 Cl -1 ↓
