1. นางสาวนิติมา รุจิเรขาสุวรรณ
วิชา เคมี สอวน. ชั้นมัธยมศึกษาปีที่ 1
โรงเรียนเฉลิมพระเกียรติสมเด็จพระศรีนครินทร์ กาญจนบุรี
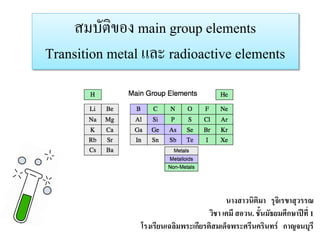
สมบัติของ main group elements
Transition metal และ radioactive elements 2. ปฏิกิริยาของธาตุหมู่ IA
ธาตุหมู่ IA (หมู่แอลคาไลน์)
ธาตุหมู่ IA ได้แก่ ธาตุลิเทียม(Li) โซเดียม(Na) โพแทสเซียม(K) รูบิเดียม(Rb)
ซีเซียม(Cs) และ แฟรนเซียม(Fr)
สมบัติทั่วไปของธาตุหมู่ IA
1. เป็นธาตุที่มีเวเลนซ์อิเล็กตรอนเท่ากับ 1 ธาตุหมู่นี้มีความเป็นโลหะมากที่สุด
2. เป็นธาตุที่มีความว่องไวทางเคมีสูงมาก เช่น ทาปฏิกิริยากับ O2 ในอากาศได้เร็ว,
ทาปฏิกิริยากับน้ารุนแรงมาก ดังนั้นโลหะหมู่ IA ต้องเก็บไว้ในน้ามัน
3. มีสถานะเป็นของแข็ง เป็นโลหะอ่อน
3. 4. ปฏิกิริยาของธาตุหมู่ IA
4.1 ทาปฏิกิริยากับออกซิเจน( O2) ได้สารประกอบออกไซด์
4.2 ทาปฏิกิริยากับน้า (H2O) รุนแรง ได้สารละลายเบสและแก๊สไฮโดรเจน
ธาตุหมู่ IA (หมู่แอลคาไลน์)
เช่น 2Li(s) + O2(g) Li2O(s)
เช่น 2Na(s) + 2H2O(l) 2Na+ (aq) + 2OH- (aq) + H2(g)
ปฏิกิริยาของธาตุหมู่ IA 4. ปฏิกิริยาของธาตุหมู่ IIA
ธาตุหมู่ IIA (หมู่แอลคาไลน์เอิร์ท)
ธาตุหมู่ IIA ได้แก่ ธาตุเบริลเลียม(Be) แมกนีเซียม(Mg) แคลเซียม(Ca) สทรอนเซียม(Sr)
แบเรียม(Ba) และ เรเดียม(Ra)
สมบัติทั่วไปของธาตุหมู่ IIA
1. เป็นธาตุที่มีเวเลนซ์อิเล็กตรอนเท่ากับ 2 ทุกธาตุเป็นโลหะ
2. ทุกธาตุมีสถานะเป็นของแข็งมีความหนาแน่นมากกว่าน้า
3. มีจุดเดือดจุดหลอมเหลวสูงกว่าธาตุหมู่ IA ในคาบเดียวกัน เพราะธาตุหมู่ IIA
มีความแรงของพันธะโลหะมากกว่า
5. 4. ปฏิกิริยาของธาตุหมู่ IIA
4.1 ทาปฏิกิริยากับออกซิเจน( O2) ได้สารประกอบออกไซด์
4.2 ทาปฏิกิริยากับน้า (H2O) ยกเว้น Be แต่ช้ากว่าหมู่ IA ได้สารละลายเบส
และแก๊สไฮโดรเจน
เช่น Mg(s) + O2(g) 2MgO(s)
เช่น Mg(s) + 2H2O(l) Mg2+ (aq) + 2OH- (aq) + H2(g)
ธาตุหมู่ IIA (หมู่แอลคาไลน์เอิร์ท)
ปฏิกิริยาของธาตุหมู่ IIA 6. ธาตุหมู่ VIIA ได้แก่ ธาตุฟลูออรีน(F) คลอรีน(Cl) โบรมีน(Br) ไอโอดีน(I)
และ แอสทาทีน(At)
สมบัติทั่วไปของธาตุหมู่ VIIA
1. เป็นธาตุที่มีเวเลนซ์อิเล็กตรอนเท่ากับ 7 มีความเป็นอโลหะมาก
2. ทุกธาตุ 1 โมเลกุล มี 2 อะตอม เรียกว่า Diatomic molecule เช่น F2, Cl2, I2
3. มีทุกสถานะ ได้แก่ F2, Cl2 เป็นแก๊ส, Br2 เป็นของเหลว, I2 เป็นของแข็ง
ปฏิกิริยาของธาตุหมู่ VIIA
ธาตุหมู่ VIIA (หมู่แฮโลเจน) 7. 4. มีสีต่างๆ เช่น F2 สีเหลืองอ่อน , Cl2 สีตองอ่อน,
Br2 สีน้าตาลแดง
5. ทุกธาตุไม่นาไฟฟ้าเพราะเป็นธาตุอโลหะ
ปฏิกิริยาของธาตุหมู่ VIIA
ธาตุหมู่ VIIA (หมู่แฮโลเจน) 10. ธาตุแทรนซิชัน
เป็นโลหะซึ่งส่วนใหญ่มีจุดหลอมเหลว จุดเดือดสูง
สมบัติของธาตุแทรนซิชัน (properties of transition elements)
รัศมีอะตอมมีขนาดใกล้เคียงกัน
เป็นตัวนาไฟฟ้าและนาความร้อนที่ดี เช่น Fe, Cu, Ag
สารประกอบส่วนมากของธาตุแทรนซิชันมีสี
สารประกอบ เชิงซ้อน
ไอออนบวก
ไอออนลบ
สีของ สารประกอบ
KMnO4
K+
[MnO4]-
ม่วงแดง
K2MnO4
K+
[MnO4]2-
เขียว
PbCrO4
Pb2+
[CrO4]2+
เหลือง
K3[Fe(CN)6]
K+
[Fe(CN)6]3-
ส้มแดง
Cu[(NH3)4SO4}]
[Cu(NH3)4]2+
[SO4]2-
คราม
Cu[(H2O)5SO4]
[Cu(H2O)5]2+
[SO4]2-
น้าเงิน 11. ธาตุกัมมันตรังสี (radioactive element)
อองตวน อองรี เบ็กเคอเรล พบว่าแผ่นฟิล์มถ่ายรูปที่ห่อหุ้มด้วยกระดาษดา
ที่เก็บรวมไว้กับสารประกอบยูเรเนียมมีลักษณะเหมือนแสงสว่าง จึงทาการ
ทดลองและสรุปว่า ธาตุยูเรเนียมมีสมบัติในการแผ่รังสีออกมาได้
Antoine henri becquerel discoverd the
phenomenon of radioactivity by exposing
a photographic plate to uranium 1896.
โลหะยูเรเนียมธรรมชาติ ประกอบด้วย
U-235 ประมาณ 0.71%,
U-238 ประมาณ 99.28%
U-234 ประมาณ 0.0054% 12. ปิแอร์ คูรี และมารี คูรี พบเพิ่มเติมว่า ยังมีธาตุอื่นที่
สามารถแผ่รังสีได้เช่นเดียวกัน เช่น ธาตุพอลโลเนียม (Po),
เรเดียม (Ra) และทอเรียม(Th)
ธาตุกัมมันตรังสี (radioactive element) 13. ธาตุกัมมันตรังสี
คือธาตุที่แผ่รังสีได้ ส่วนใหญ่มีเลขอะตอมสูงกว่า 83 เช่น ยูเรเนียม( )
ทอเรียม ( ) เรเดียม ( )
กัมมันตภาพรังสี คือ ปรากฏการณ์ที่ธาตุแผ่รังสีได้เองอย่างต่อเนื่อง
เกิดจากนิวเคลียสของไอโซโทปที่ไม่เสถียร แผ่รังสีออกมาเพื่อปลดปล่อย
พลังงานส่วนเกินที่อยู่ภายในออกไป จนกว่าจะได้นิวเคลียสที่เสถียรจึงจะ
หยุดแผ่รังสี
ธาตุกัมมันตรังสี 20. 2. ผลต่อร่างกาย ( Somatic Effect)
ทาให้โมเลกุลแตกตัว สารต่างๆในร่างกายเสียสมดุล เซลล์ตาย
ทาให้เกิดความเจ็บป่วย หากได้รับปริมาณมากอาจเสียชีวิต
ธาตุกัมมันตรังสี
อันตรายของกัมมันตรังสี 22. ค่าครึ่งชีวิต (Half life) สัญลักษณ์ ( )
หมายถึง ระยะเวลาที่ปริมาณสารกัมมันตรังสีสลายตัวจนเหลือ
ครึ่งหนึ่งของปริมาณเริ่มต้น
ตัวอย่าง 1 S-35 มีครึ่งชีวิต 80 วัน ถ้ามี S-35 อยู่ 8 กรัม เมื่อเวลาผ่านไป
240 วัน จะเหลือกี่กรัม
ธาตุกัมมันตรังสี
ตัวอย่างเช่น C-14 มีครึ่งชีวิต 5730 ปี หมายความว่า ถ้ามี C-14 จานวน 1 กรัม
เมื่อเวลาผ่านไป 5730 ปี จะเหลือ C-14 อยู่ 0.5 กรัม และเมื่อเวลาผ่านไปอีก
5730 ปี จะเหลืออยู่ 0.25 กรัม เป็นดังนี้ไปเรื่อยๆ
5730 ปี 5730 ปี
C-14 จานวน 1 กรัม 0.5 กรัม 0.25 กรัม 23. ตัวอย่าง 2 Co มีครึ่งชีวิต 10 วัน เมื่อเวลาผ่านไป 30 วัน เหลือ 5 g
เริ่มต้นมี Co กี่กรัม
ตัวอย่าง 3 กัมมันตรังสีชนิดหนึ่ง เริ่มต้นมี 20 กรัม เมื่อผ่านไป 2 ชม.
เหลือ 1.25 g ค่าครึ่งชีวิตของกัมมันตรังสีนี้มีค่าเท่าใด
ธาตุกัมมันตรังสี 24. ธาตุกัมมันตรังสี
การบ้าน
1. ไอโอดีน-131 มีครึ่งชีวิต 8 วัน จานวน 10 g เมื่อเวลาผ่านไปกี่วันจึงจะมี
ไอโอดีน-131 เหลือ 2.5 g
2. ไอโซโทปกัมมันตรังสีชนิดหนึ่งจานวน 20 g เมื่อเวลาผ่านไป 2 ชั่วโมง
ไอโซโทปนั้นเหลืออยู่ 1.25 g ครึ่งชีวิตของไอโซโทปนี้มีค่าเท่าใด
3. เมื่อเวลาผ่านไป 120 วัน จะมีซีเซียม-137 เหลืออยู่ 300 g
ถ้าครึ่งชีวิตของซีเซียม-137 เท่ากับ 30 วัน จงหาว่าเมื่อเริ่มต้นมีซีเซียม
อยู่เท่าใด