Статья описывает необходимость улучшения лечения острых респираторных инфекций (ОРИ) у детей, так как текущие методы неэффективны и приводят к осложнениям. Исследование показало, что применение инозина пранобекс способствует улучшению клинической симптоматики и укреплению иммунного статуса у детей с ОРИ, что делает его рекомендуемым средством для лечения. Работа подтверждает высокую эффективность и безопасность инозина пранобекс, необходимого для расширения схем терапии ОРИ у детей старше трех лет.
![Оригинальная статья
Э.Н. Симованьян, Э.Е. Бадальянц, Л.П. Сизякина, А.А. Лебеденко, В.Б. Денисенко, М.А. Ким
Ростовский государственный медицинский университет Минздрава России, Ростов-на-Дону
Совершенствование программы
лечения острых респираторных
инфекций у детей
Контактная информация:
Симованьян Эмма Никитична, доктор медицинских наук, профессор, заведующая кафедрой детских инфекционных болезней ГБОУ ВПО
«РостГМУ» Минздрава России
Адрес: 344022, Ростов-на-Дону, пер. Нахичеванский, д. 29, тел.: (863) 232-73-58; e-mail: detinfrostov@gmail.com
Статья поступила: 12.10.2012 г., принята к печати: 15.01.2013 г.
Высокая заболеваемость, частое развитие тяжелых форм осложнений, неблагоприятные отдаленные последствия
для здоровья детей, недостаточная эффективность применяемых схем терапии острых респираторных инфекций
диктуют необходимость совершенствования программы лечения этой группы заболеваний. Проведено комплексное
клинико-лабораторное обследование 72 детей в возрасте от 3 до 6 лет с острыми ринофарингитами и бронхитами.
Выявлена зависимость клинической формы заболевания, особенностей течения от состояния преморбидного фона
и выраженности изменений иммунного статуса. Установлено, что включение инозина пранобекс в комплексное
лечение острых респираторных инфекций у детей способствует быстрой положительной динамике клинической сим-
34
птоматики и показателей иммунного статуса, не сопровождается развитием побочных эффектов. Таким образом,
высокая эффективность и безопасность применения инозина пранобекс позволяют рекомендовать включение этого
препарата в программу лечения детей старше трех лет жизни с острыми респираторными инфекциями независимо
от формы заболевания и состояния иммунного статуса.
Ключевые слова: острые респираторные инфекции, дети, инозин пранобекс.
(Педиатрическая фармакология. 2013; 10 (1): 0–0)
Проблема острых респираторных инфекций (ОРИ) оста- стую приобретают тяжелое течение и у 20–30% больных
ется по-прежнему одной из наиболее актуальных в совре- сопровождаются развитием осложнений [3, 6]. К небла-
менной педиатрии и детской инфектологии. Это связано гоприятным последствиям перенесенных ОРИ относятся
не только с высокой заболеваемостью ОРИ в популяции возникновение вторичного иммунодефицитного состоя-
детского населения, но и с неблагоприятными послед- ния (ИДС), дисбиоз слизистых оболочек, нарушение нор-
ствиями инфекций респираторного тракта для здоровья мального роста и развития ребенка, созревание функцио-
ребенка, всего общества в целом [1–3]. В настоящее нальных систем, формирование хронической патологии
время заболеваемость ОРИ у детей сохраняется на высо- ЛОР-органов, легких, почек, желудочно-кишечного тракта,
ком уровне (65–70 тыс. на 100 тыс.) и превышает анало- центральной нервной системы (ЦНС), аллергических забо-
гичный показатель у взрослых в 3–4 раза [4]. Наиболее леваний [7, 8]. Проблема ОРИ имеет не только медицин-
высокий показатель заболеваемости регистрируют в воз- ские, но и социально-экономические аспекты. Доказано,
растной группе от 2 до 6 лет [5]. На долю ОРИ приходится что у детей с повторными эпизодами ОРИ достаточно
до 90% заболеваний детского возраста и до 80% обра- часто возникает социальная дезадаптация, снижает-
щений за медицинской помощью [3]. ОРИ у детей зача- ся успеваемость в школе, нарушается качество жизни
Avtor
Uchrejdenie
Zagolovok
Rezume.
(Pediatricheskaya farmakologiya — Pediatric pharmacology. 2013; 10 (1): 0–0)](https://image.slidesharecdn.com/simovanyanpf120132-130416165100-phpapp01/85/Simovan-yan-pf1-2013_2-1-320.jpg)
![не только самого ребенка, но и членов его семьи. Весьма активности вируса Эпштейна–Барр (ВЭБ); положительная
высоким является экономический ущерб для государства динамика иммунологических показателей, характеризую-
и общества в целом [1, 3]. щих активацию иммунокомпетентных клеток, иммунный
В связи с этим нуждается в совершенствовании такти- ответ по клеточному и гуморальному типу, факторы врож-
ка лечебных мероприятий, о чем свидетельствуют факты денной резистентности [14]. Аналогичные данные полу-
недостаточной эффективности применяемых схем, увели- чены М. С. Савенковой и соавт., которые использовали
чения частоты заболеваний после окончания терапии, раз- инозин пранобекс у детей с хронической герпесвирусной
вития побочных эффектов, особенно в случае полипрагма- инфекцией, вызванной ВЭБ, цитомегаловирусом, а также
зии [3, 6]. Это диктует необходимость разработки новых смешанной хламидийно-микоплазменной инфекцией [11].
подходов к лечению больных ОРИ с использованием пре- На фоне лечения этим препаратом отмечена положитель-
паратов комплексного этиопатогенетического действия, ная динамика клинической симптоматики, уменьшение
обладающих высокой эффективностью и безопасностью. частоты выявления лабораторных показателей активности
Перспективным направлением совершенствования инфекционного процесса.
терапии ОРИ у детей представляется использование в ком- В последние годы появились данные об эффективно-
плексном лечении инозина пранобекс (Изопринозин, Teva сти использования инозина пранобекс у детей при ОРИ.
Pharmaceutical Industries Ltd, Израиль). Этот препарат Так, исследование, проведенное Л. В. Осидак и соавт.,
обладает комплексной противовирусной, иммуномодули- показало, что на фоне приема препарата происходи-
рующей и цитопротективной активностью. Инозин прано- ло сокращение продолжительности симптомов ОРИ —
бекс тормозит репликацию широкого спектра ДНК- и РНК- лихорадки, интоксикации, катаральных симптомов [11].
содержащих вирусов [9]. Противовирусная активность В. А. Булгакова и соавт. исследовали эффективность пре-
препарата обусловлена изменением стереохимической парата при ОРИ у детей, страдающих атопической бронхи-
структуры рибосом за счет встраивания в них инозин- альной астмой [12]. Установлено, что назначение инозина
оротовой кислоты [10]. В результате не происходит присое- пранобекс способствовало уменьшению длительности
динения адениловой кислоты к вирусной РНК, и нарушает- симптомов ОРИ и предупреждало развитие обострений
ся синтез вирусных белков. В опытах на культурах клеток, бронхиальной астмы. Эффективность препарата авторы
проведенных Л. В. Осидак и соавт., доказано наличие у ино- связывают с противовирусным действием, что докумен-
35
зина пранобекс противовирусной активности в отношении тировано снижением выделения из носоглоточной слизи
возбудителей ОРИ, в том числе вирусов гриппа, парагрип- респираторных вирусов, а также с его иммуномодули-
ПЕДИАТРИЧЕСКАЯ ФАРМАКОЛОГИЯ /2013/ ТОМ 10/ № 1
па, респираторно-синцитиального вируса [11]. Подавление рующей активностью — поляризацией иммунного ответа
репликации вируса гриппа отмечено как до заражения в сторону Th1, повышением продукции IFN ␥ и IL 2.
культуры клеток (профилактический режим), так и после Вместе с тем требует уточнения ряд аспектов приме-
ее инфицирования (терапевтический режим). Кроме того, нения инозина пранобекс при ОРИ у детей. Это касается,
применение инозина пранобекс при экспериментальной прежде всего, оценки эффективности использования
летальной гриппозной инфекции у белых мышей приводи- препарата при различных формах острой респираторной
ло к снижению смертности лабораторных животных: в отли- патологии. Кроме того, нуждаются в исследовании имму-
чие от группы контроля отмечено уменьшение титра вируса номодулирующая активность инозина пранобекс, в том
гриппа в легочной ткани, что, по мнению авторов, является числе влияние препарата на систему IFN. Все это послу-
несомненным достоинством этого препарата. жило предпосылкой для проведения данного клинико-
Кроме того, инозин пранобекс обладает иммунокор- иммунологического исследования.
ригирующей активностью [9, 10, 12, 13]. Он модулирует Цель исследования — оценить эффективность вклю-
иммунный ответ по клеточному типу — увеличивает функци- чения инозина пранобекс в комплексную терапию ОРИ
ональную активность Т хелперов 1-го типа (Th1), продукцию у детей.
интерлейкина (IL) 2, интерферона (IFN) ␥, ускоряет диффе-
ренцировку предшественников Т лимфоцитов в Т хелперы ПАЦИЕНТЫ И МЕТОДЫ
и цитотоксические CD8 лимфоциты. Усиление иммунного Обследовано 72 ребенка в возрасте от 3 до 6 лет
ответа по клеточному типу связано также с повышением с острыми респираторными инфекциями, протекавшими
хемотаксической и фагоцитарной активности макрофагов, в форме острого ринофарингита (38 человек; 52,8%)
выработки этими клетками IL 1. Происходит улучшение и острого бронхита (34 человека; 47,2%). Методом слу-
функциональной активности нейтрофилов и естественных чайной выборки пациенты были распределены на две
киллерных клеток. Сочетание прямого подавления репли- группы, сопоставимые по клинико-лабораторным показа-
кации вирусов с активацией клеточного иммунитета потен- телям на момент начала лечения. Обе группы насчитыва-
цирует противовирусную активность препарата. Кроме ли по 36 детей, из них с острым ринофарингитом — по 19,
того, инозин пранобекс оказывает влияние на иммунный с острым бронхитом — по 17), соответственно, в каждой
ответ по гуморальному типу. Препарат способствует диф- группе. Пациентам 1-й группы назначали стандартное
ференцировке В лимфоцитов в плазматические клетки лечение: дезинтоксикационную терапию, поливитамины,
и стимулирует продукцию иммуноглобулинов (Ig) классов A, местные антисептики, по показаниям антибиотики, муко-
M и G. Установлено также, что инозин пранобекс улучшает литики, жаропонижающие, антигистаминные препараты,
обменные процессы в пораженных клетках. ингаляции и др. Пациентам 2-й группы помимо стандарт-
Имеется опыт использования инозина пранобекс при ной терапии назначали инозин пранобекс в дозе 50 мг/кг
различных инфекционных заболеваниях — герпесвирус- в сут в 3–4 приема внутрь в течение 10 дней.
ных инфекциях, кори, эпидемическом паротите, вирусных Клинико-иммунологическое обследование пациен-
гепатитах, папилломавирусной инфекции, подостром скле- тов осуществляли до начала лечения и через 10 дней.
розирующем панэнцефалите и др. [12, 13]. Так, в проведен- Определение различных типов иммунокомпетентных кле-
ном нами исследовании установлено, что при назначении ток проводили методом непрямой иммунофлуоресценции
инозина пранобекс детям с хронической Эпштейна–Барр с использованием соответствующих мышиных монокло-
вирусной инфекцией имели место уменьшение частоты нальных антител («Сорбент ЛТД», Россия): для Т лимфоци-
лимфопролиферативного, интоксикационного, инфекцион- тов — CD3, для Т хелперов — CD4, для цитотоксических
ного и церебрального синдромов, лабораторных маркеров Т лимфоцитов — CD8, для клеток в состоянии ранней](https://image.slidesharecdn.com/simovanyanpf120132-130416165100-phpapp01/85/Simovan-yan-pf1-2013_2-2-320.jpg)

![резистентности, иммунного ответа по клеточному и гумо- интоксикации, влажного кашля, хрипов в легких, а также
ральному типам [1–3]. Кроме того, неблагоприятное частым развитием осложнений.
влияние оказывают экзогенные и эндогенные факторы Оптимизация лечения ОРИ заключается во включе-
риска, которые приводят к нарушению функции барьер- нии в программу терапии Изопринозина, приводяще-
ных механизмов респираторного тракта, функциональ- го к выраженной положительной динамике клинико-
ных систем организма ребенка в целом, формированию иммунологических показателей у 94,4% больных, что
вторичного ИДС [6–8]. является следствием комплексной противовирусной,
В результате незрелости защитных систем организма иммунокорригирующей и цитопротективной активности
ребенка, влияния факторов риска, наличия фонового ИДС, препарата [9–13]. Независимо от формы ОРИ отме-
иммунодепрессивной активности возбудителей у больных чается быстрая положительная динамика клинических
развиваются не только признаки активации, но и повреж- симптомов — проявлений общеинфекционного и ката-
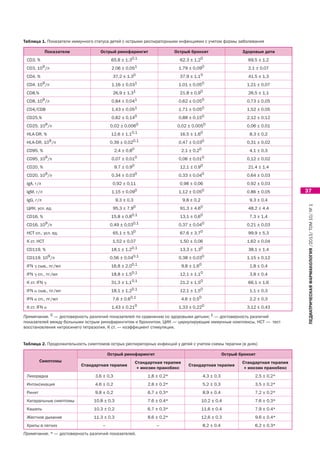
дения иммунной системы. У обследованных больных обна- рального синдромов. Препарат обладает достаточно
ружено нарушение процессов активации, пролиферации, широким спектром иммуномодулирующей активности.
дифференцировки иммунокомпетентных клеток — умень- Иммунокорригирующее действие инозина пранобекс
шение содержания CD3-, CD4-, CD8 лимфоцитов, клеток заключается в модуляции иммунного ответа по клеточ-
с маркером ранней активации (CD25), экспрессирующих ному типу — нормализации CD3-, CD4-, увеличении
рецептор готовности к апоптозу (CD95), увеличение числа CD8 лимфоцитов. Отмечается стимуляция антителогене-
лимфоцитов в состоянии поздней активации (HLA-DR), за (увеличение IgA, переключение синтеза с IgM на IgG)
снижение CD20 лимфоцитов, продукции IgA, IgG, повыше- на фоне улучшения элиминации ЦИК. Со стороны фак-
ние ЦИК, увеличение CD16 клеток, угнетение метаболиче- торов врожденной резистентности имеет место повы-
ской активности нейтрофилов, нарушение состояния IFN- шение количества естественных киллерных клеток, вос-
статуса (увеличение продукции IFN ␥, IFN ␣, уменьшением становление метаболической активности нейтрофилов.
экспрессии CD119 рецептора). Препарат влияет также на IFN-статус — восстанавливает
Поражение клеток-мишеней инфекционными аген- продукцию IFN ␥ и IFN ␣, улучшает их рецепцию.
тами в условиях иммуносупрессии приводит к формиро- Изопринозин хорошо переносится больными. Высокая
ванию очага воспаления в слизистой оболочке респи- клиническая эффективность препарата, широкий спектр
40
раторного тракта, что клинически манифестирует в виде иммуномодулирующей активности, безопасность при-
симптоматики общеинфекционного и катарального син- менения позволяют рекомендовать включение инозина
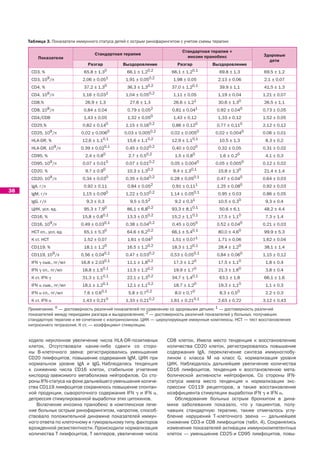
дромов [3, 6]. У больных с острым ринофарингитом имеют пранобекс в комплекс лечения ОРИ у детей старше трех
место низкая частота групп риска, умеренные изменения лет жизни независимо от формы заболевания и характе-
иммунного статуса. Клиническая симптоматика включает ра нарушений иммунного статуса.
субфебрилитет и умеренно выраженные симптомы инток-
сикации в сочетании с яркими катаральными явления- ВЫВОДЫ
ми — выраженной ринореей, сухим кашлем, гиперемией 1. Клиническая форма и характер течения ОРИ у детей
слизистой оболочки ротоглотки. зависят от патогенных свойств возбудителя, а также
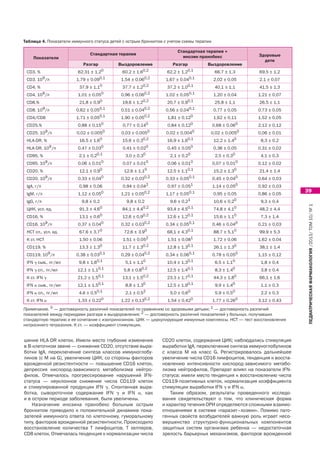
У больных острым бронхитом выявлена высокая от состояния преморбидного фона пациента, выра-
частота анамнестических факторов риска, зарегистри- женности изменений иммунного статуса.
рованы более глубокие нарушения со стороны адаптив- 2. Для повышения эффективности лечения ОРИ у детей
ного иммунного ответа по клеточному и гуморальному в комплекс лечебных мероприятий необходимо вклю-
типам, показателей активации иммунокомпетентных кле- чать инозин пранобекс, который способствует сокра-
ток, факторов врожденной резистентности (системы IFN, щению продолжительности симптомов заболевания,
CD16 лимфоцитов). При этом выраженность воспали- положительной динамике иммунологических показа-
тельной реакции в слизистой оболочке респираторного телей и обладает хорошей переносимостью.
тракта более значительная, в связи с чем клиническая 3. Инозин пранобекс показан больным ОРИ старше
симптоматика острого бронхита характеризуется появ- трех лет жизни независимо от формы заболевания
лением фебрильной лихорадки, выраженных симптомов и характера нарушений иммунного статуса.
СПИСОК ЛИТЕРАТУРЫ
1. Альбицкий В. Ю., Баранов А. А., Камаев И. А., Огнева М. Л. Часто 8. Зайцева О. В. Острые респираторные инфекции и их
болеющие дети. Нижний Новгород: Изд-во НГМА. 2003. 180 с. осложнения в детской практике. Практика педиатра. 2011;
2. Намазова Л. С., Ботвиньева В. В., Торшхоева Р. М. и др. 2: 64–67.
Лечение и профилактика острых респираторных инфекций 9. Исаков В. А., Архипова Е. И., Исаков Д. В. Герпесвирусные
у часто болеющих детей, проживающих в мегаполисах. Детские инфекции человека. СПб.: Спецлит. 2006. 303 с.
инфекции. 2007; 2: 49–52. 10. Ершов Ф. И. Антивирусные препараты: Справочник. М.:
3. Острые респираторные заболевания у детей: лечение и про- ГЭОТАР-Медиа. 2006. 311 с.
филактика. Научно-практическая программа Союза педиатров 11. Осидак Л. В., Зарубаев В. В., Образцова Е. В. и др. Изопри-
России. Под ред. А. А. Баранова. М., 2002. 69 с. нозин в терапии ОРВИ у часто болеющих детей. Детские инфек-
4. Вознесенская Н. И., Маргиева Т. В. Острые респираторные ции. 2008; 4: 35–41.
инфекции у детей — выбор тактики ведения. Педиатрическая 12. Булгакова В. А., Балаболкин И. И., Ханова Н. И. и др.
фармакология. 2011; 2: 102–106. Применение изопринозина (инозин пранобекс) для про-
5. Самсыгина Г. А. О рецидивирующих инфекциях респиратор- филактики и лечения респираторных инфекций у детей. М.,
ного тракта и диспансерной группе часто болеющих детей. 2010. 19 с.
Детские инфекции. 2012; 3: 52–53. 13. Савенкова М. С., Афанасьева А. Л., Минасян В. С., Тюркина С. И.
6. Таточенко В. К., Рачинский С. В., Волков И. К. и др. Практи- Лечение часто болеющих детей со смешанной инфекцией.
ческая пульмонология детского возраста. М., 2006. 250 с. Вопросы современной педиатрии. 2011; 4; 83–88.
7. Коровина Н. А., Заплатников А. Л., Леписева И. В. и др. 14. Симованьян Э. Н., Денисенко В. Б., Сарычев А. М., Григорян А. В.
Современные возможности иммунопрофилактики острых респи- Хроническая инфекция вируса Эпштейна–Барр у детей: совре-
раторных инфекций у часто болеющих детей. Педиатрическая менные аспекты диагностики и лечения. Consilium medicum.
фармакология. 2008; 1: 21–25. Приложение «Педиатрия». 2006; 2: 29–35.](https://image.slidesharecdn.com/simovanyanpf120132-130416165100-phpapp01/85/Simovan-yan-pf1-2013_2-7-320.jpg)
