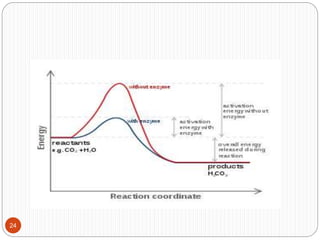
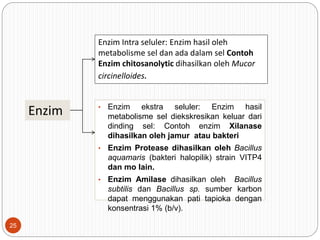
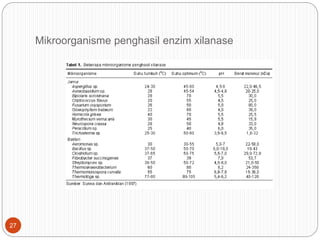
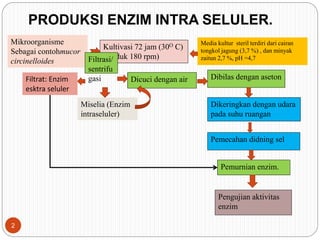
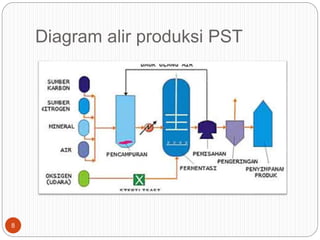
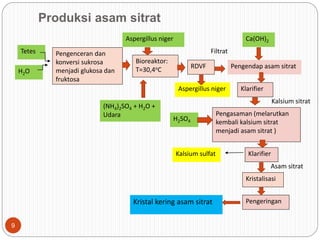
Dokumen ini membahas proses produksi enzim intraseluler dan ekstra seluler dari mikroorganisme, termasuk metode pemecahan dinding sel dan pemurnian enzim. Selain itu, dijelaskan tentang produksi protein sel tunggal dari mikroba serta keuntungan dan aplikasi mikroorganisme tertentu dalam menghasilkan protein dan enzim. Penjelasan mengenai struktur, mekanisme, dan penamaan enzim juga disertakan.






![Sekilas mengenai enzim
(Wikipedia Free Enciklopedia).
Hal-ihwal yang berkaitan dengan enzim dipelajari dalam
enzimologi. Dalam dunia pendidikan tinggi, enzimologi tidak
dipelajari tersendiri sebagai satu jurusan tersendiri tetapi
sejumlah program studi memberikan mata kuliah ini. Enzimologi
terutama dipelajari dalam kedokteran, ilmu pangan, teknologi
pengolahan pangan, dan cabang-cabang ilmu pertanian.
Pada akhir tahun 1700-an dan awal tahun 1800-an, pencernaan
daging oleh sekresi perut[3] dan konversi pati menjadi gula oleh
ekstrak tumbuhan dan ludah telah diketahui. Namun, mekanisme
bagaimana hal ini terjadi belum diidentifikasi.[4]
10](https://image.slidesharecdn.com/pertemuan14produkenzim-211028213926/85/PRODUKSI-ENZIM-10-320.jpg)
![ Pada tahun 1897, Eduard Buchner memulai kajiannya mengenai
kemampuan ekstrak ragi untuk memfermentasi gula walaupun ia
tidak terdapat pada sel ragi yang hidup. Pada sederet
eksperimen di Universitas Berlin, ia menemukan bahwa gula
difermentasi bahkan apabila sel ragi tidak terdapat pada
campuran.[6] Ia menamai enzim yang memfermentasi sukrosa
sebagai "zymase" (zimase).[7] Pada tahun 1907, ia menerima
penghargaan Nobel dalam bidang kimia "atas riset biokimia dan
penemuan fermentasi tanpa sel yang dilakukannya". Mengikuti
praktek Buchner, enzim biasanya dinamai sesuai dengan reaksi
yang dikatalisasi oleh enzim tersebut. Umumnya, untuk
mendapatkan nama sebuah enzim, akhiran -ase ditambahkan
pada nama substrat enzim tersebut (contohnya: laktase,
merupakan enzim yang mengurai laktosa) ataupun pada jenis
reaksi yang dikatalisasi (contoh: DNA polimerase yang
menghasilkan polimer DNA).
11](https://image.slidesharecdn.com/pertemuan14produkenzim-211028213926/85/PRODUKSI-ENZIM-11-320.jpg)
![ Penemuan bahwa enzim dapat bekerja diluar sel hidup
mendorong penelitian pada sifat-sifat biokimia enzim tersebut.
Banyak peneliti awal menemukan bahwa aktivitas enzim
diasosiasikan dengan protein, namun beberapa ilmuwan seperti
Richard Willstätter berargumen bahwa proten hanyalah
bertindak sebagai pembawa enzim dan protein sendiri tidak
dapat melakukan katalisis. Namun, pada tahun 1926, James B.
Sumner berhasil mengkristalisasi enzim urease dan
menunjukkan bahwa ia merupakan protein murni.
Kesimpulannya adalah bahwa protein murni dapat berupa enzim
dan hal ini secara tuntas dibuktikan oleh Northrop dan Stanley
yang meneliti enzim pencernaan pepsin (1930), tripsin, dan
kimotripsin. Ketiga ilmuwan ini meraih penghargaan Nobel tahun
1946 pada bidang kimia.[8]
12](https://image.slidesharecdn.com/pertemuan14produkenzim-211028213926/85/PRODUKSI-ENZIM-12-320.jpg)
![ Penemuan bahwa enzim dapat dikristalisasi pada akhirnya
mengijinkan struktur enzim ditentukan melalui kristalografi sinar-
X. Metode ini pertama kali diterapkan pada lisozim, enzim yang
ditemukan pada air mata, air ludah, dan putih telur, yang
mencerna lapisan pelindung beberapa bakteri. Struktur enzim ini
dipecahkan oleh sekelompok ilmuwan yang diketuai oleh David
Chilton Phillips dan dipublikasikan pada tahun 1965.[9] Struktur
lisozim dalam resolusi tinggi ini menandai dimulainya bidang
biologi struktural dan usaha untuk memahami bagaimana enzim
bekerja pada tingkat atom.
13](https://image.slidesharecdn.com/pertemuan14produkenzim-211028213926/85/PRODUKSI-ENZIM-13-320.jpg)


![ Enzim umumnya merupakan protein globular dan ukurannya
berkisar dari hanya 62 asam amino pada monomer 4-oksalokrotonat
tautomerase[10], sampai dengan lebih dari 2.500 residu pada asam
lemak sintase.[11] Terdapat pula sejumlah kecil katalis RNA, dengan
yang paling umum merupakan ribosom; Jenis enzim ini dirujuk
sebagai RNA-enzim ataupun ribozim. Aktivitas enzim ditentukan oleh
struktur tiga dimensinya (struktur kuaterner).[12] Walaupun struktur
enzim menentukan fungsinya, prediksi aktivitas enzim baru yang
hanya dilihat dari strukturnya adalah hal yang sangat sulit.[13]
Sama seperti protein-protein lainnya, enzim merupakan rantai asam
amino yang melipat. Tiap-tiap urutan asam amino menghasilkan
struktur pelipatan dan sifat-sifat kimiawi yang khas. Rantai protein
tunggal kadang-kadang dapat berkumpul bersama dan membentuk
kompleks protein. Kebanyakan enzim dapat mengalami denaturasi
(yakni terbuka dari lipatannya dan menjadi tidak aktif) oleh
pemanasan ataupun denaturan kimiawi. Tergantung pada jenis-jenis
enzim, denaturasi dapat bersifat reversibel maupun ireversibel.
16](https://image.slidesharecdn.com/pertemuan14produkenzim-211028213926/85/PRODUKSI-ENZIM-16-320.jpg)
![Kespesifikan
Enzim biasanya sangat spesifik terhadap reaksi yang ia kataliskan
maupun terhadap substrat yang terlibat dalam reaksi. Bentuk,
muatan dan katakteristik hidrofilik/hidrofobik enzim dan substrat
bertanggung jawab terhadap kespesifikan ini. Enzim juga dapat
menunjukkan tingkat stereospesifisitas, regioselektivitas, dan
kemoselektivitas yang sangat tinggi.[15]
Beberapa enzim yang menunjukkan akurasi dan kespesifikan
tertinggi terlibat dalam pengkopian dan pengekspresian genom.
Enzim-enzim ini memiliki mekanisme "sistem pengecekan ulang".
Enzim seperti DNA polimerase mengatalisasi reaksi pada langkah
pertama dan mengecek apakah produk reaksinya benar pada
langkah kedua.[16] Proses dwi-langkah ini menurunkan laju
kesalahan dengan 1 kesalahan untuk setiap 100 juta reaksi pada
polimerase mamalia.[17] Mekanisme yang sama juga dapat
ditemukan pada RNA polimerase,[18] aminoasil tRNA sintetase[19] dan
ribosom.[20]
17](https://image.slidesharecdn.com/pertemuan14produkenzim-211028213926/85/PRODUKSI-ENZIM-17-320.jpg)
![ Beberapa enzim yang menghasilkan metabolit sekunder
dikatakan sebagai "tidak pilih-pilih", yakni bahwa ia dapat
bekerja pada berbagai jenis substrat yang berbeda-beda.
Diajukan bahwa kespesifikan substrat yang sangat luas ini
sangat penting terhadap evolusi lintasan biosintetik yang baru.[21]
Model "kunci dan gembok"
Enzim sangatlah spesifik. Pada tahun 1894, Emil Fischer
mengajukan bahwa hal ini dikarenakan baik enzim dan substrat
memiliki bentuk geometri yang saling memenuhi.[22] Hal ini sering
dirujuk sebagai model "Kunci dan Gembok". Manakala model ini
menjelaskan kespesifikan enzim, ia gagal dalam menjelaskan
stabilisasi keadaan transisi yang dicapai oleh enzim. Model ini
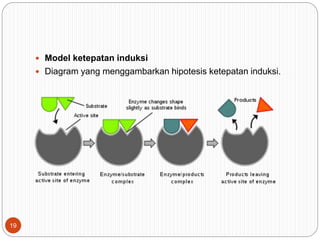
telah dibuktikan tidak akurat, dan model ketepatan induksilah
yang sekarang paling banyak diterima.
18](https://image.slidesharecdn.com/pertemuan14produkenzim-211028213926/85/PRODUKSI-ENZIM-18-320.jpg)
![Kofaktor dan koenzim
Kofaktor
Beberapa enzim tidak memerlukan komponen tambahan untuk
mencapai aktivitas penuhnya. Namun beberapa memerlukan
pula molekul non-protein yang disebut kofaktor untuk berikatan
dengan enzim dan menjadi aktif.[38] Kofaktor dapat berupa zat
anorganik (contohnya ion logam) ataupun zat organik
(contohnya flavin dan heme). Kofaktor dapat berupa gugus
prostetik yang mengikat dengan kuat, ataupun koenzim, yang
akan melepaskan diri dari tapak aktif enzim semasa reaksi.
20](https://image.slidesharecdn.com/pertemuan14produkenzim-211028213926/85/PRODUKSI-ENZIM-20-320.jpg)
![ Enzim yang memerlukan kofaktor namun tidak terdapat kofaktor
yang terikat dengannya disebut sebagai apoenzim ataupun
apoprotein. Apoenzim beserta dengan kofaktornya disebut
holoenzim (bentuk aktif). Kebanyakan kofaktor tidak terikat
secara kovalen dengan enzim, tetapi terikat dengan kuat.
Namun, gugus prostetik organik dapat pula terikat secara
kovalen (contohnya tiamina pirofosfat pada enzim piruvat
dehidrogenase). Istilah holoenzim juga dapat digunakan untuk
merujuk pada enzim yang mengandung subunit protein
berganda, seperti DNA polimerase. Pada kasus ini, holoenzim
adalah kompleks lengkap yang mengandung seluruh subunit
yang diperlukan agar menjadi aktif.
Contoh enzim yang mengandung kofaktor adalah karbonat
anhidrase, dengan kofaktor seng terikat sebagai bagian dari
tapak aktifnya.[39]
21](https://image.slidesharecdn.com/pertemuan14produkenzim-211028213926/85/PRODUKSI-ENZIM-21-320.jpg)
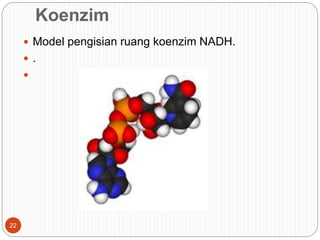
![ Koenzim adalah kofaktor berupa molekul organik kecil yang
mentranspor gugus kimia atau elektron dari satu enzim ke enzim
lainnya.[38][40][41] Contoh koenzim mencakup NADH, NADPH dan
adenosina trifosfat. Gugus kimiawi yang dibawa mencakup ion
hidrida (H–) yang dibawa oleh NAD atau NADP+, gugus asetil
yang dibawa oleh koenzim A, formil, metenil, ataupun gugus
metil yang dibawa oleh asam folat, dan gugus metil yang dibawa
oleh S-adenosilmetionina. Beberapa koenzim seperti riboflavin,
tiamina, dan asam folat adalah vitamin.
Oleh karena koenzim secara kimiawi berubah oleh aksi enzim,
adalah dapat dikatakan koenzim merupakan substrat yang
khusus, ataupun substrat sekunder. Sebagai contoh, sekitar 700
enzim diketahui menggunakan koenzim NADH.[42]
Regenerasi serta pemeliharaan konsentrasi koenzim terjadi
dalam sel. Contohnya, NADPH diregenerasi melalui lintasan
pentosa fosfat, dan S-adenosilmetionina melalui metionina
adenosiltransferase.
23](https://image.slidesharecdn.com/pertemuan14produkenzim-211028213926/85/PRODUKSI-ENZIM-23-320.jpg)