Dokumen ini adalah laporan praktikum mengenai pengujian amina dan turunannya yang dilakukan oleh Sabila Izzati di Fakultas Keguruan dan Ilmu Pendidikan Universitas Lampung. Tujuan praktik tersebut adalah untuk memahami reaksi-reaksi analisis gugus karboksilat dalam senyawa, dengan berbagai metode seperti oksidasi, hidrolisis, dan esterifikasi. Hasil pengamatan menunjukkan reaksi positif yang mengindikasikan adanya pembentukan asam karboksilat dan garam karboksilat dengan ciri fisika dan kimia yang khas.










![1.
2.
0,5 ml Na-Asetat + 0,5 ml
FeCl3hingga terbentuk warna
merah. Dipanaskan
Diamati perubahan yang terjadi.
Warna orange
Warna orange tua
4.2 Pembahasan
1. Pembentukan Asam Karboksilat
a. Oksidasi aldehid
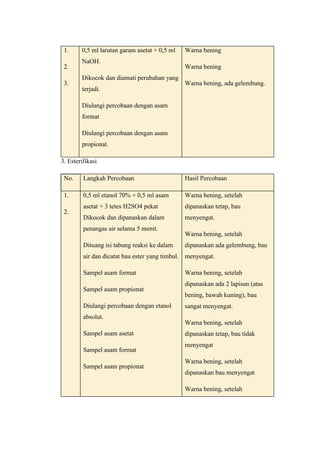
Langkah pertama yang perlu dilakukan adalah memasukkan 0,5 ml KMnO4 ke
dalam tabung reaksi dan menambahkan 2 tetes H2SO4 pekat. Kemudian dikocok
agar larutan homogen. Menambahkan 0,5 ml sampel asetaldehid lalu dipanaskan
dalam penangas air, pemanasan dilakukan untuk mempercepat reaksi yang
berlangsung. Maka didapatkan perubahan yang terjadi adalah larutan terasa panas,
mengalami perubahan warna dari ungu menjadi cokelat, muncul gelembung, dan
bau menyengat. Percobaan di atas menunjukkan adanya reaksi positif dari sampel
asetaldehid karena terbentuknya asam karboksilat yang dibuktikan dengan bau
yang menyengat. Reaksi yang terjadi adalah sebagai berikut:
O
R C H + [ O ] RCO2H
b. Hidrolisis ester
Langkah pertama yang perlu dilakukan adalah memasukkan ke dalam tabung
reaksi 0,25 ml H2SO4 dan 0,5 ml etil asetat. Maka didapatkan perubahan yang
terjadi adalah larutan terasa panas berwarna bening, dan bau yang dihasilkan
adalah bau balon. Hal tersebut menunjukkan adanya reaksi positif dari etil asetat
karena munculnya bau balon yang menunjukkan ada proses pembentukan asam
karboksilat. Reaksi yang terjadi adalah sebagai berikut:
O](https://image.slidesharecdn.com/pengujianaminadanturunanny1-140522093215-phpapp02/85/Pengujian-amina-dan-turunanny1-13-320.jpg)




![Fehling A dan B (Kalor)
CH3COOH + 2CuO CH2CO2 + H2O + Cu2O
Asam asetat
Fehling A dan B (Kalor)
CH2CH3COOH + 2CuO CH2CH2CO2 + H2O + Cu2O
Asam Propionat
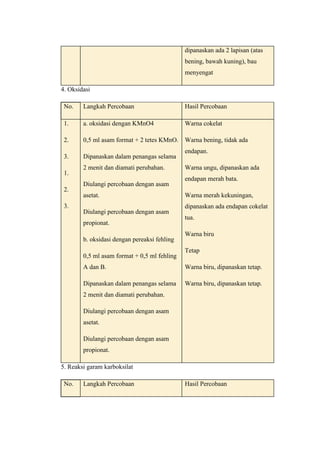
5. Reaksi garam karboksilat
Langkah pertama yang perlu dilakukan adalah dimasukkan ke dalam tabung
reaksi 0,5 ml Na-Asetat dan ditambahkan 0,5 ml FeCl3 hingga terbentuk warna
merah. Maka didapatkan larutan berwarna orange setelah dipanaskan warna
larutan berubah lagi menjadi warna orange tua. Hal tersebut menunjukan bahwa
terjadi reaksi positif dari na-asetat. Reaksi yang terjadi adalah sebagai berikut:
3NaCH3COO + FeCl3 3NaCl + 3CH3COO- + Fe3+
6CH3COO- + 3Fe3+ + 2H2O [Fe (OH)2 (CH3COO)6]+ + 2H+](https://image.slidesharecdn.com/pengujianaminadanturunanny1-140522093215-phpapp02/85/Pengujian-amina-dan-turunanny1-18-320.jpg)

