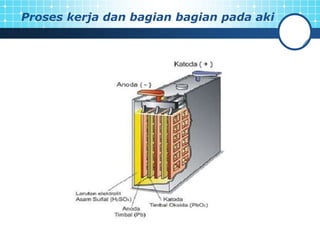
Dokumen ini membahas tentang fungsi dan proses kerja aki sebagai sumber arus listrik searah yang menyimpan energi kimia. Aki terdiri dari elektroda timbal dan larutan elektrolit asam sulfat, dan dapat diisi ulang untuk menyimpan energi kembali. Selain itu, dokumen menjelaskan perbedaan pengisian antara aki basah dan aki kering.