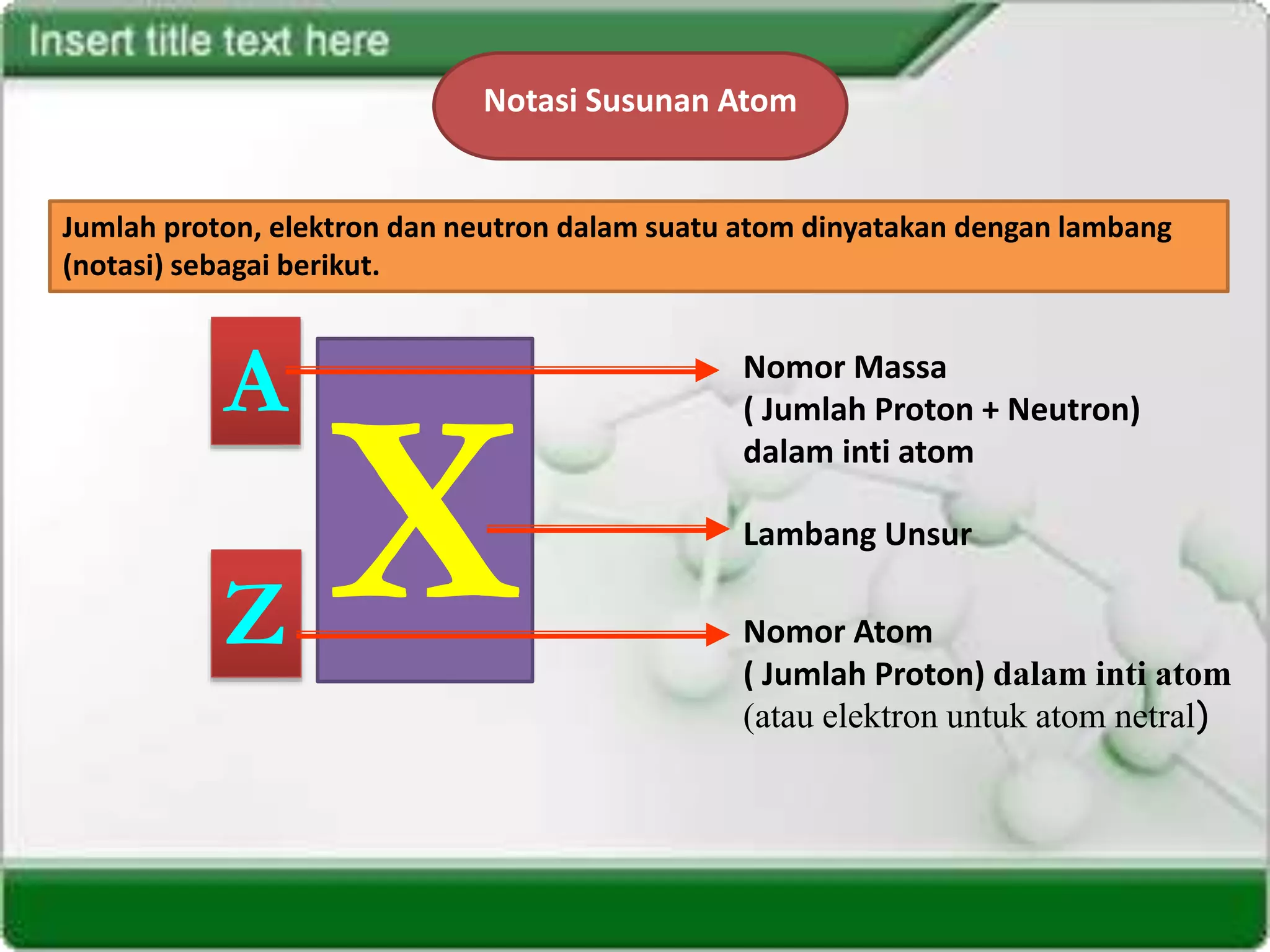
1. Nomor atom menunjukkan jumlah proton dan elektron dalam atom netral, sedangkan nomor massa menunjukkan jumlah proton dan neutron dalam inti atom.
2. Notasi susunan atom menyatakan lambang unsur, nomor atom, dan nomor massa untuk menunjukkan jumlah partikel dalam suatu atom.
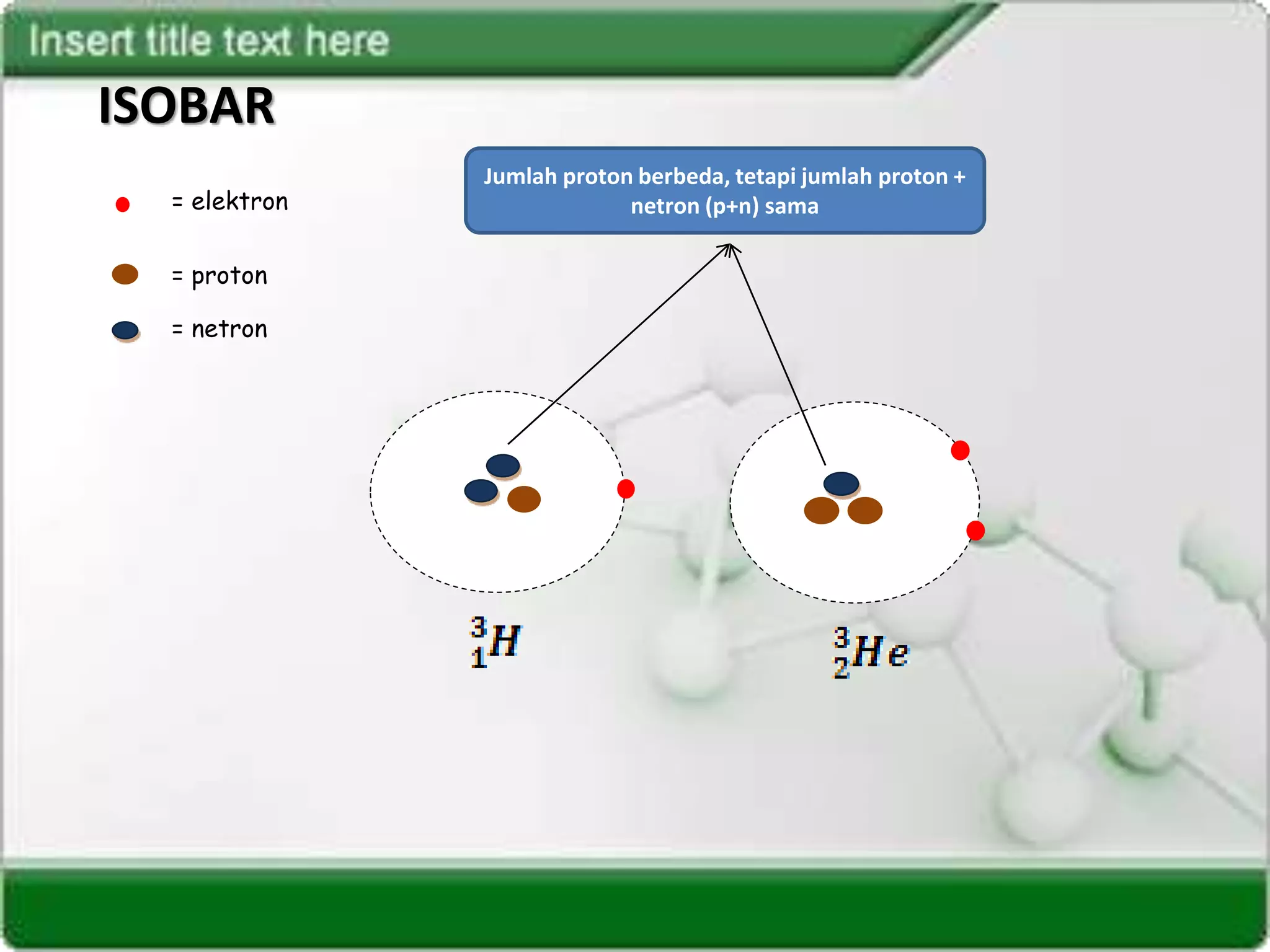
3. Terdapat tiga jenis pasangan atom yang berbeda berdasarkan jumlah partikelnya, yaitu isotop, isobar, dan isoton.