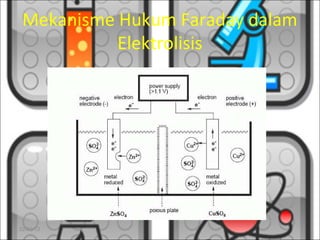
Hukum I Faraday menyatakan bahwa jumlah massa zat yang diendapkan pada elektroda sebanding dengan jumlah muatan listrik yang dialirkan melalui larutan elektrolit. Secara matematis, massa zat yang dibebaskan atau diendapkan oleh arus listrik sebanding dengan berat ekivalen zat tersebut dikalikan kuat arus dan waktu. Hukum ini kemudian diterapkan dalam proses elektrolisis untuk memproduksi logam.