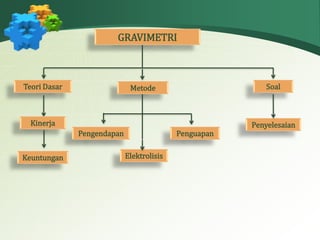
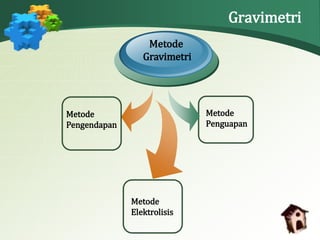
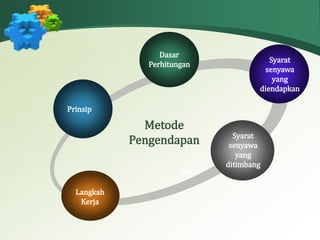
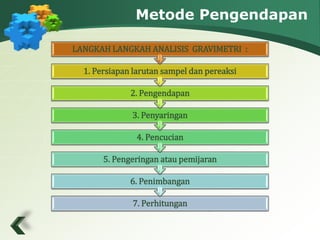
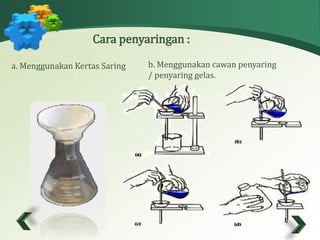
Dokumen ini membahas analisis gravimetri, yang merupakan metode kuantitatif untuk pemurnian dan penimbangan zat dengan prinsip pengendapan, penguapan, dan elektrolisis. Metode ini memerlukan sedikit peralatan dan memiliki akurasi tinggi, meskipun prosesnya relatif lambat. Dokumen juga menjelaskan langkah-langkah dan perhitungan dalam analisis gravimetri, serta contoh-contoh aplikasinya.