8 клас будова електронних оболонок атомів
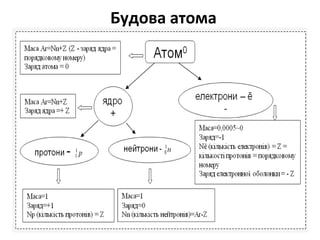
- 1. Будова атома
- 2. Стан електрона в атомі • Кожен електрон рухається навколо ядра так швидко, що його не тільки не можна розглянути за допомогою найпотужнішого мікроскопа, але неможливо навіть представити у вигляді крапки, що рухається по певній траєкторії. Електрон має подвійну природу (дуалізм)- частинки і хвилі. Електрони немов "розмазані" в просторі і утворюють електронні хмари – атомні орбіталі. • Навколо ядра електрони можуть утворювати орбіталі (хмари) різної форми:
- 3. s-орбіталь сферичну s-орбіталь – кулеподібну електронну хмару (немов нещільно намотаного клубка пухнастої шерсті або ватяної кульки). Вона найстійкіша і міститься найближче до ядра.
- 4. p-орбіталь: чим більше енергія електрона в атомі, тим швидше він обертається, тим сильніше витягується область його перебування і нарешті перетворюється на гантелеподібну p-орбіталь: Електронна хмара такої форми може займати в атомі три положення вздовж осей координат x, у і z:
- 5. Всі разом три електронні хмари, які називають px-, py- або pz-орбіталями, вони утворюють симетричну геометричну фігуру, в центрі якої знаходиться атомне ядро. Вона схожа на потрійний бант Отже, видів p-орбіталей може бути три, їхня енергія однакова, але положення в просторі різне.
- 6. Окрім s- і p-орбіталей, існують електронні орбіталі ще складнішої форми; їх позначають буквами d і f. Електрони, що потрапляють сюди, набувають ще більшого запасу енергії, складніших рухів, і у результаті утворюються складні і красиві об'ємні геометричні фігури. Всі d-орбіталі (а їх може бути вже п'ять) однакові за енергією, але по-різному розташовані в просторі. Та і формою, що нагадує перев'язану стрічками подушечку, однакові тільки чотири. А п'ята - на зразок гантелі, протягнутої в бублик.
- 7. Запам’ятай! Кількість орбіталей певного виду чітко визначена такими числами: s-орбіталь – 1, p-орбіталей – 3, d-орбіталей – 5, f-орбіталей – 7.
- 8. Електронна оболонка – це сукупність електронів, що рухаються в атомі навколо ядра. Дослідження фізиків показали, електрони в атомі розташовуються не безладно, а шарами – енергетичними рівнями. Ці рівні, подібно до поверхів у будинку – перший, другий, третій і так далі. Окрім того, кожен рівень поділяється на підрівні - s, p, d, f, на яких розташовуються атомні орбіталі – s, p, d, f. Чим більше номер "поверху" - рівня, тим "вище" (далі від ядра) знаходяться електрони цього рівня. На першому рівні може бути один-єдиний s-підрівень, на другому підрівнів вже два: s і р. На третьому "поверсі" три підрівні (s, p і d), на четвертому - чотири (s, p, d, f).
- 9. Запам’ятай! Кількість підрівнів дорівнює номеру рівня. • Перший рівень містить один підрівень – s, тому перший рівень можна записати як 1s. • Другий рівень містить два підрівні – s, p, позначаємо 2s2p. • Третій рівень містить три підрівні – s, p, d – запис матиме вигляд 3s3p3d. • Четвертий рівень містить чотири підрівні – s, p, d, f, звідки 4s4p4d4f. 1s 2s2p 3s3p3d 4s4p4d4f
- 10. Перший рівень є найближчим до ядра. Чим більший номер рівня, тим він далі від ядра і містить більшу кількість електронів Електрони певного рівня, а також і підрівня відрізняються між собою за енергією: чим далі від ядра, тим енергія притягування електрона менша. Вони розміщені на певній «енергетичній» висоті.
- 11. Вчені домовились позначати кожну орбіталь коміркою – квадратиком. На s-підрівні може знаходитися одна атомна орбіталь, а на p-підрівні їх може бути вже три (відповідно до трьох осей координат): Орбіталей d- і f-підрівня в атомі може бути вже п'ять і сім відповідно: s – одна орбіталь p – три орбіталі d – п’ять орбіталей f – сім орбіталей
- 12. Фізиками встановлено, що на кожній орбіталі може знаходитись максимально два електрони (правило, принцип Паулі), один з яких обертається навколо своєї осі за годинниковою стрілкою, а другий – проти. Це схематично зображують так Звідси, на s-підрівні міститься два електрона, на р- підрівні – шість, на d-підрівні – десять, на f–підрівні – чотирнадцять Запис 1s2 означає, що на одній s-орбіталі s-підрівня першого рівня міститься два електрона. Такий запис називається електронною конфігурацією і читається «один-ес-два».
- 13. За третім правилом (правилом Хунда): всі орбіталі одного підрівня (!) спочатку заповнюються одним, а потім другим електроном. Наприклад для р-орбіталей: Зверніть увагу, правилом користуються при заповнені підрівнів, але ні в якому разі рівнів! запис позначає один неспарений електрон (наполовину заповнену орбіталь) позначення двох спарених електронів (електрони знаходяться в парі)
- 25. Валентність елемента визначається кількістю неспарених електронів. При наданні атому додаткової енергії електрони останнього рівня “збуджуються” і переходять на рівень з більшою енергією, говорять, що атом з основного стану перейшов у *збуджений.