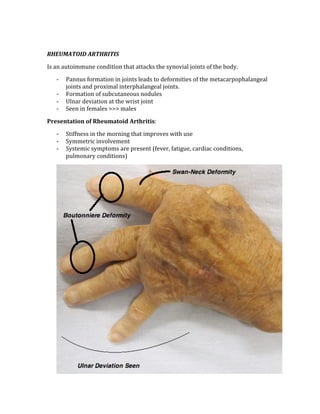
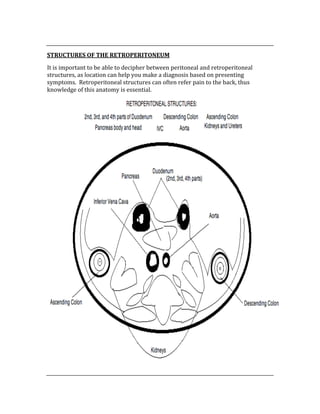
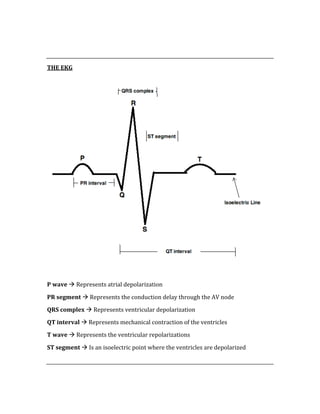
The document is a foreword for a study guide called "The USMLE Step 1 BIBLE" for the United States Medical Licensing Exam Step 1. It was written to help students understand medicine and score as high as possible on the exam. It covers high-yield topics in depth to adequately prepare students. The best way to use the guide is combined with a quality question bank.





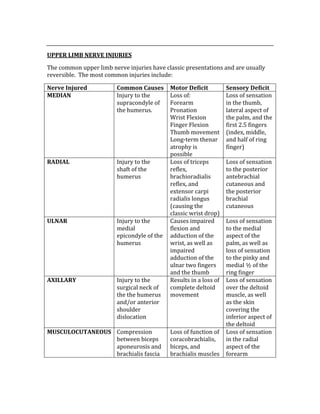

























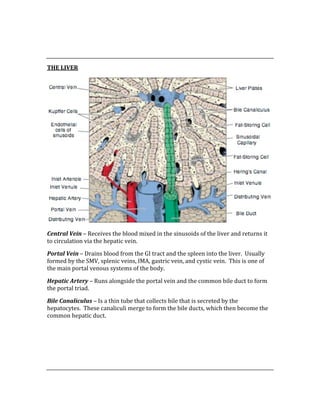














































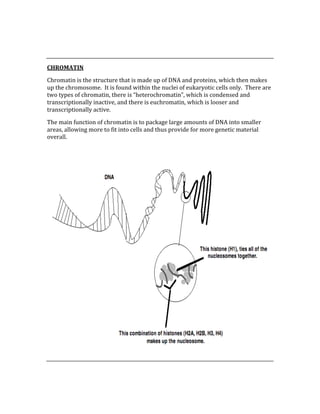
































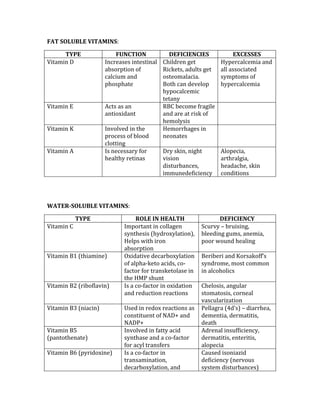








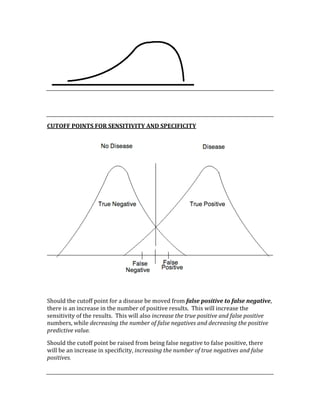
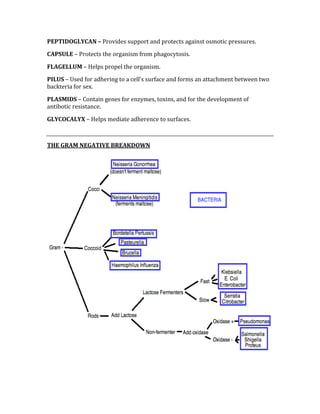
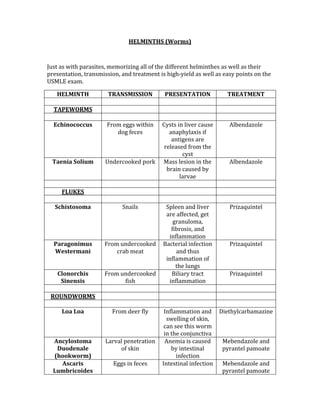
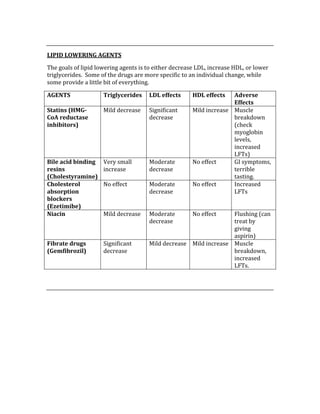
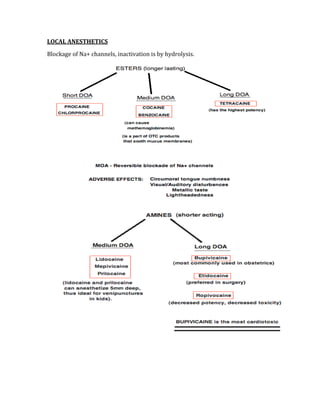
![Negative Predictive Value = d/d + c
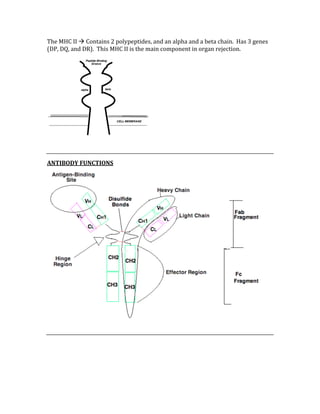
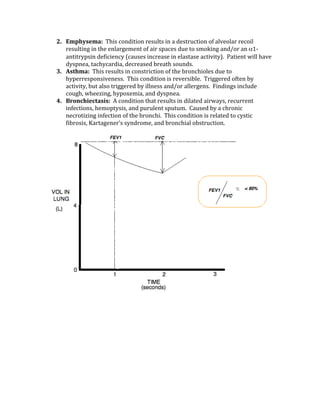
The NPV is used to determine the probability of not having a condition when the test
result is negative.
Odds Ratio = (a/b)/ (c/d)
The OR determines the incidence of disease in people in the exposed groups divided
by those in an unexposed group.
OR > 1 = States that the factor being studied is a risk factor for the outcome
OR<1 = States that the factor being studied is a protective factor in respect to the
outcome
OR = 1, States that no significant difference in outcome in either exposed or
unexposed group
Relative Risk = [a/(a+b) / d/(c+d)]
Relative risk compares the disease risk in people exposed to a certain factor with
disease risk in people who have not been exposed
Attributable Risk = [a/(a+b) – d/(c+d)]
The attributable risk is the number of cases that can be attributed to one risk factor
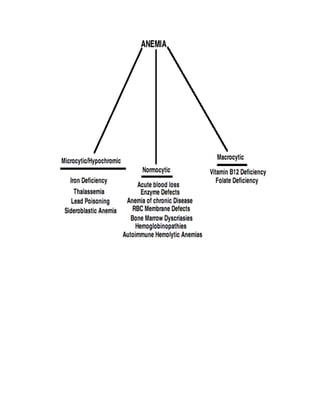
INCIDENCE vs. PREVALENCE
Incidence is the number of new cases of a disease over a unit time, whereas
prevalence is the total number of cases of a disease (both new and old) at a certain
point in time. Any disease treated with the sole purpose of prolonging life (ie
terminal cancers), the incidence stays the same but prevalence will increase.
Shortterm diseases: Incidence > Prevalence
Longterm diseases: Prevalence > Incidence
VALIDITY vs. RELIABILITY
Validity is simply a test’s ability to measure what it claims to measure, whereas the
reliability of a test determines its ability to consistent results on repeated attempts.](https://image.slidesharecdn.com/usmlestep1biblewithnotes-150512235651-lva1-app6891/85/Usmle-Step-1-Bible-201-320.jpg)
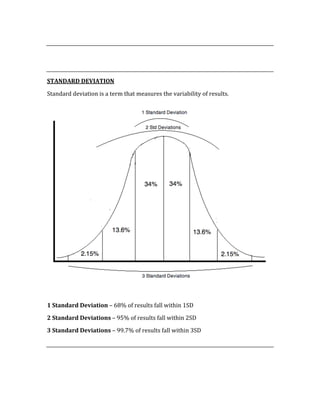
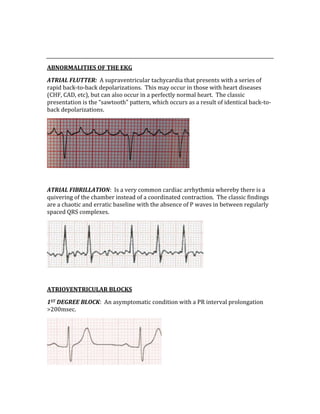
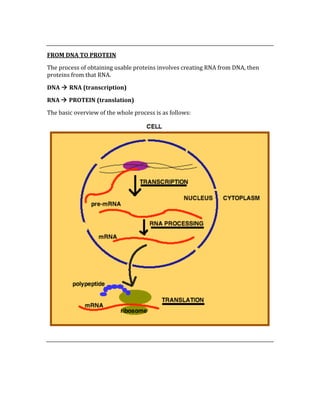
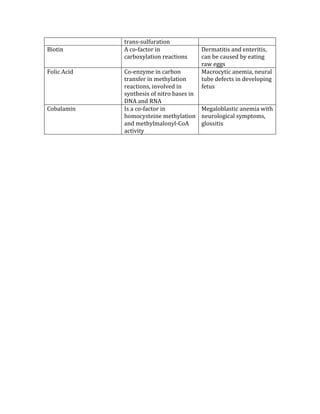
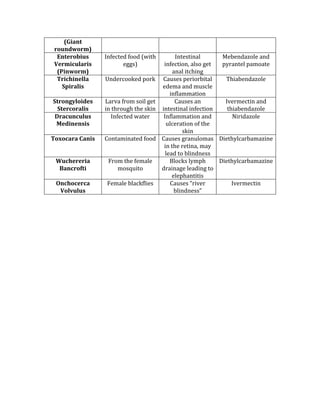
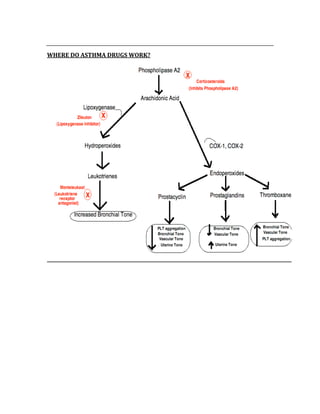
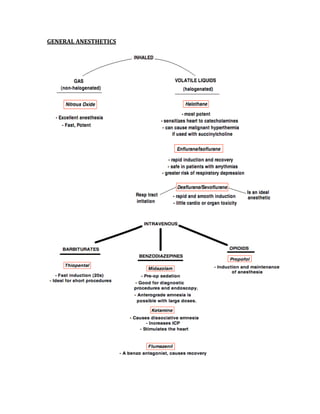
![CONFIDENCE INTERVAL AND pVALUE
These values strengthen the results of a study. For statistical significance, the CI
mustn’t contain the null value (RR = 1), and the closer the two numbers are
together, the more confident you can be that the results are statistically significant.
As far as the significance of the p‐value goes, a statistically significant result has a p‐
value of <0.05 (this means there is <5% chance that the results obtained were due
to chance alone).
CORRELATION COEFFICIENT
Two numbers that are between ‐1 and +1, it measures to what degree the variables
are related.
‐ A number of zero (0) means there is no correlation between variables.
‐ A number of +1 means there is a perfect correlation (both variables increase
or decrease proportionally)
‐ A number of ‐1 means there is a perfect negative correlation (variables move
in opposite directions proportionally)
ATTRIBUTABLE RISK PERCENT (ARP)
The ARP measures the impact of the particular risk factor being studied on a
particular population. It represents excess risk that can be explained by exposure to
a particular risk factor.
Calculate the ARP: ARP = [(RR ‐1)/RR]
STATISTICAL HYPOTHESES
The statistical hypotheses are used to determine whether or not there is an
association between risk factors and disease in a population. They are the ‘null
hypothesis’ and the ‘alternative’ hypothesis.
Null Hypothesis (Ho) – This hypothesis is the ‘hypothesis of no difference’, meaning
there is not an association between the disease and the risk factor.
Alternative Hypothesis (H1) – This hypothesis is the ‘hypothesis of some
difference’, meaning there is an association between the disease and the risk factor.](https://image.slidesharecdn.com/usmlestep1biblewithnotes-150512235651-lva1-app6891/85/Usmle-Step-1-Bible-205-320.jpg)




















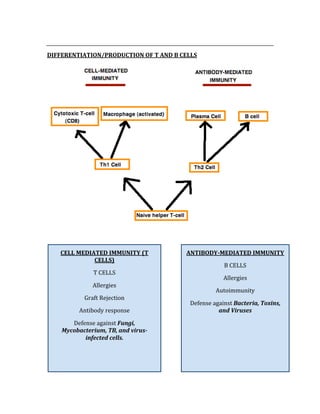








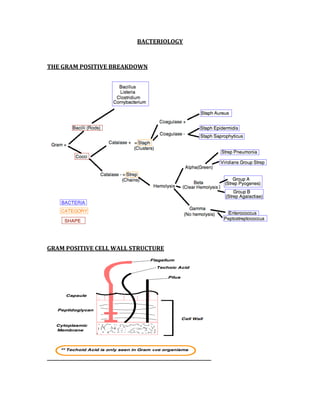
























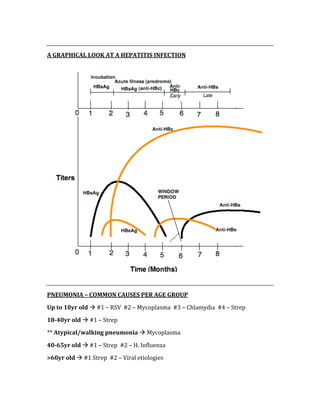



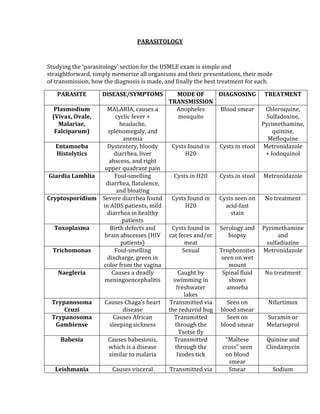




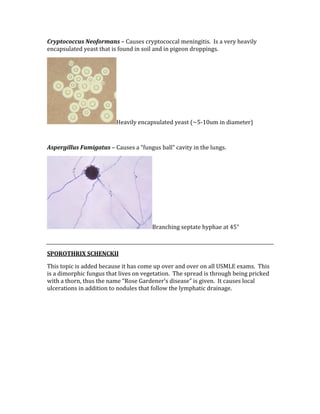

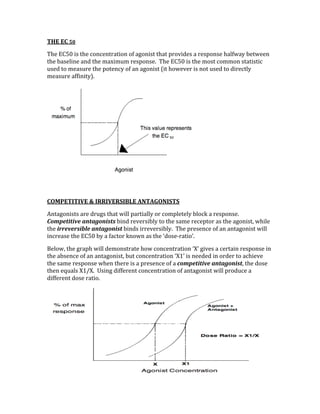
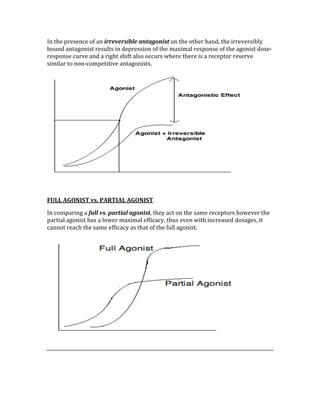
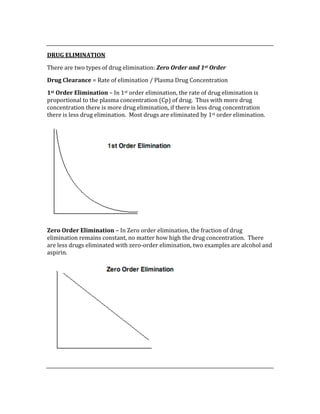


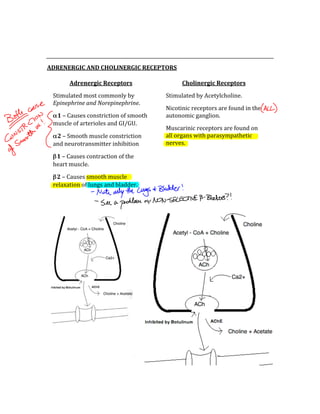
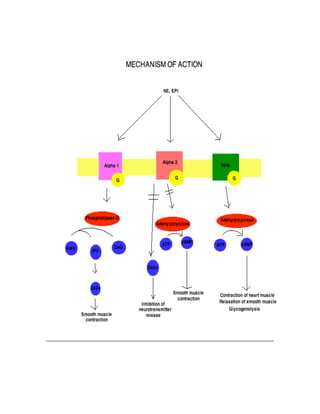










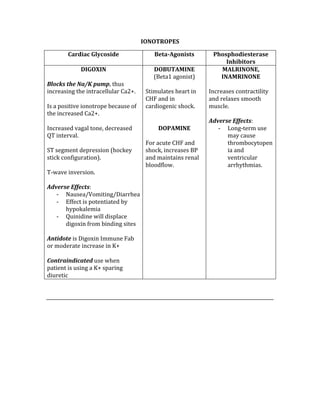



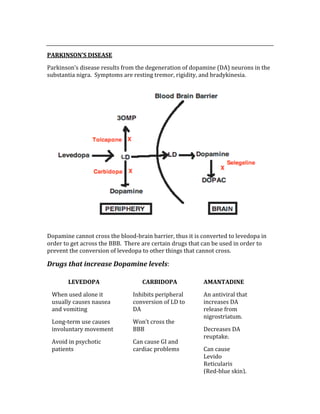



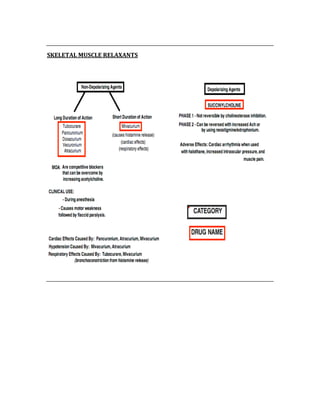





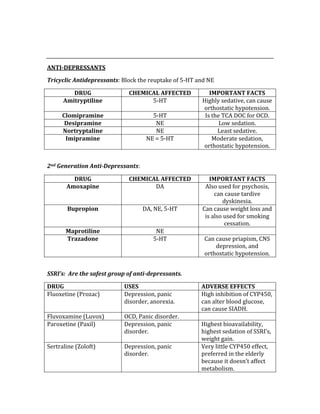














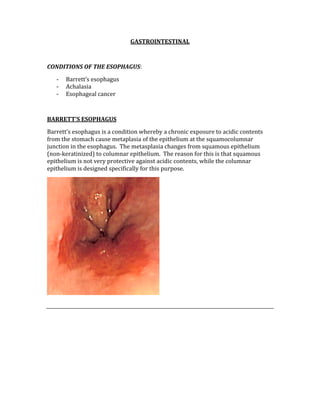


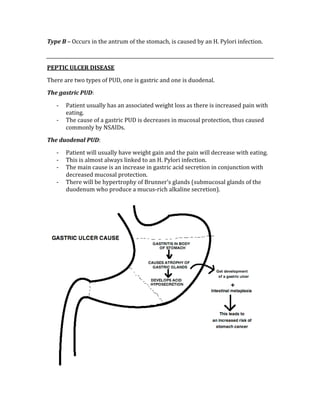
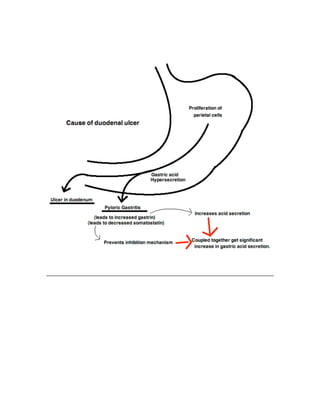




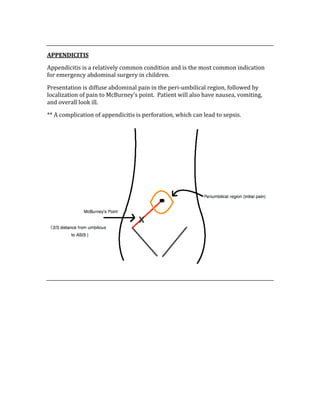






























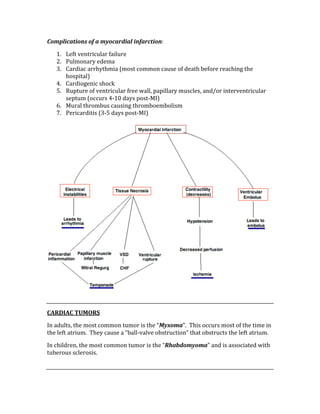




































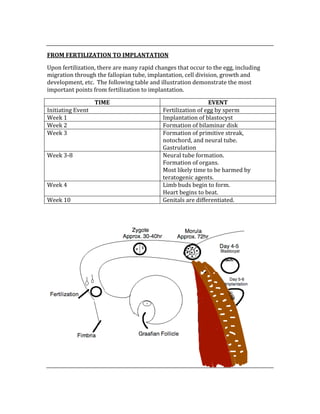
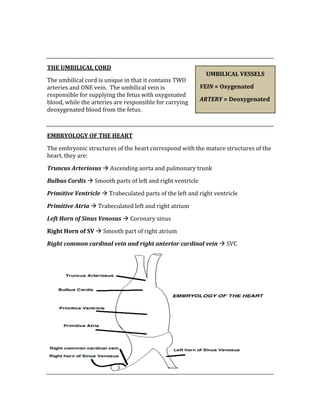
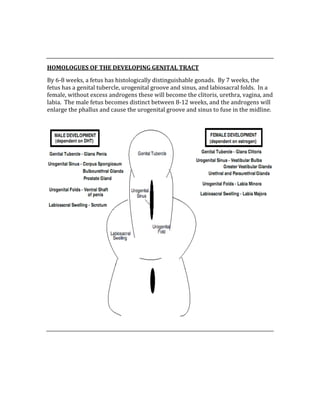
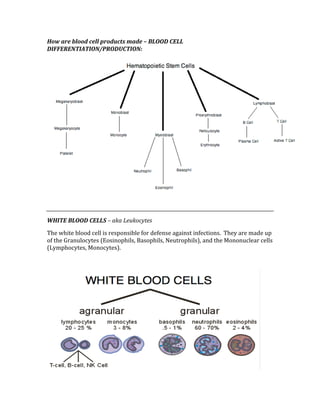
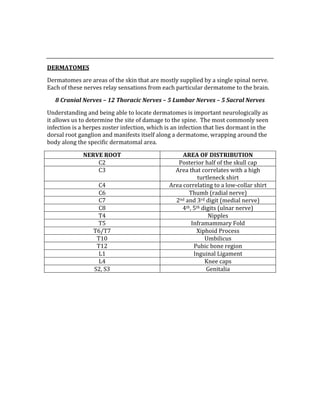
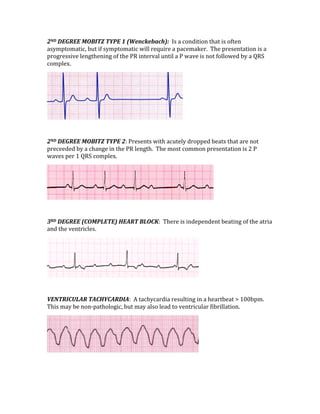
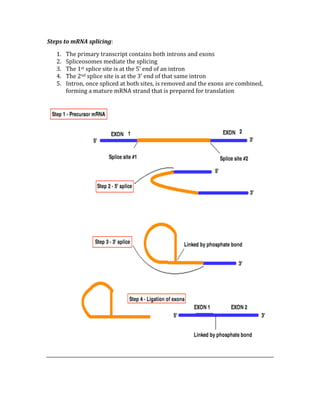
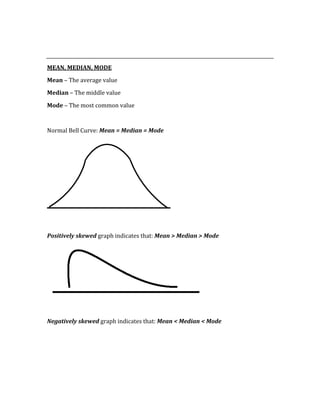
![ACID/BASE PHYSIOLOGY
Problem pH PCO2 [HCO3] Compensation Causes
Metabolic
Acidosis
⇓ ⇓ ⇓⇓ Patient will
hyperventilate
to blow off CO2
DKA, ASA
overdose,
lactic
acidosis
Respiratory
Acidosis
⇓ ⇑⇑ ⇑ Bicarb
absorption in
kidney
Obstruction
of airway
Respiratory
Alkalosis
⇑ ⇑⇑ ⇓ Kidney
secretes bicarb
Hypervent,
high alt.
Metabolic
Acidosis
⇑ ⇓ ⇑⇑ Pt will
hypoventilate
vomiting](https://image.slidesharecdn.com/usmlestep1biblewithnotes-150512235651-lva1-app6891/85/Usmle-Step-1-Bible-424-320.jpg)