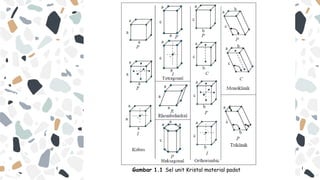
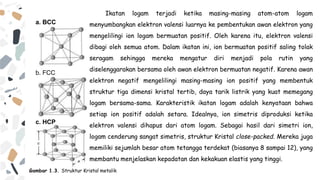
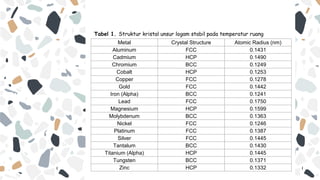
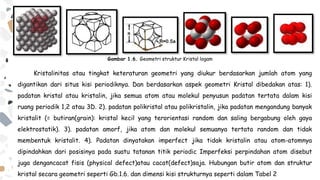
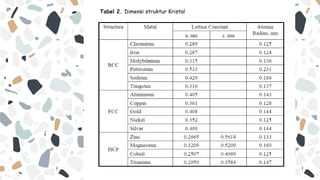
Dokumen ini membahas struktur kristal, termasuk pengertian, proses pembentukan, dan jenis-jenis ikatan dalam kristal. Kristal terbentuk dari atom atau molekul yang teratur dalam pola tiga dimensi, dan dapat dibedakan menjadi kristal tunggal atau polikristalin. Selain itu, dokumen menjelaskan sifat-sifat fizikal dan kimia dari berbagai jenis kristal serta perbedaan antara padatan kristal, polikristalin, dan amorf.