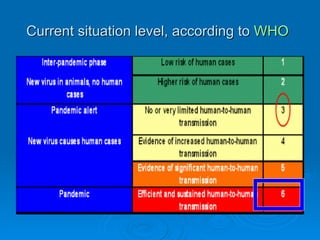
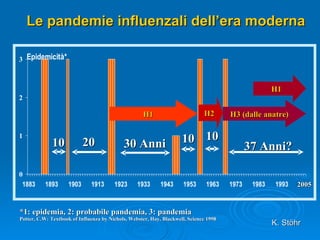
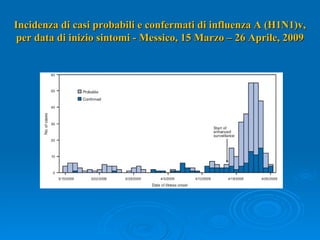
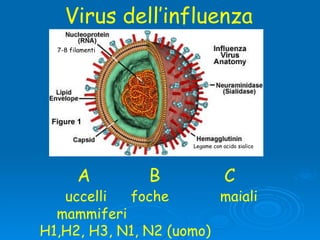
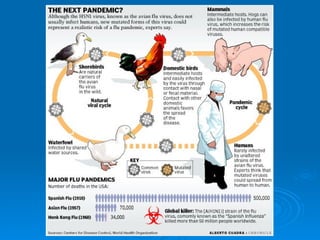
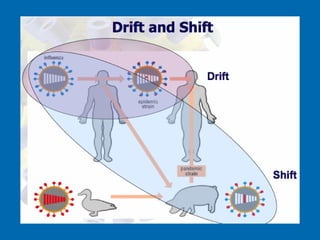
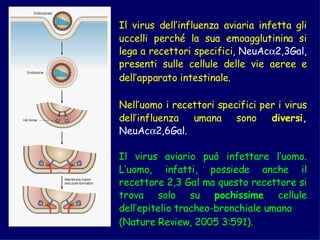
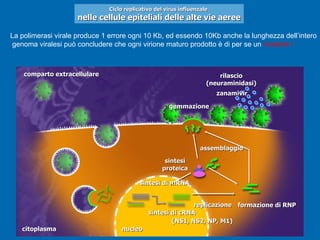
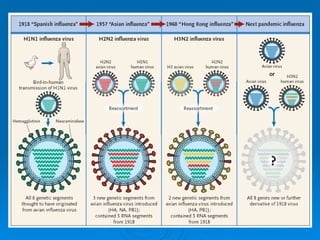
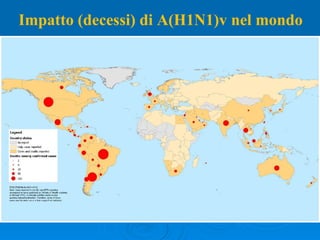
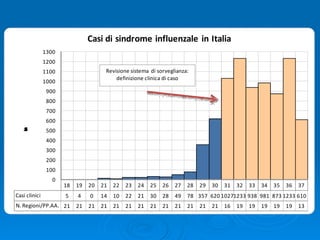
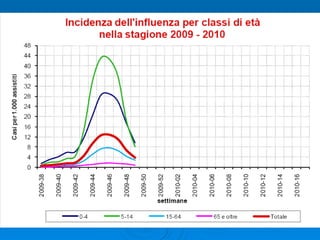
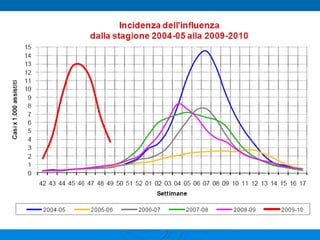
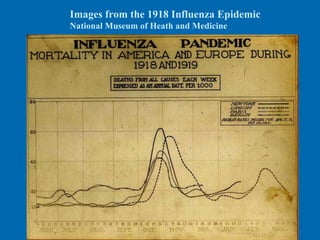
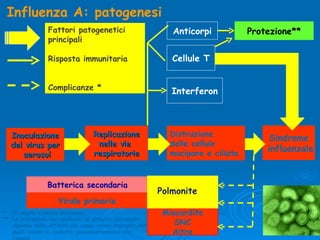
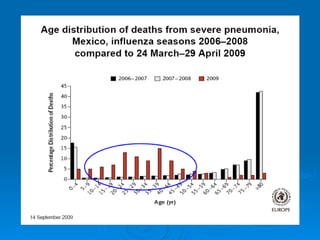
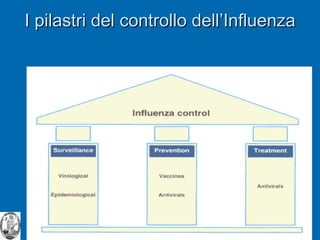
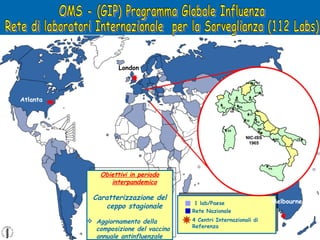
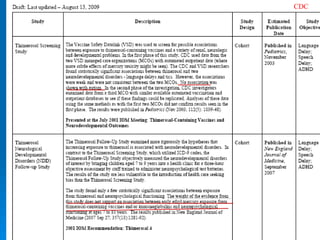
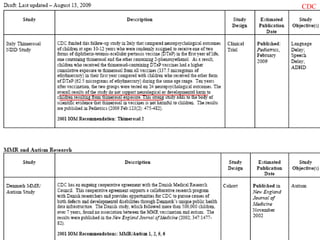
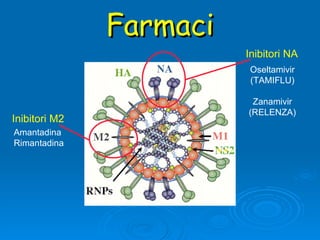
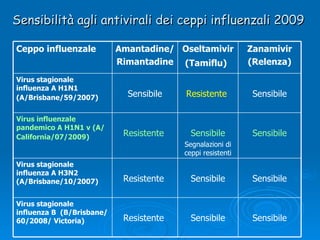
Il documento discute la pandemia di influenza A/H1N1, sottolineando la diffusione globale del virus e la sua bassa virulenza. Si evidenzia l'importanza della vaccinazione e dei farmaci antivirali nella mitigazione dell'impatto clinico. Inoltre, vengono esaminati i parametri epidemiologici e le dinamiche della trasmissione del virus, nonché i gruppi a rischio e le complicazioni associate.