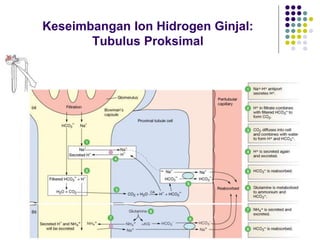
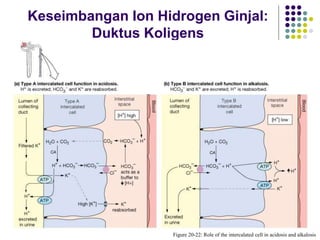
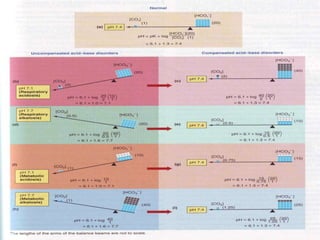
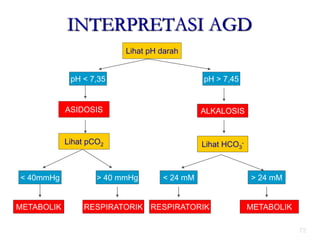
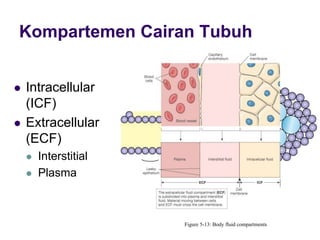
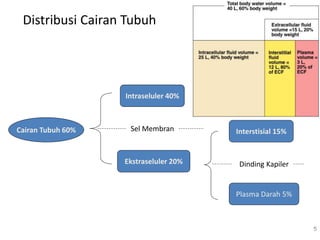
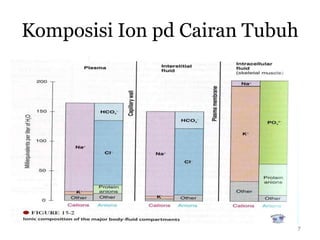
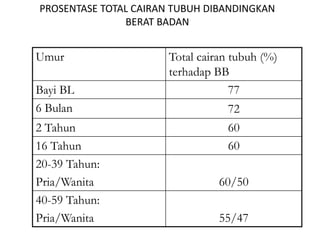
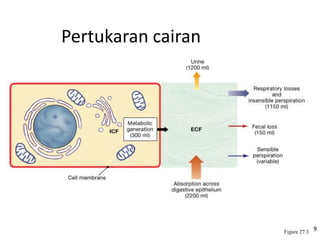
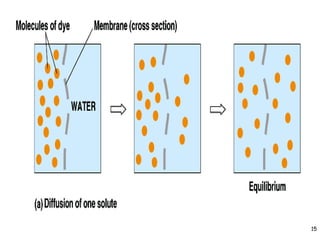
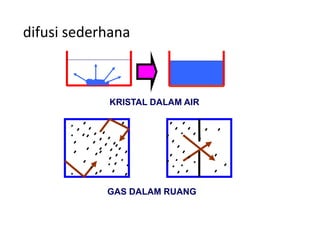
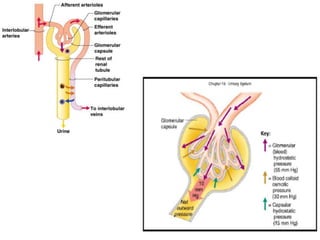
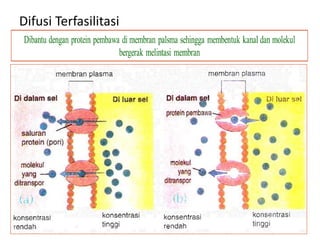
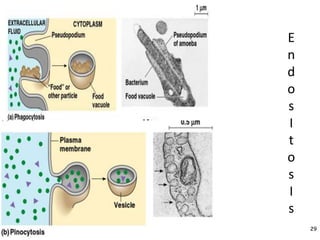
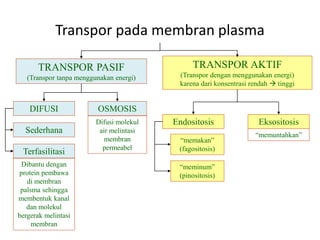
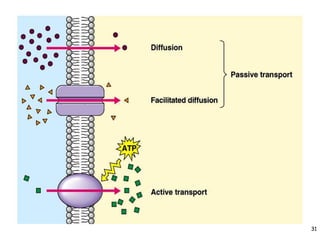
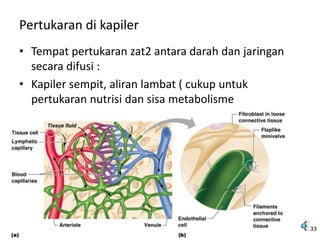
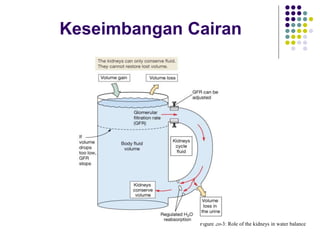
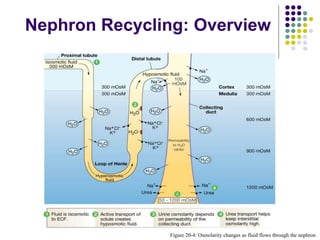
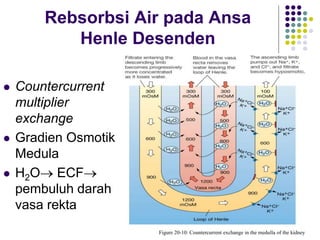
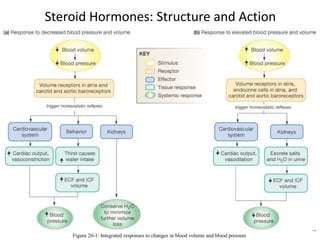
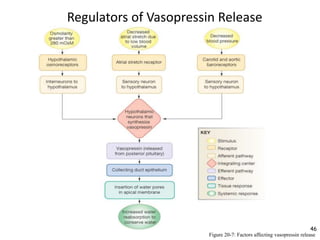
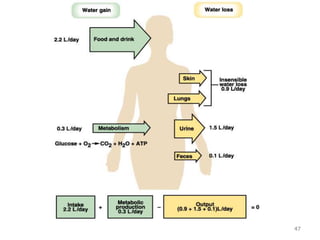
Mekanisme fisiologi tubuh manusia mempertahankan homeostasis melalui tiga mekanisme utama: pertukaran cairan antar kompartemen tubuh, pengaturan keseimbangan asam basa, dan pengendalian osmolaritas dan volume cairan ekstraseluler. Ginjal memainkan peran penting dalam mekanisme ini melalui filtrasi, reabsorpsi, dan ekskresi ion dan air.



























![ASIDITAS ( DERAJAT KEASAMAN = pH )
Derajat keasaman menyatakan seberapa kuat
atau lemahnya suatu asam didasarkan atas
nilai pH.
Keasaman atau kebasaan suatu larutan tergantung kepada
banyak/sedikitnya jumlah ion H+
Karena keberadaan ion H+ atau OH- sangat kecil dalam
larutan maka untuk perhitungan digunakan satuan pH
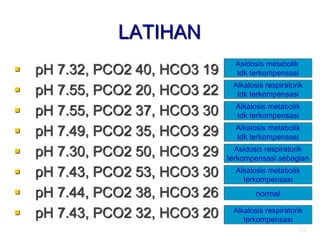
Secara matematis : pH = - log [ H+]
Larutan bersifat asam : [ H+] > [OH- ]
Larutan bersifat basa : [OH- ] < [ H+]
Larutan bersifat netral : [ H+] = [OH- ]](https://image.slidesharecdn.com/homeostasiscairanasbasa-220106064256/85/Homeostasis-cairan-asam-basa-55-320.jpg)
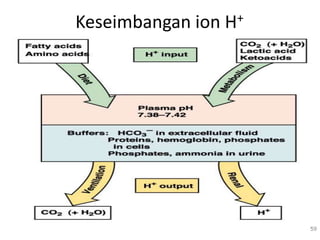
![Keseimbangan Asam & Basa
• Keseimbangan asam-basa pengaturan
konsentrasi ion H+ dalam cairan tubuh
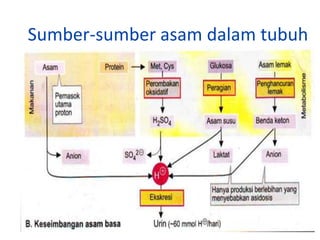
• Ion H+ sbg hasil dari metabolisme:
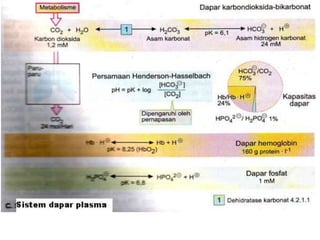
C6H12O6 + O2 CO2 + H2O H2CO3 H+ + HCO3
-
• [H+] dlm plasma pH plasma darah = 7,4
• Sistem dapar (buffer) menghambat perubahan
pH yang besar jika ada penambahan asam
atau basa
56](https://image.slidesharecdn.com/homeostasiscairanasbasa-220106064256/85/Homeostasis-cairan-asam-basa-56-320.jpg)