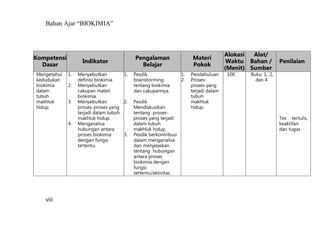
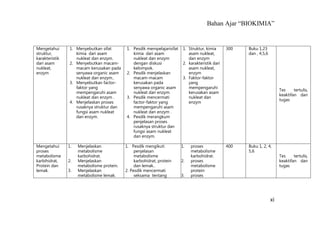
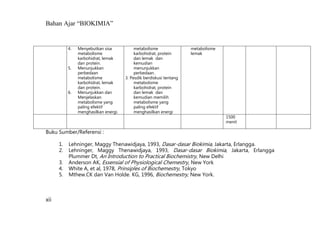
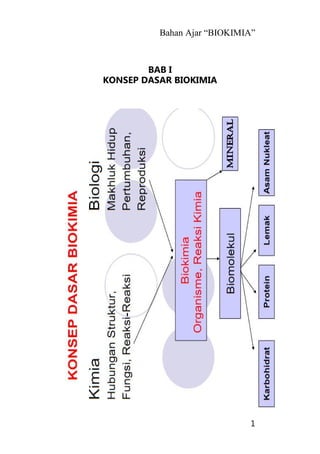
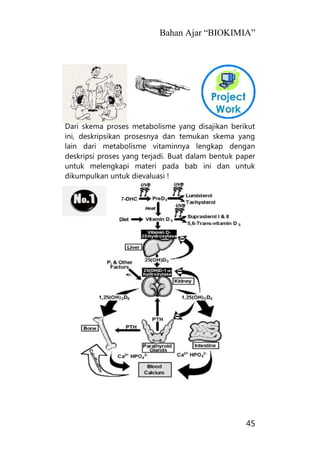
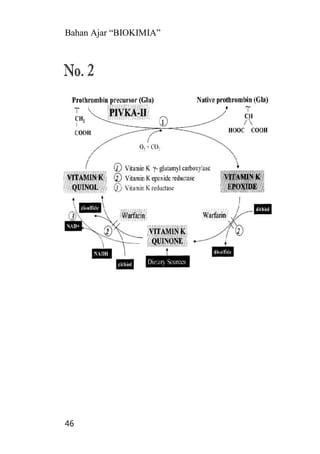
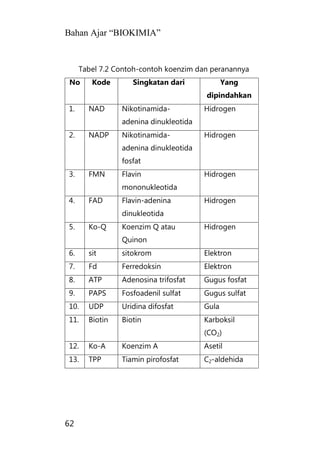
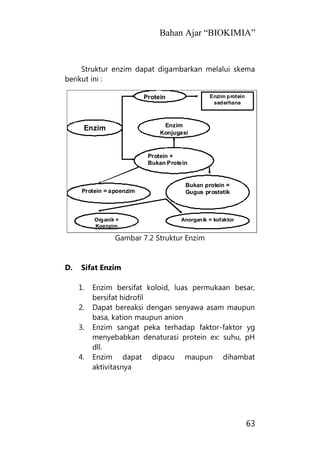
Bahan ajar ini membahas tentang karbohidrat sebagai sumber energi utama bagi manusia dan hewan yang dihasilkan melalui fotosintesis tanaman dari karbondioksida dan air dengan bantuan sinar matahari menjadi glukosa dan oksigen, kemudian glukosa dapat mengalami polimerisasi menjadi pati atau polisakarida nonpati."