алканууд
- 1. ОРГАНИК ХИМИ ЛЕКЦ 5
ХАНАСАН НҮҮРСУСТӨРӨГЧДИЙН ШИНЖ ЧАНАР, ГОМОЛОГИ ЭГНЭЭ
CnH2n+2 гэсэн ерөнхий томьёонд захирагдах зөвхөн нүүрстөрөгч ба устөрөгчөөс
тогтсон дан сигма холбоо агуулсан задгай хэлхээт энгийн органик нэгдлийг алкан гэнэ.
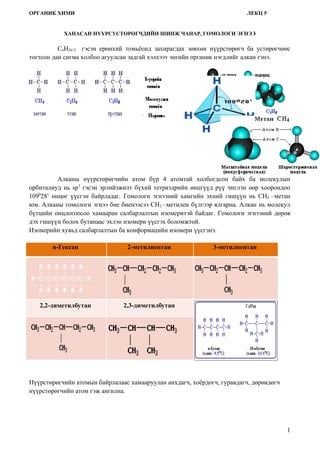
Алканы нүүрстөрөгчийн атом бүр 4 атомтай холбогдсон байх ба молекулын
орбиталиуд нь sp3 гэсэн эрлийзжилт бүхий тетраэдрийн өнцгүүд рүү чиглэн өөр хоорондоо
1090281 өнцөг үүсгэн байрладаг. Гомологи эгнээний хамгийн эхний гишүүн нь СН4 –метан
юм. Алканы гомологи эгнээ бие биенээсээ СН2 –метилен бүлгээр ялгарна. Алкан нь молекул
бүтцийн онцлогоосоо хамааран салбарлалтын изомеритэй байдаг. Гомологи эгнээний дөрөв
дэх гишүүн болох бутанаас эхлэн изомери үүсгэх боломжтой.
Изомерийн хувьд салбарлалтын ба конформацийн изомери үүсгэнэ.
н-Гексан 2-метилпентан 3-метилпентан
2,2-диметилбутан 2,3-диметилбутан
Нүүрстөрөгчийн атомын байрлалаас хамааруулан анхдагч, хоёрдогч, гуравдагч, дөрөвдөгч
нүүрстөрөгчийн атом гэж ангилна.
1
- 2. ОРГАНИК ХИМИ ЛЕКЦ 5
Алканы нэршлийн хувьд олон улсын нэршил болох IUPAC- аар нэрлэх боломжтой.
Алканы үндсэн эх сурвалж нь байгалийн хий С1-С4 болон газрын тос юм. Газрын
тосноос нүүрсустөрөгчдийн буцлах температурынх нь зөрүүгээр шат дараалан фракцлан
нэрэх замаар гарган авдаг.
1. Нефтийн крекингээр (салгах бутаргах) буюу энэ нь үйлдвэрийн арга юм.
C6H14 C2H6 + C4H8
2. Ханаагүй нүүрсустөрөгчдийн гидрогенжих урвалаар гарган авдаг.
3. Өндөр температур, даралт ба никель катализаторын орчинд хатуу түлшний
хийжүүлэлтээр
4. Хийн синтезээс алканы хольцыг гарган авдаг.
5. Энгийн нүүрсустөрөгчдийн галогент уламжлалыг металл натригаар үйлчлэхэд зөвхөн
тэгш тооны нүүрстөрөгчийн атом бүхий алкан үүсдэг. Үүнийг Вюрцийн урвал (1855)
гэдэг.
6. Карбон хүчлийн давсыг шүлтээр үйлчлэх Дюмагийн урвал
7. Нэг суурьт карбон хүчлийн электролизоор гарган авдаг. Энэ урвалыг анх 1894 онд
Кольбе нээсэн тул Кольбегийн урвал гэдэг.
2
- 3. ОРГАНИК ХИМИ ЛЕКЦ 5
8. Металлын карбидыг усаар үйлчлэн гарган авна.
9. Бертлогийн урвалаар 1868 онд алканы янз бүрийн уламжлалыг өндөр температурт
иодотустөрөгчийн хүчлээр ангижруулан гарган авдаг.
1. Алканы хувьд 4-өөс дээш нүүрстөрөгч агуулсан нэгдэл нь катализатор ба өндөр
температурын нөлөөгөөр изомержих урвалд ордог.
2. Алканы галогенжих (хлоржих) урвал.
гэх мэтээр
хлоржих урвал явагддаг. Мөн бромжих урвал нь:
3. Алканы нитрожих урвал. (Коноваловын урвал).
3
- 4. ОРГАНИК ХИМИ ЛЕКЦ 5
4. Алканы дегидрогенжих урвал. Алканыг никель катализаторын орчинд халаахад
дегидрогенжих урвалд ордог.
5. Мөн 15000С температурт метаныг дегидрогенжих урвалд оруулахад ацетилен
үүснэ. Энэ урвалыг ацетиленыг гарган авах үйлдвэрт өргөн ашигладаг.
6. Алканы исэлдэх урвал. Алканы молекул дах нүүрстөрөгчийн атомын
исэлдэлтийн зэргээс хамааран алканы исэлдэлтээр янз бүрийн нэгдэл үүсдэг.
+4 исэлдэхүйн хэм үзүүлдэг нүүрстөрөгч агуулсан алкан нь нүүрсхүчлийн хий ба ус
үүсгэн исэлддэг.
+2 исэлдэхүйн хэм үзүүлдэг нүүрстөрөгч агуулсан алкан нь угаарын хий ба ус үүсгэн
исэлддэг.
Мөн бутаны хагас исэлдүүлэлтээр карбон хүчлийг гарган авдаг.
4
- 5. ОРГАНИК ХИМИ ЛЕКЦ 5
Хийн синтез болох метан ба усны уурын харилцан үйлчлэлээр устөрөгч болон
нүүрстөрөгчийн дутуу ислийн хольц үүсдэг.
7. Алканы сульфо исэлдэх урвал.
Циклоалкан. Зөвхөн эрлийз төлөвт орших нүүрстөрөгчүүд битүү цагираг үүсгэн
холбогдсон бүтэцтэй нүүрстөрөгчдийг цагираг алкан буюу циклан гэнэ.
Жишээ нь 1,2 диметил ц-бутан
Изомерийн хувьд: Салбарлалтын
5
- 6. ОРГАНИК ХИМИ ЛЕКЦ 5
Халагч бүлгийн бүтцээс
Халагч бүлгийн байрлалын
Анги хоорондын
Орон зайн
Оптикийн
Гарган авах арга. Нефтийн боловсруулалтаар гарган авах С5 - С7 тэдгээрийг нафтенууд гэнэ.
1. Вюрцийн урвалаар: энэ урвалд катализатораар металл натрийн оронд нунтаг цайрыг
ашиглаж болно.
6
- 7. ОРГАНИК ХИМИ ЛЕКЦ 5
2. Бензол ба түүнийг гомологийн гишүүдийн гидрогенжих урвалаар:
Цикланууд нь хэвийн нөхцөлд: - циклопpопан ба циклобутан – хий, - циклоалканууд
С5 – С16 – шингэн, - С17, – дээш хатуу бодисууд байдаг. Буцлах температурын хувьд
алкануудтай харьцуулахад өндөр температурт буцалдаг ба энэ нь молекул хоорондын цагираг
бүтэцтэй холбоотой.
Хими шинж:
1. Бага цагирагт нэгдлүүд маш амархан гидрогенжих урвалд ордог.
2. Галогенжих ба гидрогалогенжих урвалд ордог.
Жишээ нь хлоржих урвал нь алканы халалцах урвалтай адил радикалийн механизмаар
явагддаг.
3. Дегидрогенжих урвал. Циклогексан ба түүний алкилын уламжлал нь энэ урвалд ордог.
7