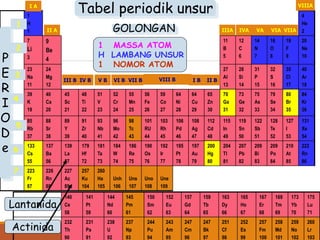
Dokumen ini membahas berbagai pengelompokan unsur kimia berdasarkan sifat dan struktur atom, mulai dari teori awal Antoine Lavoisier hingga sistem periodik modern yang diperkenalkan oleh Henry Moseley. Pengelompokan meliputi berbagai pendekatan, termasuk pengelompokan berdasarkan massa atom relatif dan kemiripan sifat. Tabel periodik unsur yang disusun modern berdasarkan nomor atom menghasilkan pemahaman yang lebih baik mengenai keteraturan unsur-unsur.