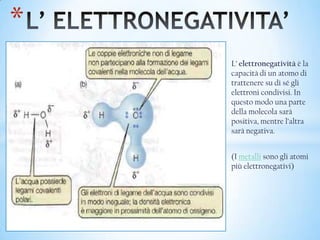
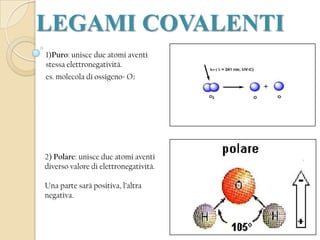
La chimica studia la materia e le sue trasformazioni, risalendo all'alchimia. Gli atomi, che formano la materia e sono classificati nella tavola periodica, si uniscono attraverso legami chimici per formare molecole. I legami chimici, influenzati dall'elettronegatività, comprendono covalenti, ionici, metallici e intermolecolari.