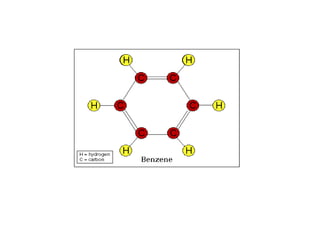
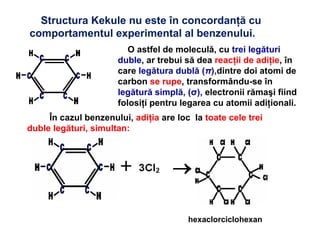
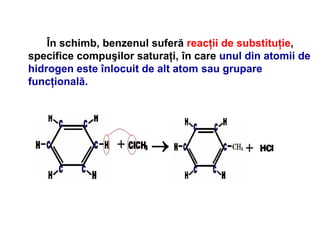
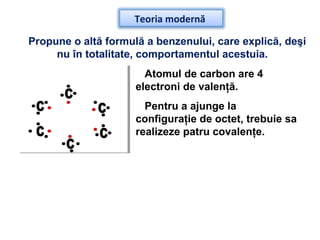
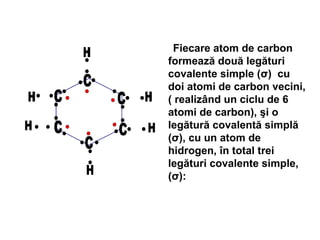
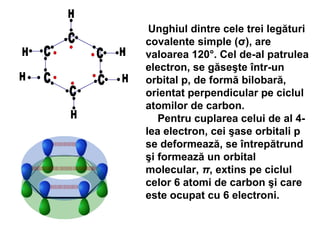
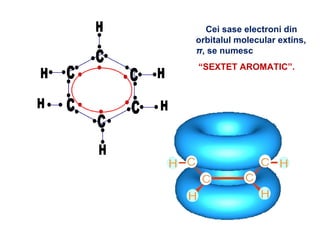
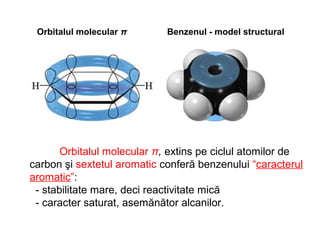
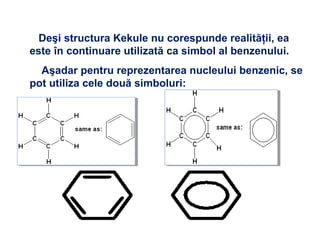
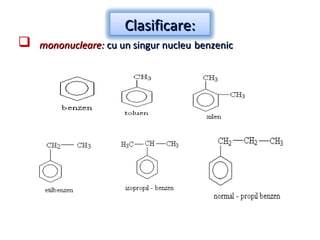
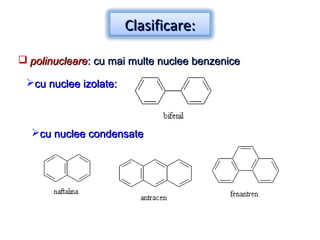
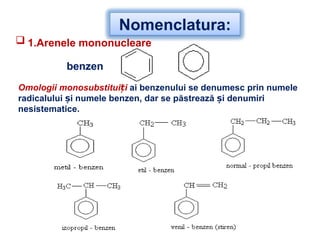
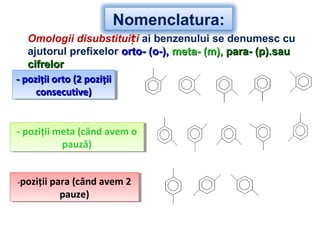
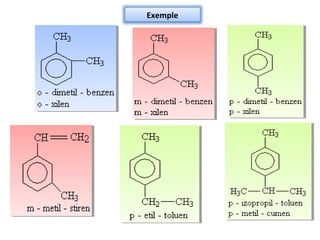
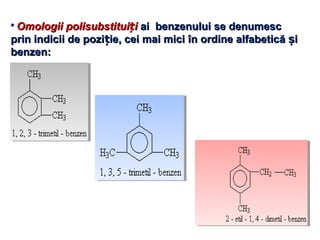
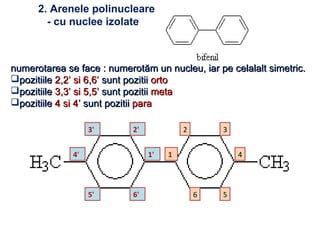
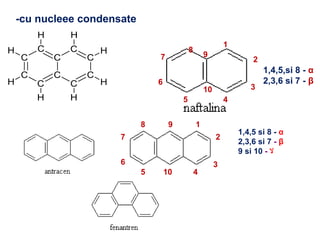
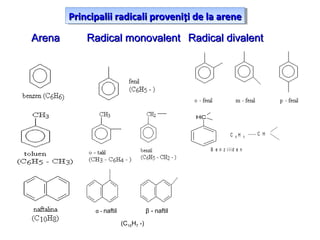
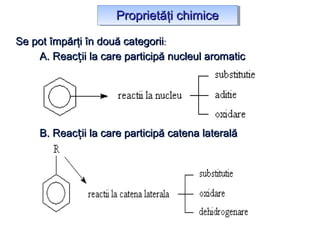
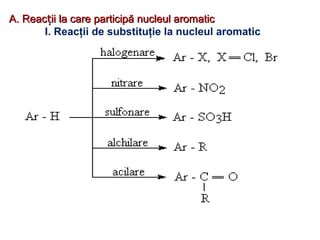
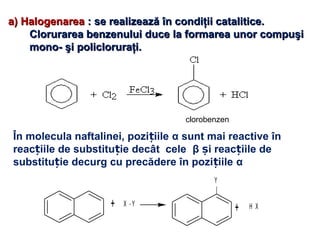
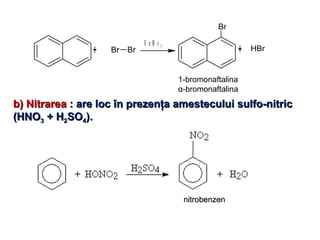
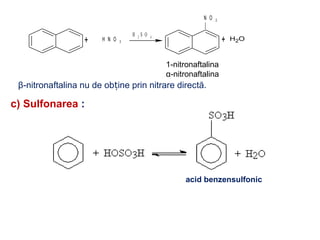
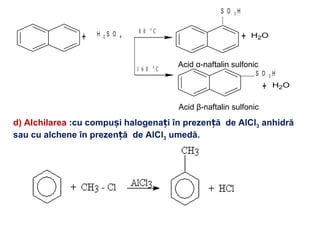
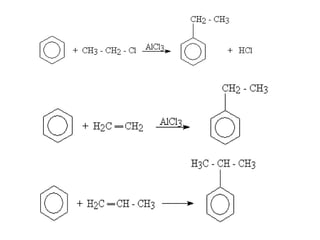
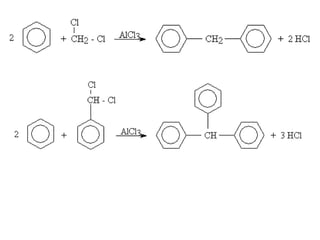
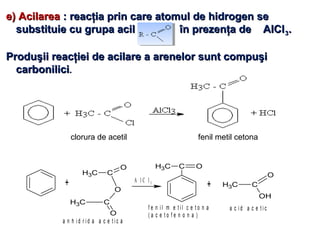
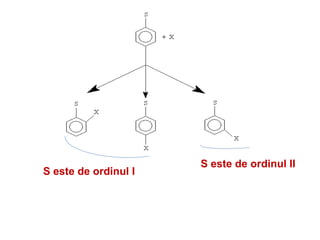
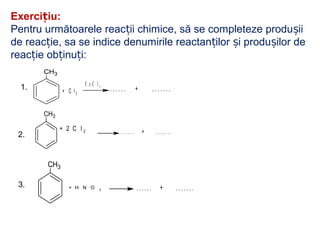
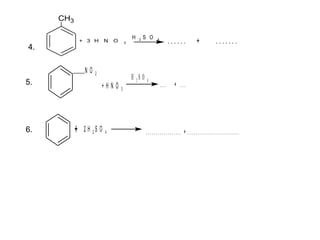
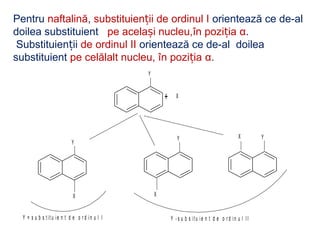
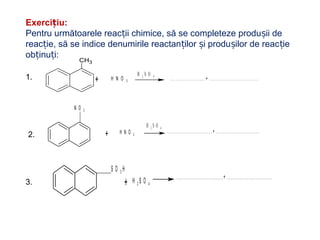
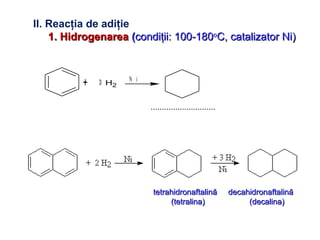
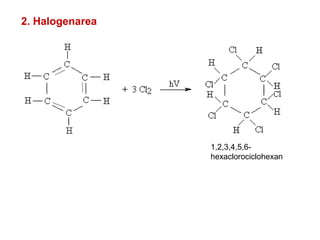
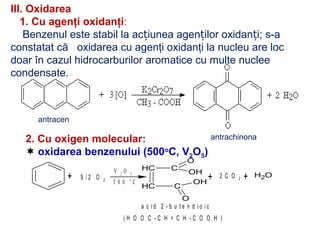
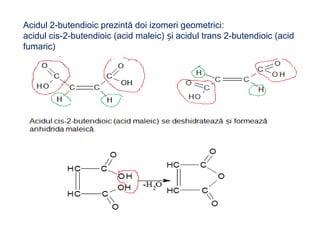
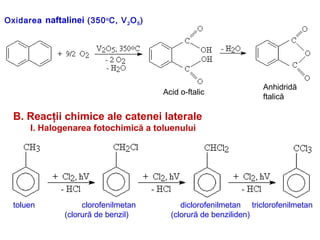
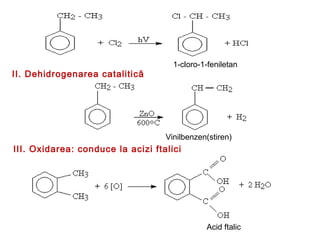
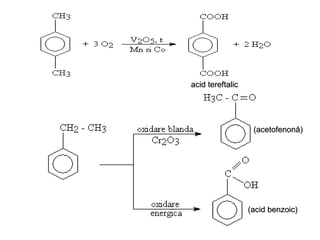
Arenele sunt hidrocarburi cu unul sau mai multe nuclee benzenice, iar benzenul este cel mai simplu reprezentant. Structura benzenului a fost propusă de Kekulé și se caracterizează printr-o stabilitate mare și reacții de substituție. Arenele pot fi clasificate în mononucleare și polinucleare și au proprietăți chimice distincte, incluzând reacții de substituție și adiție.