Report
Share
Recommended
More Related Content
What's hot
What's hot (20)
ΣΗΜΕΙΩΣΕΙΣ ΡΕΥΣΤΟΜΗΧΑΝΙΚΗΣ Ι. - ΘΟΔΩΡΗΣ ΠΑΠΑΣΓΟΥΡΙΔΗΣ

ΣΗΜΕΙΩΣΕΙΣ ΡΕΥΣΤΟΜΗΧΑΝΙΚΗΣ Ι. - ΘΟΔΩΡΗΣ ΠΑΠΑΣΓΟΥΡΙΔΗΣ
Πανελλήνιος Διαγωνισμός Φυσικής 2016 - Γ' Λυκείου (ΛΥΣΕΙΣ)

Πανελλήνιος Διαγωνισμός Φυσικής 2016 - Γ' Λυκείου (ΛΥΣΕΙΣ)
Πανελλήνιος Διαγωνισμός Φυσικής 2016 - Β' Λυκείου (ΘΕΜΑΤΑ)

Πανελλήνιος Διαγωνισμός Φυσικής 2016 - Β' Λυκείου (ΘΕΜΑΤΑ)
ΦΥΛΛΑΔΙΟ ΑΕΡΙΩΝ-ΘΕΡΜΟΔΥΝΑΜΙΚΗΣ "ΣΑΝ ΔΙΑΓΩΝΙΣΜΑ Β΄ΛΥΚΕΙΟΥ ΚΑΤΕΥΘΥΝΣΗ"

ΦΥΛΛΑΔΙΟ ΑΕΡΙΩΝ-ΘΕΡΜΟΔΥΝΑΜΙΚΗΣ "ΣΑΝ ΔΙΑΓΩΝΙΣΜΑ Β΄ΛΥΚΕΙΟΥ ΚΑΤΕΥΘΥΝΣΗ"
Πανελλήνιος Διαγωνισμός Φυσικής 2016 - Α' Γυμνασίου (ΛΥΣΕΙΣ)

Πανελλήνιος Διαγωνισμός Φυσικής 2016 - Α' Γυμνασίου (ΛΥΣΕΙΣ)
ΠΙΕΣΗ-ΥΔΡΟΣΤΑΤΙΚΗ ΠΙΕΣΗ-ΑΤΜΟΣΦΑΙΡΙΚΗ ΠΙΕΣΗ-ΑΡΧΗ ΤΟΥ ΠΑΣΚΑΛ (ppt)

ΠΙΕΣΗ-ΥΔΡΟΣΤΑΤΙΚΗ ΠΙΕΣΗ-ΑΤΜΟΣΦΑΙΡΙΚΗ ΠΙΕΣΗ-ΑΡΧΗ ΤΟΥ ΠΑΣΚΑΛ (ppt)
Πανελλήνιος Διαγωνισμός Φυσικής 2016 - Γ' Γυμνασίου (ΘΕΜΑΤΑ)

Πανελλήνιος Διαγωνισμός Φυσικής 2016 - Γ' Γυμνασίου (ΘΕΜΑΤΑ)
Πανελλήνιος Διαγωνισμός Φυσικής 2016 - Β' Γυμνασίου (ΘΕΜΑΤΑ)

Πανελλήνιος Διαγωνισμός Φυσικής 2016 - Β' Γυμνασίου (ΘΕΜΑΤΑ)
Πανελλήνιος Διαγωνισμός Φυσικής 2016 - Β' Γυμνασίου (ΛΥΣΕΙΣ)

Πανελλήνιος Διαγωνισμός Φυσικής 2016 - Β' Γυμνασίου (ΛΥΣΕΙΣ)
ΣΗΜΕΙΩΣΕΙΣ ΡΕΥΣΤΟΜΗΧΑΝΙΚΗΣ ΙΙ. - ΘΟΔΩΡΗΣ ΠΑΠΑΣΓΟΥΡΙΔΗΣ

ΣΗΜΕΙΩΣΕΙΣ ΡΕΥΣΤΟΜΗΧΑΝΙΚΗΣ ΙΙ. - ΘΟΔΩΡΗΣ ΠΑΠΑΣΓΟΥΡΙΔΗΣ
Recently uploaded
Recently uploaded (20)
ΙΣΤΟΡΙΑ Γ ΄ΓΥΜΝΑΣΙΟΥ : ΕΠΑΝΑΛΗΠΤΙΚΕΣ ΑΣΚΗΣΕΙΣ ΜΕΡΟΣ 1ο 

ΙΣΤΟΡΙΑ Γ ΄ΓΥΜΝΑΣΙΟΥ : ΕΠΑΝΑΛΗΠΤΙΚΕΣ ΑΣΚΗΣΕΙΣ ΜΕΡΟΣ 1ο
ΙΣΤΟΡΙΑ Γ΄ΓΥΜΝΑΣΙΟΥ: ΕΠΑΝΑΛΗΠΤΙΚΕΣ ΑΣΚΗΣΕΙΣ ΜΕΡΟΣ 2ο

ΙΣΤΟΡΙΑ Γ΄ΓΥΜΝΑΣΙΟΥ: ΕΠΑΝΑΛΗΠΤΙΚΕΣ ΑΣΚΗΣΕΙΣ ΜΕΡΟΣ 2ο
Η ΒΙΟΜΗΧΑΝΙΚΗ ΕΠΑΝΑΣΤΑΣΗ,ΜΠΟΗΣ ΧΡΗΣΤΟΣ - ΜΑΓΟΥΛΑΣ ΘΩΜΑΣ

Η ΒΙΟΜΗΧΑΝΙΚΗ ΕΠΑΝΑΣΤΑΣΗ,ΜΠΟΗΣ ΧΡΗΣΤΟΣ - ΜΑΓΟΥΛΑΣ ΘΩΜΑΣ
ΒΥΖΑΝΤΙΝΗ ΚΟΥΖΙΝΑ ΚΑΙ ΜΟΔΑ, ΕΛΕΑΝΑ ΣΤΑΥΡΟΠΟΥΛΟΥ.pptx

ΒΥΖΑΝΤΙΝΗ ΚΟΥΖΙΝΑ ΚΑΙ ΜΟΔΑ, ΕΛΕΑΝΑ ΣΤΑΥΡΟΠΟΥΛΟΥ.pptx
Inclusion - Εργασία για τη συμπερίληψη 2ο Γυμνάσιο Αλεξανδρούπολης

Inclusion - Εργασία για τη συμπερίληψη 2ο Γυμνάσιο Αλεξανδρούπολης
Βενετία, μια πόλη πάνω στο νερό, Βασιλική Μπράβου - Αποστολία Μπάρδα

Βενετία, μια πόλη πάνω στο νερό, Βασιλική Μπράβου - Αποστολία Μπάρδα
ΧΑΝΟΣ ΚΡΟΥΜΟΣ-ΒΑΣΙΛΙΑΣ ΝΙΚΗΦΟΡΟΣ,ΚΡΙΣΤΙΝΑ ΚΡΑΣΤΕΒΑ

ΧΑΝΟΣ ΚΡΟΥΜΟΣ-ΒΑΣΙΛΙΑΣ ΝΙΚΗΦΟΡΟΣ,ΚΡΙΣΤΙΝΑ ΚΡΑΣΤΕΒΑ
ΘΕΣΣΑΛΟΝΙΚΗ Η ΔΕΥΤΕΡΗ ΠΟΛΗ ΤΗΣ ΒΥΖΑΝΤΙΝΗΣ ΑΥΤΟΚΡΑΤΟΡΙΑΣ, ΔΑΝΑΗ ΠΑΝΟΥ

ΘΕΣΣΑΛΟΝΙΚΗ Η ΔΕΥΤΕΡΗ ΠΟΛΗ ΤΗΣ ΒΥΖΑΝΤΙΝΗΣ ΑΥΤΟΚΡΑΤΟΡΙΑΣ, ΔΑΝΑΗ ΠΑΝΟΥ
Safe Driving - Εργασία για την ασφαλή οδήγηση 2ο Γυμνάσιο Αλεξανδρούπολης

Safe Driving - Εργασία για την ασφαλή οδήγηση 2ο Γυμνάσιο Αλεξανδρούπολης
Η ΑΔΙΚΕΙΑ ΤΟΥ ΔΙΑΓΩΝΙΣΜΟΥ ΑΣΕΠ 2008 ΓΙΑ ΕΚΠΑΙΔΕΥΤΙΚΟΥΣ

Η ΑΔΙΚΕΙΑ ΤΟΥ ΔΙΑΓΩΝΙΣΜΟΥ ΑΣΕΠ 2008 ΓΙΑ ΕΚΠΑΙΔΕΥΤΙΚΟΥΣ
ΕΜΕΙΣ ΕΔΩ ΠΑΙΖΟΥΜΕ ΜΠΑΛΑ, εργασία για την οπαδική βία

ΕΜΕΙΣ ΕΔΩ ΠΑΙΖΟΥΜΕ ΜΠΑΛΑ, εργασία για την οπαδική βία
Κινητική Θεωρία των Αερίων
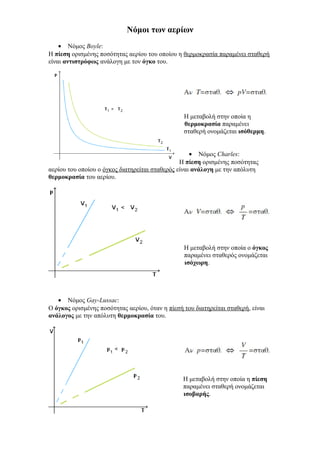
- 1. Νόμοι των αερίων • Νόμος Boyle: Η πίεση ορισμένης ποσότητας αερίου του οποίου η θερμοκρασία παραμένει σταθερή είναι αντιστρόφως ανάλογη με τον όγκο του. Η μεταβολή στην οποία η θ ε ρ μ θερμοκρασία παραμένει σ τα α θ σταθερή ονομάζεται ισόθερμη. • Νόμος Charles: Η πίεση ορισμένης ποσότητας αερίου του οποίου ο όγκος διατηρείται σταθερός είναι ανάλογη με την απόλυτη θερμοκρασία του αερίου. π ι Η μεταβολή στην οποία ο όγκος παραμένει σταθερός ονομάζεται ισόχωρη. • Νόμος Gay-Lussac: Ο όγκος ορισμένης ποσότητας αερίου, όταν η πίεσή του διατηρείται σταθερή, είναι ανάλογος με την απόλυτη θερμοκρασία του. π σ Η μεταβολή στην οποία η πίεση παραμένει σταθερή ονομάζεται ι ισοβαρής.
- 2. Οι παραπάνω νόμοι ισχύουν με μεγαλύτερη ακρίβεια για ένα μονοατομικό, θερμό και αραιό αέριο, παρά για ένα πολυατομικό ψυχρό και πυκνό. Μακροσκοπικά ιδανικό αέριο, είναι αυτό που υπακούει στους τρεις νόμους των αερίων σε οποιεσδήποτε συνθήκες και αν βρίσκεται. Κινητική Θεωρία Σύμφωνα με την κινητική θεωρία: 1. Τα αέρια αποτελούνται από πολύ μεγάλο πλήθος απειροελάχιστων σφαιριδίων που κινούνται τυχαία. Τα σφαιρίδια ονομάζονται μόρια του αερίου. 2. Τα μόρια του αερίου συμπεριφέρονται σαν μικροσκοπικές, απόλυτα ελαστικές, σφαίρες. Ο όγκος τους θεωρείται αμελητέος, σε σχέση με τον αυτόν του δοχείου. 3. Στα μόρια δεν ασκούνται δυνάμεις, παρά μόνο τη στιγμή της κρούσης με άλλα μόρια ή με τα τοιχώματα του δοχείου. Στο μεσοδιάστημα, η κίνηση είναι Ε.Ο.Κ. 4. Οι κρούσεις των μορίων με τα τοιχώματα είναι ελαστικές. Η κινητική ενέργεια δεν μεταβάλλεται κατά την κρούση. Τυπολόγιο p=πίεση V=όγκος T=απόλυτη θερμοκρασία m=μάζα n=mols Mr=μοριακή μάζα ρ=πυκνότητα N=αριθμός μορίων uμ2 =μέση τιμή των τετραγώνων της ταχύτητας uεν =ενεργός ταχύτητα R=σταθερά=8,314 (S.I)=0,082 (καταστατική) k=σταθερά=1,381*10-23