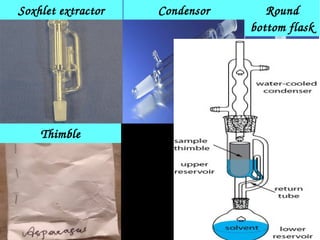
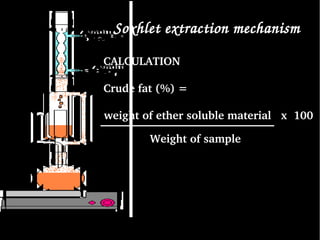
This document discusses nutraceuticals and proximate analysis. It defines nutraceuticals as foods or food components that provide health or medical benefits, including nutrients like dietary fiber, probiotics, antioxidants, and spices. The document then describes various methods for proximate analysis, including determining the moisture, ash, fat, protein, carbohydrate, and crude fiber content. These standard methods involve processes like distillation to measure moisture, ignition in a furnace to measure ash, Soxhlet extraction for fat, and the Kjeldahl method for determining protein content.




















![DETERMINATION OF CARBOHYDRATE
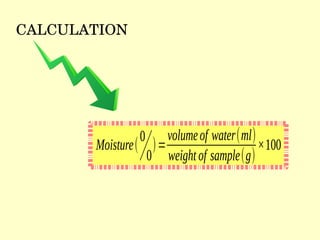
% of carbohydrate = 100 [ Moisture + Ash + Fat
+ Protein ]](https://image.slidesharecdn.com/linkedin-181230181055/85/Nutraceuticals-and-Proximate-Analysis-in-Brief-27-320.jpg)




