MATA KULIAH KIMIA ORGANIK 1 (ALKANA).pptx
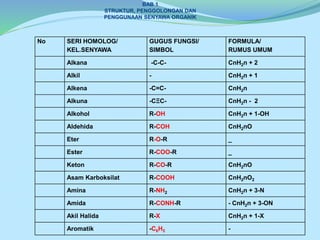
- 1. BAB 1 STRUKTUR, PENGGOLONGAN DAN PENGGUNAAN SENYAWA ORGANIK No SERI HOMOLOG/ KEL.SENYAWA GUGUS FUNGSI/ SIMBOL FORMULA/ RUMUS UMUM Alkana -C-C- CnH2n + 2 Alkil - CnH2n + 1 Alkena -C=C- CnH2n Alkuna -CΞC- CnH2n - 2 Alkohol R-OH CnH2n + 1-OH Aldehida R-COH CnH2nO Eter R-O-R _ Ester R-COO-R _ Keton R-CO-R CnH2nO Asam Karboksilat R-COOH CnH2nO2 Amina R-NH2 CnH2n + 3-N Amida R-CONH-R - CnH2n + 3-ON Akil Halida R-X CnH2n + 1-X Aromatik -C6H5 -
- 3. Keterangan : n = jumlah atom C X= unsur halogen R = H = Alkil = Aril = Kombinasi alkyl dan aril Rumus umum hanya berlaku untuk senyawa alifatik, tidak berlaku untk senyawa siklik. Contoh –contoh senyawa sebagai berikut
- 4. KELOMPOK SENYAWA STRUKTUR SENYAWA CONTOH ALIFATIK NAMA SENYAWA SIKLIK NAMA SENYAWA ALKANA Pentana Metilsikloheksana ALKENA (E)-3-metil pentena-2 etilsiklopentena ALKUNA (E)-3-metil penta-3- ena-1-una Siklopentuna H3C H2 C C H2 H2 C CH3 CH3 H3C H2 C C H C CH3 CH3 CH2-CH3 HC C C H C CH3 CH3
- 5. KELOMPOK SENYAWA STRUKTUR SENYAWA CONTOH ALIFATIK NAMA SENYAWA SIKLIK NAMA SENYAWA ALKIL HALIDA 2-klorobutana Bromo siklohekasana ALKOHOL Propanol fenol ALDEHIDA Butanaldehida Benzaldehida Br H3C H C C H2 CH3 Cl CH3-CH2-CH2-OH OH CH3-CH2-CH2-C O H C O H
- 6. KELOMPOK SENYAWA STRUKTUR SENYAWA CONTOH ALIFATIK NAMA SENYAWA SIKLIK NAMA SENYAWA ETER Dietileter/gas epiji etilsikloheksileter ESTER Etilmetilester /etilasetat Metilsikloheksil ester KETON Aseton 1-siklopentiletanon H3C H2 C O H2 C CH3 H3C C O H2 C CH3 O H3C C CH3 O O CH2-CH3 O C-CH3 O C O CH3
- 7. KELOMPOK SENYAWA STRUKTUR SENYAWA CONTOH ALIFATIK NAMA SENYAWA SIKLIK NAMA SENYAWA ASAM KARBOKSILAT Asam butirat Sikloheksilkarboks ilat AMINA Propilamina Sikloheksilamina AMIDA N-metil propionamida N-metil siklopentilnamida AROMATIK Fenasetin (obt trn panas) H3C H2 C C H2 C O OH H3C H2 C C H2 NH2 H3C H2 C C H N CH3 O C O OH NH2 C O H N CH3 OC2H5 HN C CH3 O
- 8. BAB 2 ALKANA 2.1. KONSEP DASAR ALKANA Alakna merupakan hidrokarbon alifatik maupaun siklik (siklo alkana). Rumus Umum alkana: CnH2n + 2, hanya berlaku untuk alifatik. Sumber utama alkana antara lain minyak bumi dan gas alam. Misalnya gas Metana- CH4, etana- C2H6, propana- C3H8 dan butana C4H10 Minyak bumi mengandung senyawa alkana berupa gas dengan berat molekul atau massa molekul relatif (Mr) rendah dan alkana padat dengan berat molekul/Mr tinggi. Alkana disebut juga Hidrokarbon parifin
- 9. 2.2. SIFAT FISIKA ALKANA Beberapa sifat fisika alkana antara lain : 1. Alkana yang mengandung 1-4 atom C berwujud gas, 5-17 atom C berwujud cair dan lebih besar dari 17 ke atas berwujud padat. 2. Titik didih alkana bertambah tinggi dengan bertambahnya jumlah atom C, terutama pada senyawa alkana normal. Pada homolog alkana dengan jumlah atom C-banyak, perbedaan titik ididih realtif kecil. 3. Titik lebur, densitas, viskositas alkana meningkat jika jumlah atom C bertambah banyak, terutama pada alkana rantai lurus. Titik didih/lebur menurun dengan bertambah banyak jumlah cabang pada senyawa alkana.
- 10. Alkana mudah larut dalam etanol/alkohol lainnya dan eter. Kelarutan alkana tersebut menurun jika jumlah atom C atau Mr- bertambah banyak. Alkana sukar larut dalam air. 2.3. SIFAT KIMIA ALKANA Pada umumnya alkana dapat berekasi dengan cara sbb 2.3.1. HALOGENASI ALKANA Halogenasi artinya mengganti/mensubstitusi 1 atau lebih atom H dengan atom halogen, terutama Cl, Br, dan I. Untuk F dibutuhkan kondisi khusus karena sangat eksplosif/mudah bereaksi, At Jarang dipakai dalam reaksi senyawa organik. Klorinasi dan brominasi pada alkana dibantu dengan suhu, cahaya matahari, katalis antara lain AlCl3, AlBr3, FeCl3, FeBr3. Iodinasi alkana dibantu dengan oksidator HIO3
- 11. 2.3.1.1. REAKSI KLORINASI-Cl2 ALKANA Klorinasi pada alkana dapat terjadi menggunakan cahaya matahari, panas dan katalis, antara lain AlCl3, FeCl3. Tingkat klorinasi sangat tergantung pada jumlah klor yang dingunakan. Adanya desakan/dorongan gaya Coloumb dari atom atau gugus, oleh karena beda inti atom menyebabkan laju protonasi H atau putusnya atom H pada alkana berbeda-beda sehingga substitusi antar atom H- primer, H-sekunder, H-tersier dst berbeda-beda. Dengan demikian maka hasil reaksi klorinasi alkana jumlahnya berbeda-beda. Markovnikov (1875), menemukan bahwa urutan Substitusi atom H adalah H-tersier > H-sekunder, > H-primer.
- 12. Contoh. Klorinasi pada 2,3,3-trimetil pentana dengan pemanasan pada suhu 425 OC. Mdkanisme reaksi kimianya sbb
- 13. Contoh lain klorinasi 2,3,3-trimetl butana dengan katalis AlCl3 Mekanisme reaksi kimianya sbb.
- 14. 2.3.1.2. REAKSI BROMINASI-Br2 ALKANA Brominasi pada senyawa alkana dapat terjadi seperti pada klorinasi alkana. Brominasi pada senyawa alkana berlangsung lebih lambat dari pada klorinasi, karena Massa molekul relatif-Mr - Br lebih besar sehingga proses substitusi H tersier, H-sekunder dan H-primer oleh Br lambat dibandingkan dengan substitusi atom Cl+ pada H tersier, H-sekunder dan H-primer. .
- 15. Reaksi brominasi pada alkana menggunakan cahaya matahari, panas dan katalis, antara lain AlBr3, FeBr3 Contoh brominasi isobutil dengan katalis FeBr3 Mekanisme reaksi kimianya sbb
- 16. 2.3.1.3. REAKSI IODINASI-I2 ALKANA Iodinasi alkana merupakan reaksi dapat balik/kesetimbangan atau reversible Contoh iodinasi propana Agar tidak terjadi reaksi kesetimbangan, diperlukan reaktan HIO3 sebagai oksidator untuk mereduksi HI menghasilkan I2, kemudian di reaksikan dengan senyawa alkana menghasilkan alkil iodida + Air yang tidak merupakan reaksi kesetimbangan. H3C H2 C CH3 + I2 H3C C H CH3 I + HI propana 2-iodopropil
- 17. Contoh idonasi 2-metil butana dengan oksidator HIO3 Mekanis reaksi kimianya sbb
- 18. Alkil Iodida mudah dibuat dengan cara mereaksikan NaI dengan alkil klorida atau alkil bromida dalam pelarut metanol atau aseton. Secara umum dapat ditulis sebagai berikut : Contoh reaksi butil klorida dengan NaI dalam pelarut aseton. Mekanisme reaksi kimianya sbb.
- 19. 2.3.2. NITRASI ALKANA Nitrasi alkana merupakan reaksi substitusi atom H-primer/H- Sekunder/H-tersier dengan gugus nitro-NO2 dari asam nitrat- HNO3/HONO2 atau campuran HNO3 dengan H2SO4 pekat dan berlansung pada suhu 150-475oC. Hasil reaksi nitrasi pada senyawa alkana berupa campuran senyawa mono nitroalkana. Contoh nitrasi 2,2,3-trimetil butana. Mekanisme reaksi kimianya sbb.
- 21. 2.3.3. SULFONASI ALKANA Sulfonasi alkana merupakan proses substitusi H-primer/H- Sekunder/H-tersier pada senyawa alkana dengan gugus sulfonat dari asam sulfat-H2SO4, terutama asam sulfat berasap agar reaksinya lebih cepat berlangsung menghasilkan sulfonat alkana. Sulfonasi pada alkana normal mulai dari heksana dan seterusnya. Mudahnya substitusi atom H oleh gugus solfonat–SO3H mengikuti protonasi H+ dengan urutan H-tersier >H-sekunder > H-primer. Contoh Sulfonasi pada 2-sikloheksil-3,3,4-trimetil-4-etil heksana.
- 22. Contoh sulfonasi 2-sikoheksil-3,3,4-trimetil-4-etil heksana Mekanisme reaksi kimianya sbb
- 23. 2.3.4. OKSIDASI ALKANA Oksidasi senyawa alkana merupakan proses oksidasi dengan cara mereduksi ikatan -C-H, -C-C- pada senyawa alkana oleh oksidator menghasilkan senyawa alkohol, aldehida, asam karboksilat dan senyawa alkohol glikol tergantung pada struktur alkana dan kondisi reaksi. Semua senyawa alkana dapat terbakar pada oksigen berlebihan atau oksigen dalam udara menghasilkan gas CO2 dan H2O. Oksidator yang sering digunakan pada senyawa alkana antara lain KMnO4 panas dan KMnO4 dingin, K2Cr2O7, KCrO4. Jika digunakan KMnO4 panas menghasilkan senyawa aldehida, alkohol, keton dan asam karboksilat tergantung pada struktur senyawa alkana. Jika digunakan KMnO4 dingin menghasilkan senyawa alkohol glikol.
- 24. Laju oksidasi senyawa alkana mengikuti laju substitusi H-tersier > H- sekunder > H-primer. Selain memutuskan ikatan-C- H, KMnO4 panas dapat memutuskan ikatan -C-C- dalam senyawa alkana, sedangkan KMnO4 dingin tidak memutuskan ikatan-C-C- pada alkana. Demikian juga jika menggunakan K2Cr2O7, KCrO4. Contoh Oksidasi 3-etil-2-metil-2-siklopentil pentana dengan KMnO4 panas dan KMnO4 dingin.
- 27. 2.3.5. ISOMERISASI ALKANA Isomerisasi alkana merupakan perubahan struktur senyawa alkana normal/rantai lurus menjadi senyawa alkana bercabang, terutama cabang metil dengan bantuan pemanasan pada suhu minimal 300 0C dan katalis AlCl3. Contoh. Isomerisasi pentana pada suhu 3400C dengan bantuan katalis AlCl3.
- 28. 2.4. SINTESIS ALKANA Senyawa alkana dapat dibuat atau disintesis dengan beberapa cara sebagai berikut 2.4.1. Hidrogenasi/reduksi katalitik senyawa hidrokarbon tidak jenuh. Sintesis alkana dengan cara hidrogenasi, umumya digunakan katalis Ni atau disebut Reduksi Sabatier-Senderens. Selain Ni, katalis lain yang dapat digunakan antara lain Pd, dan Nikel Rayney-Ni-Al pada NaOH. Pola umum mekanisme reaksinya sebagai berikut
- 29. Contoh Hidrogenasi 2, 3-dimetil pentena-2 Mekanisme reaksinya sebagai berikut Catatan perbaiki reaksi dan nama sywa yg msh salah 2.4.2. Reduksi alkil halida. Reduksi alkil halida pada alkena dapat dilakukan dengan 2 cara sebagai berikut 2.4.2.1. Reduksi alkil halida dengan cara melarutkan reduktor logam Zn dalam asam asetat atau asam klorida, atau reduktot paduan Zn-Cu dilarutakan dalam etanol. Pola umum mekanisme reaksi ditulis sebagai berikut
- 30. Contoh reduksi alkil halida isobutil klorida dengan reduktor logam Zn dilarutkan dalam asam klorida. Mekanisme reaksinya sebagai berikut
- 31. 2.4.2.2. Reduksi Alkil halida primer dan sekunder dengan reduktor litium alminium hidrida-LiAlH4 menghasilkan alkana. Contoh Reduksi isobuti klorida dengan redutor LiAlH4 Mekanisme reaksinya sebagai berikut