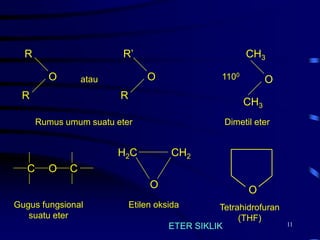
Dokumen ini menjelaskan struktur, nama, dan sifat-sifat alkohol dan eter, termasuk penggolongan alkohol menjadi primer, sekunder, dan tersier. Selain itu, juga dibahas proses sintesis alkohol dari alkena melalui hidrasi dan reaksi oksimerkurasi-demerkurasi. Contoh alkohol penting seperti metanol dan etanol serta sifat fisiknya seperti kelarutan dan titik didih juga diuraikan.