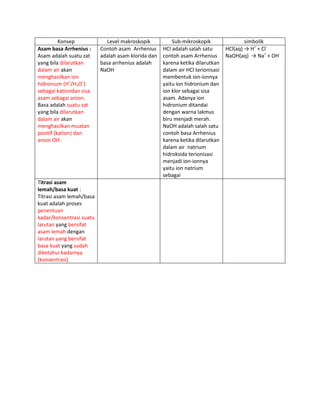
Konsep Asam Basa Arrhenius dan Titrasi Asam Lemah Basa Kuat
- 1. Konsep Level makroskopik Sub-mikroskopik simbolik Asam basa Arrhenius : Contoh asam Arrhenius HCl adalah salah satu HCl(aq) → H+ + Cl- Asam adalah suatu zat adalah asam klorida dan contoh asam Arrhenius NaOH(aq) → Na+ + OH- yang bila dilarutkan basa arrhenius adalah karena ketika dilarutkan dalam air akan NaOH dalam air HCl terionisasi menghasilkan ion membentuk ion-ionnya hidronium (H+/H3O+) yaitu ion hidronium dan sebagai kationdan sisa ion klor sebagai sisa asam sebagai anion. asam. Adanya ion Basa adalah suatu zat hidronium ditandai yang bila dilarutkan dengan warna lakmus dalam air akan biru menjadi merah. menghasilkan muatan NaOH adalah salah satu positif (kation) dan contoh basa Arrhenius anion OH-. karena ketika dilarutkan dalam air natrium hidroksida terionisasi menjadi ion-ionnya yaitu ion natrium sebagai Titrasi asam lemah/basa kuat : Titrasi asam lemah/basa kuat adalah proses penentuan kadar/konsentrasi suatu larutan yang bersifat asam lemah dengan larutan yang bersifat basa kuat yang sudah diketahui kadarnya (konsentrasi)