CU_Reliv_MDT_FIRST_2023_TR.pptx
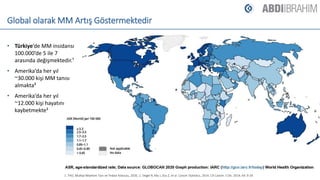
- 1. Global olarak MM Artış Göstermektedir • Türkiye’de MM insidansı 100.000’de 5 ile 7 arasında değişmektedir.¹ • Amerika’da her yıl ~30.000 kişi MM tanısı almakta² • Amerika’da her yıl ~12.000 kişi hayatını kaybetmekte² 1. THD, Multipl Miyelom Tanı ve Tedavi Kılavuzu, 2020, 2. Siegel R, Ma J, Zou Z, et al. Cancer Statistics, 2014. CA Cancer J Clin. 2014; 64: 9-29.
- 2. MM Tüm Kanserlerin %1.5’unu ve Hematolojik Malignitelerin %13’ünü Oluşturur • t(11; 14), t(14; 18), t(8; 14); 13q del, C MYC, RAS onkogen aktivasyonu, IL 6, IL1-, IL-2, IFN 1. https://www.aferez.org/download/10-ulusal-aferez-kongresi/sunumlar/multipl-miyelom-patogenezi-ve-lenalidomid-ile-hastalik-progresyonuna-kadar-tedavi.pdf • Her yıl ~90.000 (50.000 erkek, 40.000 kadın) yeni vaka tespit edilmektedir.¹ • Her yıl ~65.000 kişi MMʼdan ölmektedir.¹
- 3. Türkiye’de her sene 7.500’den fazla hasta MM tanısı alacaktır Tablo: Global Cancer Observatory: Cancer Today. Lyon, France: International Agency for Research on Cancer. https://gco.iarc.fr/today (accessed on 7 May 2020) • Amerika verilerinden yola çıkarak: Türkiye’de her sene 3.000’den fazla hastanın hayatını kaybedeceğini öngörebiliriz. • Türkiye, jeopolitik konumu sebebiyle göç almaktadır ve önümüzdeki yıllarda bu göçün artması beklenmektedir.
- 4. IMID Sayesinde 7 yılı aşan OS Sürelerine ulaşılmıştır¹ • Proteozom inhibitörleri (PI) ve İmmünomodülatör ilaçların (IMID) MM’de kullanıma girmesi ile birlikte: 5 yıllık OS %25-34’ten, %49-56’lara kadar yükselmiştir.² Tablo: Kumar et al Leukemia 2014 May;28(5):1122-8. 1. THD, Ulusal MM Tanı ve Tedavi Kılavuzu, 2020 2. Relaps Refrakter Multiple Myelomda Lenalidomid, deksametazon, Iksazomib Kombinasyonu Deneyimi, Uludağ Üniversitesi Tıp Fakültesi Dergisi 49 (1) 95-99, 2023 • 1056 hasta 2001–2005 ve 2006–2010 kollarında gruplandırılmıştır. • Özellikle > 65 yaş hastalarda genel sağkalım (OS) iyileşmiştir (P = 0.001). 1.0 0.8 0.6 0.4 0.2 0 0 1 2 3 4 5 Teşhisten sonraki izlem (yıl) Kumar et al Leukemia 2014 May;28(5):1122-8. 2006–2010’da teşhis 2001–2005’de teşhis Sağkalım oranı Sağkalım 2001 – 2005 2006 – 2010 P Medyan OS, yıl 4.6 NR 0.001 1-yıllık sağkalım, % 83 90 5-yıllık tahmini OS, % Genel 48 66 > 65 yaş 31 56 0.001 < 65 yaş 63 73 NS Tablo: Global Cancer Observatory: Cancer Today. Lyon, France: International Agency for Research on Cancer. https://gco.iarc.fr/today (accessed on 7 May 2020)
- 5. Tümör süpresör genleri indükler Stromal hücre desteğini bozar İmmün fonksiyonu düzenler, tümör ölümünü arttırır Hüre siklüs arresti Kaspaz aktivasyonu Tümör hücre apoptozisi NK hücre aracılı tümör hücresi ölümü Aşı cevabında artış DC, T, NK ve NKT hücrelerini aktive eder Humoral cevap artışı Tümör yükü Lenalidomid Anti-Kanser ve Anti-Enflamatuar Etkinlikleriyle Beraber Multifonksiyonel bir Tedavi Yaklaşımıdır Ludwig H, et al. Oncologist. 2012;17:592-606. Zaman Lenalidomid
- 6. Lenalidomid gibi standart tedaviler, KHT olamayanlara, PFS ve OS’de anlamlı ölçüde katkıda bulunmaktadır.² 1. THD, Multipl Miyelom Ulusal Tanı ve Tedavi Kılavuzu, 2020 2. Aladağ Karakulak E, Büyükaşık Y. Kök hücre transplantasyonuna uygun olmayan hastalarda İmmünomodülatör tedavinin rolü. Göker H, editör. Multipl Miyelom. 1. Baskı. Ankara: Türkiye Klinikleri; 2019. • OKHN’e uygun hastalarda indüksiyon rejimi olarak siklofosfamid kombinasyonu ile karşılaştırıldığı 2 Randomize çalışma vardır. • Her 2 çalışmada da, 4 kürlük indüksiyon sonrası en az çok iyi kısmi yanıt oranları PI, Lenalidomid ve deksametazon kolunda anlamlı olarak yüksek saptanmıştır. • *THD-MM BAK OKHN’e uygun olmayan kırılgan hasta grubunda Vd rejimini remisyon indüksiyon seçeneği olarak uygun bulmuştur.¹
- 7. 1:1:1 ARM A Kol B Kol C N = 535 N = 541 N = 547 Kol A N = 535 LEN + Lo-DEX Progresif Hastalığa dek LEN 25mg D1-21/28 Lo-DEX 40mg D1,8,15, 22/28 LEN + Lo-DEX: 18 Kür (72 hafta) LEN 25mg D1-21/28 Lo-DEX 40mg D1,8,15, 22/28 MPT 12 Kür (72 hafta) MEL 0.25mg/kg D1-4/42 PRED 2mg/kg D1-4/42 THAL 200mg D1-42/42 PD, OS ve müteakip anti-MM Tx PD veya kabul edilemez toksisite Aktif Tedavi + PFS Takip Fazı 75 yaş üstü için Doz Azaltma uygulanmış 1,623 NDMM ≥65 yaş veya OKHN alamayan 18 Farklı Ülkede ve 246 Merkezde Gerçekleştirilen Randomize FIRST Faz-III Çalışmasına Yüksek Riskli Hastalar Dahil Edilmiştir pubmed.ncbi.nlm.nih.gov/29150421/ Uygunluk kriterleri: • ECOG ≤2 • CrCl <30 • Floresan in-situ Hibridizasyon analizlerinde t(4; 14), t(14; 16), del(17p) yüksek riskli olarak sınıflandırıldı. • PFS Primer Sonlanım • OS Sekonder Sonlanım Son analiz önceden belirlenmiş ≥60 aylık takip
- 8. Lenalidomid, Yüksek Riskli Hastalarda bile MPT ile Kıyaslandığında PFS ve OS’de Üstünlük Göstermiştir *Hasta sayısı başına olay sayısı. • 501 Hasta Tam Yüksek Riskli Sitogenetikler arasında yer alıyordu. 1. ashpublications.org/blood/article/131/3/301/38303/Final-analysis-of-survival-outcomes-in-the-phase-3 • 67 aylık bir medyan takipte PFS, Rd Cont. vs MPT için anlamlı olarak daha uzundu ([HR] 0.69; % 95 [CI], 0.59-0.79; P < .00001) ve benzer şekilde Rd18'e karşı genişletildi.
- 9. Kırılganlık veya Yaş Farkı Gözetmeksizin Lenalidomid MPT ile Kıyaslandığında Üstünlük Göstermiştir ashpublications.org/blood/article/131/3/301/38303/Final-analysis-of-survival-outcomes-in-the-phase-3 • ISS aşaması olan ve olmayan kırılganlık alt grupları kullanıldığında: Ölüm Riskinde: • Rd Cont. vs Rd %30 azalma • Rd vs MPT %28 azalma
- 10. IMWG Kriterleri İle Değerlendirilen Tedaviye Yanıt 1. Bahlis NJ, Corso A, Mugge L‐O, et al. Randomize FIRST çalışmasında yeni tanı konmuş multipl miyelomlu yanıt verenler için sürekli tedavinin yararı. Lösemi. 2017; 31(11):2435–2442 2. ashpublications.org/blood/article/131/3/301/38303/Final-analysis-of-survival-outcomes-in-the-phase-3 • Rd sürekli ayrıca MPT veya Rd18'e kıyasla her yanıt alt grubunda (tam yanıt [CR] olanlar dahil) önemli ölçüde daha dayanıklı yanıtlar ve uzun süreli PFS elde etti.¹ • Hem tedavi amaçlı (ITT) popülasyonunda, hem de standart riskli sitogenetiğe sahip hastalarda, MPT ile karşılaştırıldığında Lenalidomid ile hastalarda daha yüksek kalitede yanıtlar gözlemlendi.²
- 11. • Kanada (n = 312) ve ABD(n = 252) bölgelerinden hastalar Rd sürekli, Rd104 ve MPT kollarına alınmıştır. Andrew Belch, Thierry Facon, Continuous lenalidomide and low-dose dexamethasone in patients with transplant-ineligible newly diagnosed MM: FIRST trial subanalysis of Canadian/US patients, 2020 Dec;9(23):8923-8930. doi: 10.1002/cam4.3511. Epub 2020 Oct 13. Kanada/ABD alt grubunun sonuçları, FIRST Çalışmasının ITT popülasyonundan elde edilen bulgularla tutarlıdır • Lenalidomid, MPT'ye karşı medyan PFS‘de 9 ay uzatmıştır.
- 12. Lenalidomid’in Diğer Tıbbi Ürünler ile Etkileşimi • Eritropoetik ilaçlar veya hormon replasman tedavisi gibi tromboz riskini artırabilen diğer ilaçlar, deksametazon ile birlikte RELİV almakta olan multipl miyelom hastalarında dikkatle kullanılmalıdır (bkz. Bölüm 4.4 ve 4.8). • Oral kontraseptifler: Oral kontraseptiflerle hiçbir etkileşim çalışması yapılmamıştır. Tedavi süresince oral kontraseptiflerin etkililiği azalabilir. Gebeliği önlemek için etkili önlemler alınmalıdır (bkz. Bölüm 4.4 ve 4.6). 21 • Bir enzim indükleyicisi değildir. İnsan hepatositleriyle yapılan bir in vitro çalışmada RELİV, test edilen çeşitli konsantrasyonlarda CYP1A2, CYP2B6, CYP2C9, CYP2C19 ve CYP3A4/5’i indüklememiştir. Bu nedenle, RELİV’in tek başına uygulandığı durumlarda, hormonal kontraseptifler dahil olmak üzere tıbbi ürünlerin etkililiğinde azalmaya yol açan indüksiyon beklenmemektedir. Bununla birlikte, deksametazonun zayıf ila orta derecede CYP3A4 indükleyicisi olduğu bilinmektedir ve ayrıca taşıyıcıların yanı sıra diğer enzimleri de etkilemesi olasıdır. • Varfarin : Birden fazla 10 mg dozda RELİV’in tek doz (25 mg) varfarin ile birlikte uygulanmasının toplam RELİV’in veya R- ve S- varfarinin farmakokinetiği üzerine herhangi bir etkisi olmamıştır. Bununla birlikte, klinik kullanım sırasında (deksametazon ile birlikte tedavi) bir etkileşim bulunup bulunmadığı bilinmemektedir. • Deksametazon zayıf ila orta derecede enzim indükleyicisidir ve varfarin üzerine etkisi bilinmemektedir. Tedavi sırasında varfarin konsantrasyonunun yakın takibi önerilmektedir. • Digoksin: Günde bir kez lenalidomid 10 mg ile birlikte uygulanması, digoksinin (0,5 mg, tek doz) plazma konsantrasyonunu %90 GA (güven aralığı) ile %14 artırmıştır; [%0,52 - %28,2]). Etkinin klinik kullanımda (daha yüksek lenalidomid dozları ve deksametazon ile birlikte tedavi) farklı olup olmayacağı bilinmemektedir. Bu nedenle, RELİV tedavisi sırasında digoksin konsantrasyonlarının izlenmesi tavsiye edilmektedir. • Statinler: lenalidomid ile uygulandığında aditif olabilecek, artmış bir rabdomiyoliz riski söz konusudur. Tedavinin ilk haftalarında artırılmış klinik ve laboratuvar takip gerekmektedir. Deksametazon Tek ya da çoklu deksametazon dozunun (günde bir kez 40 mg) eşzamanlı uygulanmasının, lenalidomidin (günde bir kez 25 mg) çoklu doz farmakokinetiği üzerinde klinik açıdan anlamlı bir etkisi olmamıştır. https://titck.gov.tr/storage/Archive/2023/kubKtAttachments/RELV25mgKB_65596db6-6f31-4bbc-89fd-f00a93cbd7f4.pdf
- 13. Hastanın Doğurma Potansiyeline Sahip Olmadığını Gösteren Güvenilir Kanıt Bulunmuyorsa Lenalidomid Gebelik Önleme Programı Kapsamında Reçete Edilmelidir Gebelik Önleme Programı’nın tüm koşullarına uyulmayan durumlarda, çocuk doğurma potansiyeli olan kadınlar (bkz. Bölüm 4.4 ve 4.6) Teratojenik Etkisi Nedeniyle, gebelik kategorisi X’tir. Etkin maddeye veya yardımcı maddelerden herhangi birine karşı aşırı duyarlılık
Editor's Notes
- What is the difference between modulating and regulating? Modulating control valves let you position the valve anywhere between fully open and fully closed, which is typically between 0º and 90º. Regulating the flow rate lets you control other system variables like temperature, liquid level, or concentration.
- Serum ve idrar elektroforezleri, albümin, LDH, B2M, kemik survey, standart sitogenetik ve FISH ile 17p del, t(4;14), t(14;16), t(14;20) Rutin kontrol sırasında semptomsuz vakalarda, anemi, sedimantasyon yüksekliği, proteinüri şeklinde saptanırken; Geç kalınan vakalarda kemik ve eklem ağrısı, renal (miyelom böbreği) yetmezlik ve nörolojik semptomlar (hipervizkosite) ile geç tanınır. Daha sıklıkla kemik kırığı nedeniyle çekilen bir x-ray filmi sonrası doktorlar multipl miyelomdan şüphelenir. İdrar testleri: M proteininin bir tipi olan Bence Jones proteini aranır. 24-saatlik idrarda YÜKSEK Bence Jones protein miktarı ölçülür. Bence Jones proteini böbrekleri tıkayıp hasara neden olabilir. Kemik iliği aspirasyonu Kemik iliği biyopsisi
- Lenalidomide 2006 yılında FDA tarafından steroid deksametazon ile birlikte kullanılmak üzere nüks gösteren ve dirençli miyelom hastalarının tedavisi için Diğer birçok ülkede de miyelom tedavisi için onaylanmıştır. Bununla birlikte Ulusal Kapsamlı Kanser Ağının (NCCN) kılavuz incelemesine dayanarak, ABD’de Revlimid hâlen nüks eden/dirençli durumdaki kullanımına ilaveten, birinci basamak (indüksiyon) tedavi, idame tedavisi ve erken nüks dâhil, hastalığın tüm seyri boyunca yaygın şekilde kullanılmaktadır.
- İmmünosit aktivasyonunu tetikler, T-lenfositleri ve NK hücrelerinin faaliyetini arttırır. Sitokinler ve interlökinler gibi çeşitli büyüme faktörlerinin düzeylerini değiştirebilir. Lenalidomid ayrıca bir vasküler endotelyal büyüme faktörü inhibitörüdür ve malin mikrovaskularizasyonu durdurur. Lenalidomidin tümör öldürücü etkileri, E3 ubikitin ligaz kompleksinin bir bileşeni olan sereblon'u hedef alarak miyelom hücrelerinde aracılık eder. Bu etkileşim, transkripsiyon faktörleri Ikaros ve Aiolos'un proteazom yıkımını tetikler, bu da miyelom sağkalım sinyalleri IRF4 ve MYC'nin aşağı regülasyonuna ve immünoregülatör molekül interlökin 2'nin yukarı regülasyonuna neden olur. Lenalidomid deksametazon ile kombinasyon halinde uygulandığında sinerjik etkiler gözlenir, bu da bu rejimi yeni teşhis edilen ve nükseden multipl miyelomlu hastalarda tedavi standartlarından biri haline getirmiştir.
- Yeni tanı almış OKHN’ye uygun hastalarda ideal indüksiyon rejiminin tanımlanması için pek çok faz 2 ve 3 çalışma yürütülmüştür. Mevcut çalışmalar ile 3’lü indüksiyon rejimlerinin artmış yanıt oranları, yanıt derinliği, progresyonsuz sağkalım ve genel sağkalım ile ilişkili olduğunu ortaya konmuştur.
- 2008-2011 Global, açık etiketli, hastalar daha önce tedavi edilmemiş, semptomatik ve ölçülebilir MM olan ≥18 yaşındaydı. yaşa (≤75'e karşı >75 yıl), ISS (I / II vs III) ülkeye göre ayarlandı. 1-21. günlerde oral lenalidomid artı 1 günlük tedavi döngülerinin 8, 15, 22 ve 28. günlerinde oral deks verildi. MPT kolundaki hastalara 1-4. günlerde oral melfalan, 1-4. günlerde oral prednizon ve on iki 42 günlük döngüde (72 hafta) günlük oral talidomid verildi. Başlangıç dozları >75 yaş arası hastalar için ayarlandı. Medyan işletim sistemi, Rd sürekli ve MPT ile 10 ay daha uzundu (59.1'e karşı 49.1 ay; İK, 0,78; %95 CI, 0.67-0.92; P = .0023) ve Rd18 (62.3 ay) ile benzer. Primer sonlanım: PFS Sekonder sonlanım: Genel sağ kalım, ≥KY, yanıt süresi, hastalığın progresyonuna dek geçen süre, ikinci antimyelom tedavisine kadar geçen süre, yaşam kalitesi ve güvenlik Yanıt: Her tedavi siklüsü sonrası uluslarası yanıt kriterlerine göre Ortanca tedavi süresi: Rd devamlı: 18.4 ay, Rd 18 ay: 16.6 ay, MPT: 15.6 ay Rd süresi >2 yıl: Hastaların %39 Medyan izlem: 37 ay
- ORR, TTNT (which censors deaths), and safety, including second primary malignancies (SPMs), were also secondary endpoints. Time from randomization to second progression or death (PFS2) was an exploratory endpoint. 5.6 yıllık medyan takipte, çalışmadaki tüm hastaların% 56'sı sırasıyla Rd sürekli 286 Rd ve 283 MPT kollarında, 337 ve 18 ölümle (906 toplam ölüm) ölmüştür. Son analiz, MPT ile karşılaştırıldığında Rd sürekli olduğunu ortaya koymuştur (HR, 0.78; %95 CI, 0.67-0.92; P = .0023)
- Önemli bulgular: Nihai veri kesintisi: 21 Ocak 2016 Hayatta kalan hastalar için medyan takip süresi = 67 ay (0-86,8) Esas olarak hastalığın ilerlemesi nedeniyle çalışmanın kesilmesi: Rd18 (%67), MPT (%62) kolları ve Rd sürekli kolu (%51) MPT'ye karşı sürekli Rd ile PFS'de önemli artış: HR = 0,69 (%95CI, 0,59-0,79); P < 0,00001 Rd sürekli vs Rd18 vs MPT: Medyan PFS = 26,0 vs 21,0 vs 21,9 ay 4 yıllık PFS oranı = %32,6 vs %14,3 vs %13,6 Yüksek riskli olmayan sitogenetiğe sahip hastalarda Rd18 ve MPT ile karşılaştırıldığında Rd süreklisinde uzun süreli PFS Rd18'e karşı sürekli Rd (HR = 0,52; %95 GA, 0,40–0,66) ve MPT'ye karşı sürekli Rd (HR = 0,47; %95 GA, 0,38–0,59) ile CR veya VGPR elde eden hastalar için daha yüksek PFS faydası Sürekli Rd için CR, Rd18 ile MPT: Medyan PFS = 41,0 ile 37,6 ay arasında ulaşılamadı İyi yanıt verenler (VGPR veya CR) Rd sürekli tedavisinden yararlandı Rd sürekli vs Rd18 vs MPT: ≥ VGPR = %79 vs %70 vs %53 Rd sürekli vs Rd18 vs MPT: Medyan OS = 59,1 vs 62,3 vs 49,1 ay Bir sonraki antimiyelom tedavisine kadar geçen medyan süre (TNTT) = 36,7'ye karşı 28,5'e karşı 26,7 ay ≥ VGPR elde eden hastalarda medyan TNTT = 69,5 vs 39,9 vs 37,7 ay Rd sürekli ve MPT: ≥ VGPR'ye ulaşan hastalar için medyan OS = 79,5'e karşılık 55,7 ay; HR = 0,63; (%95 GA, 0,48–0,83) ORR (≥ PR) = %81 vs %67 Hem tedavi amaçlı (ITT) popülasyonda hem de standart riskli sitogenetiğe sahip hastalarda MPT ile karşılaştırıldığında sürekli Rd ile tedavi edilen hastalarda daha yüksek kalitede yanıtlar gözlemlendi İkinci basamak tedaviye ilişkin olarak, 557 hasta bortezomib bazlı rejimlerle tedavi edildi: Rd sürekli kol: 179 (%60) hasta; Kd18 kolu: 208 (%55) puan; MPT kolu: 170 (%45) puan ≥ VGPR, Rd sürekli ve Rd18 kollarında ikinci basamak tedavi olarak bortezomib alan hastalarda MPT koluna göre daha sıktır
- Önemli bulgular: Nihai veri kesintisi: 21 Ocak 2016 Hayatta kalan hastalar için medyan takip süresi = 67 ay (0-86,8) Esas olarak hastalığın ilerlemesi nedeniyle çalışmanın kesilmesi: Rd18 (%67), MPT (%62) kolları ve Rd sürekli kolu (%51) MPT'ye karşı sürekli Rd ile PFS'de önemli artış: HR = 0,69 (%95CI, 0,59-0,79); P < 0,00001 Rd sürekli vs Rd18 vs MPT: Medyan PFS = 26,0 vs 21,0 vs 21,9 ay 4 yıllık PFS oranı = %32,6 vs %14,3 vs %13,6 Yüksek riskli olmayan sitogenetiğe sahip hastalarda Rd18 ve MPT ile karşılaştırıldığında Rd süreklisinde uzun süreli PFS Rd18'e karşı sürekli Rd (HR = 0,52; %95 GA, 0,40–0,66) ve MPT'ye karşı sürekli Rd (HR = 0,47; %95 GA, 0,38–0,59) ile CR veya VGPR elde eden hastalar için daha yüksek PFS faydası Sürekli Rd için CR, Rd18 ile MPT: Medyan PFS = 41,0 ile 37,6 ay arasında ulaşılamadı İyi yanıt verenler (VGPR veya CR) Rd sürekli tedavisinden yararlandı Rd sürekli vs Rd18 vs MPT: ≥ VGPR = %79 vs %70 vs %53 5,6 yıllık (yıl) ortalama takipte ölüm sayısı: Rd sürekli =286 puan; Kd18 =283 puan; MPT =337 puan Rd sürekli vs Rd18 vs MPT: Medyan OS = 59,1 vs 62,3 vs 49,1 ay Bir sonraki antimiyelom tedavisine kadar geçen medyan süre (TNTT) = 36,7'ye karşı 28,5'e karşı 26,7 ay ≥ VGPR elde eden hastalarda medyan TNTT = 69,5 vs 39,9 vs 37,7 ay Rd sürekli ve MPT: ≥ VGPR'ye ulaşan hastalar için medyan OS = 79,5'e karşılık 55,7 ay; HR = 0,63; (%95 GA, 0,48–0,83) ORR (≥ PR) = %81 vs %67 Hem tedavi amaçlı (ITT) popülasyonda hem de standart riskli sitogenetiğe sahip hastalarda MPT ile karşılaştırıldığında sürekli Rd ile tedavi edilen hastalarda daha yüksek kalitede yanıtlar gözlemlendi İkinci basamak tedaviye ilişkin olarak, 557 hasta bortezomib bazlı rejimlerle tedavi edildi: Rd sürekli kol: 179 (%60) hasta; Kd18 kolu: 208 (%55) puan; MPT kolu: 170 (%45) puan ≥ VGPR, Rd sürekli ve Rd18 kollarında ikinci basamak tedavi olarak bortezomib alan hastalarda MPT koluna göre daha sıktır
- Bu hasta alt grubunda Rd, MPT'ye karşı medyan PFS'yi 9 ay ve Rd7'e karşı >18 ay uzatmıştır. Rd sürekli ayrıca daha derin yanıtlar elde etti (≥VGPR oranında% ≈20 artış) ve medyan TTNT'yi MPT'ye kıyasla >14 ay geciktirdi. Ayrıca, Rd sürekliliği, MPT'ye karşı daha uzun bir PFS2 ile sonuçlandı, bu da ön cephe Rd sürekliliğinin yararının nüksetmede korunduğunu düşündürmektedir. Birlikte, bu sonuçlar NDMM'li nakil için uygun olmayan hastalar için bakım standardı olarak Rd sürekli tedavisini daha da desteklemektedir. Bu çalışma,. Ayrıca, Rd sürekli veya Rd18'den sonra bortezomib bazlı tedavi ile tedavi edilen hastaların, ikinci basamak tedaviye, MPT'den sonra bortezomib bazlı tedavi verilen hastalara göre daha kaliteli yanıtlar sergiledikleri de bulunmuştur.
- 1a) 3 üncü kür sonunda en az minör yanıt yoksa tedavi sonlandırılır. 3 üncü kür sonunda en az minör yanıt, 6 ncı kür sonunda en az kısmi yanıt var ise tedaviye devam edilir. Tedavinin devamında her 6ncı kür sonunda en az kısmi yanıt var ise tedavi toplam 26 küre tamamlanabilir. 2b) Tedavinin 4. ayın sonunda yapılan yanıt değerlendirmesinde, 8 hafta içinde hiç transfüzyon yapılmamış olması koşulu ile transfüzyon ihtiyacının ortadan kalkması halinde bu durum ilgili sağlık kurulu raporunda belirtilir. Sağlık kurulu raporları ile tedavi 12. aya kadar uzatılabilir. 4. ayda yapılan yanıt değerlendirmesinde transfüzyon ihtiyacının ortadan kalkmaması halinde tedavi sonlandırılır.
- MM-020
- Kısıtlamalı Beyaz Reçete ilaç: EKLEME YENI URUN. SATIS IZNI ALINDIKTAN SONRA PAZARA SUNULABILIR. 14.03.2023 TARIHLI RESMI GAZETEDE YAYIMLANAN KARARA GORE ECZACI KAR ORANI BAREMLERI GUNCELLENMISTIR.GONULLU FIYAT DUSUSU. FIRMA STOK ZARARLARINI KARSILAMAYI TAAHHUT ETMEKTEDIR.
- Revlimid-Celgene Thalidomide analogue 2018 Sales: $9.685 billion 2017 Sales: $8.187 billion % Change: 18.3%
- Anlamı belirlenemeyen monoklonal gamopati (MGUS) semptom vermeyen premalign klonalite gösteren bir plazma hücre hastalığı ya da lenfoplazmasitik proliferatif hastalıktır. MGUS'un üç farklı klinik tipi vardır, her birinin orta düzeyde (daha ileri) bir premalign evreye ve sonra da malign plazma hücre diskrazisine ya da lenfoproliferatif hastalığa progresyon riski vardır. MGUS monoklonal gamopati ile ortaya çıkan hastalıklardan da ayrılmalıdır. Bunlar multipl miyelom (smoldering ya da semptomatik), Waldenström Makroglobulinemisi (smoldering ya da semptomatik), idiyopatik Bence Jones proteinürisi ve primer amiloidozdur. Bu nedenle, genellikle uzun süreli takip önerilir.
- *IMWG: Uluslararası Miyelom Çalışma Grubu, *MPT: Melphalan, Prednisone, Thalidomide, *MPT: Melphalan, Prednisone, Bortezomib, Rd: Len/Dex
- PN: Periferik Nöropati, Lenalidomidin tümör öldürücü etkileri, E3 ubikitin ligaz kompleksinin bir bileşeni olan sereblon'u hedef alarak miyelom hücrelerinde aracılık eder. Bu etkileşim, transkripsiyon faktörleri Ikaros ve Aiolos'un proteazom yıkımını tetikler, bu da miyelom sağkalım sinyalleri IRF4 ve MYC'nin aşağı regülasyonuna ve immünoregülatör molekül interlökin 2'nin yukarı regülasyonuna neden olur. Lenalidomid deksametazon ile kombinasyon halinde uygulandığında sinerjik etkiler gözlenir, bu da bu rejimi yeni teşhis edilen ve nükseden multipl miyelomlu hastalarda tedavi standartlarından biri haline getirmiştir.
- Cevap elde edilen hastalarda Lenalidomid + deksametazon hastalık progresyonuna kadar devam edilmelidir. Rd tedavisi diğer tedavi seçeneklerinin kullanılamadığı stabil hastalara içinde uygulanabilir. Renal yetmezlikli hastalarda Lenalidomid + deksametazon tedavisi etkin ve güvenilirdir, her siklüsde kreatinin klirensine göre doz ayarlaması yapılır.