Mодели атома
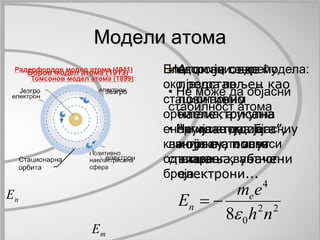
- 1. n E Модели атома m E Атом је овде представљен као позитивно наелектрисана “кугла пудинга”, у који су, попут вишања, убачени електрони... Електрони се крећу око језгра по стационарним орбитама, а укупна енергија атома је квантована и зависи од главног квантног броја... Недостаци овог модела: • Не може да објасни стабилност атома • Не може да објасни линијске атомске спектре m e 2 2 E e n 0 4 8 h n
- 2. n E Побуђивање атома Прелазак електрона са нивоа са нижом енергијом En, на ниво са вишом енергијом Em За овај процес, атому је потребна енергија • Фотон који би могао да изазове побуђивање атома између нивоа Еn и Еm, мора имати енергију: m E mn mn h E mn m n E E E
- 3. n E Зрачење атома Прелазак електрона са нивоа са вишом енергијом Еm на ниво са нижом енергијом Еn. У овом процесу, енергија се ослобађа Фотон који настаје преласком електрона са нивоа Еm, на ниво Еn има енергију: m E mn mn h E mn m n E E E
- 4. n E Спектар атома водоника m E Сви фотони који могу бити емитовани од стране неког елемента чине његов емисиони спектар Таласна дужина сваког фотона одређује једну линију у спектру... 1 1 1 2 2 n m R mn m R 1 1,097 107 R – Ридбергова константа
- 5. n E Још неки атомски спектри... m E
- 6. n E Да ли је могуће? Да атоме можемо препознати по линијама спектра? Израчунати таласну дужину фотона који настаје преласком са четвртог на други ниво енергије. Упоредити је са зелено – плавом линијом са слике спектра атома водоника. m E
