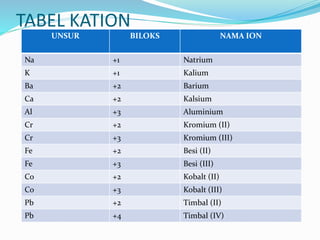
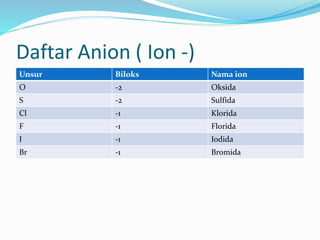
Dokumen ini membahas tentang penamaan senyawa biner dan poliatom di dalam kimia kelas X, termasuk cara penamaan senyawa ionik, senyawa non-logam, serta senyawa asam dan basa. Contoh-contoh diberikan untuk memperjelas bagaimana mengidentifikasi dan merumuskan senyawa berdasarkan bilangan oksidasi. Tabel kation dan anion juga disertakan sebagai referensi penggunaan nama ion dan senyawa.