Kurikulum 2013 dirancang untuk memperkuat kompetensi siswa dalam sikap, pengetahuan, dan keterampilan melalui pembelajaran terintegrasi di semua mata pelajaran. Buku ini menyediakan materi pendidikan yang memfasilitasi siswa untuk mencapai kompetensi yang diharapkan, dengan penekanan pada partisipasi aktif dan pencarian sumber informasi. Selain itu, peran guru sangat penting dalam menyesuaikan dan memperkaya pengalaman belajar siswa di lingkungan sosial dan alam.
































































































































































































































































![247
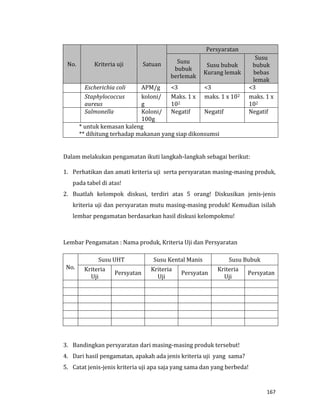
Tabel 27. Syarat Mutu Mie Instan
No Kriteria Uji Satuan Persyaratan
1. Keadaan 2]
1.1. Tekstur - Normal / Dapat diterima
1.2. Aroma - Normal/ Dapat diterima
1.3. Rasa - Normal/ Dapat diterima
1.4. Warna - Normal/ Dapat diterima
2. Benda asing2] - Tidak boleh ada
3. Keutuhan1] %,b/b Minimal 90
4. Kadar air2]
4.1. Proses penggorengan %,b/b Maksimum 10,0
4.2. Proses pengeringan %,b/b Maksimum 14,5
5. Kadar protein2]
5.1. Mi dari terigu %,b/b Minimal 8,0
5.2. Mi dari bukan terigu %,b/b Minimal 4,0
6. Bilangan asam1] mg KOH/g minyak Maksimal 2
7. Cemaran logam2]
7.1. Timbal (Pb) mg/kg Maksimal 2,0
7.2. Raksa (Hg) mg/kg Maksimal 0,05
8. Arsen (As)2] mg/kg Maks, 0,5
9. Cemaran mikroba2]
9.1. Angka lempeng total koloni/g Maks, 1,0 x 106
9.2 E.coli APM/g 3
9.3. Salmonela - Negatif per 25 g
9.4. Kapang koloni/g Maks, 1,0 x 103
1] berlaku untuk keping mi
2] berlaku untuk keping mi dan bumbunya
CATATAN Persyaratan mutu pada tingkat pedagang eceran
Sumber : SNI 01-3551-2000
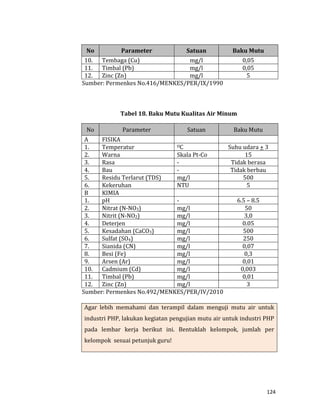
Dalam melakukan pengamatan ikuti langkah-langkah sebagai berikut:
1. Perhatikan dan amati kriteria uji serta persyaratan masing-masing produk,
pada tabel di atas!
2. Buatlah kelompok diskusi, terdiri atas 5 orang! Diskusikan jenis-jenis
kriteria uji dan persyaratan mutu masing-masing produk! Kemudian isilah
lembar pengamatan berdasarkan hasil diskusi kelompokmu!](https://image.slidesharecdn.com/pengujianmutupangan-150412232204-conversion-gate01/85/Pengujian-Mutu-Pangan-259-320.jpg)











































































































