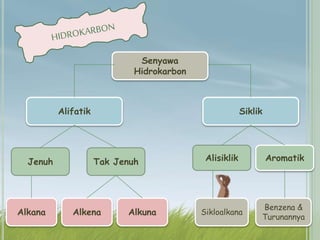
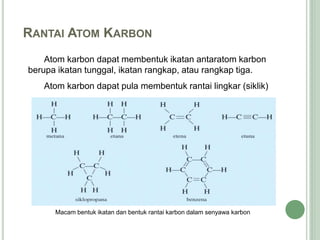
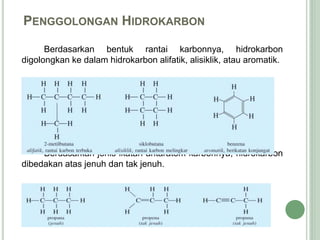
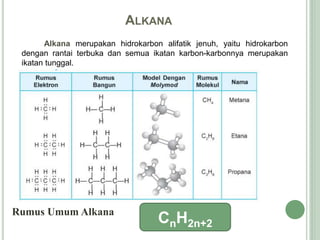
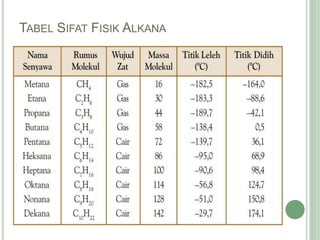
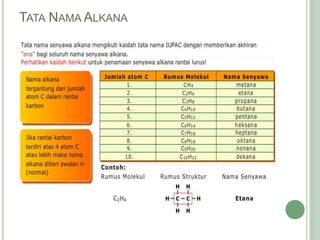
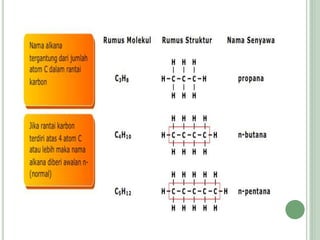
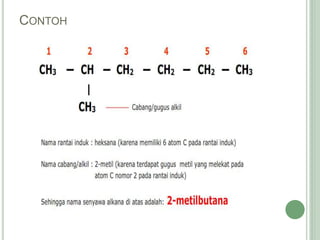
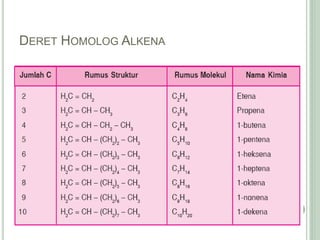
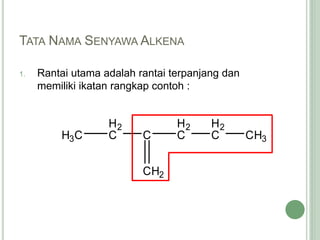
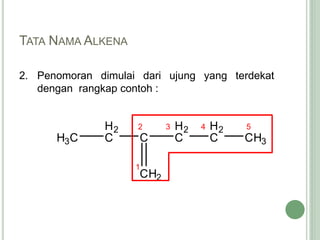
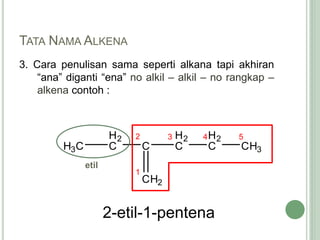
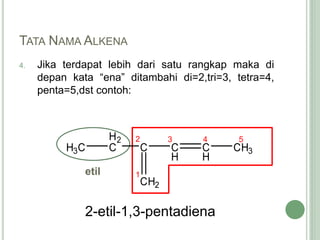
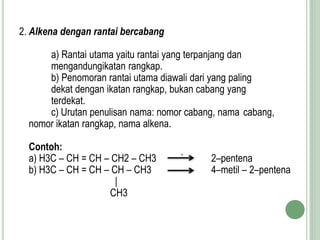
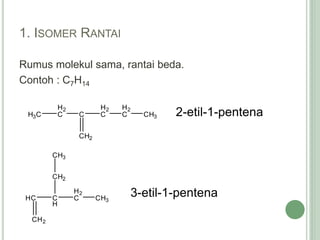
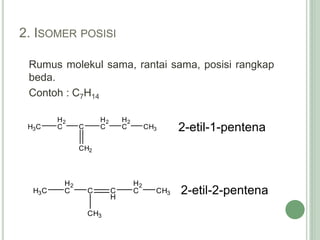
Hidrokarbon merupakan senyawa karbon yang tersusun atas karbon dan hidrogen. Terbagi menjadi alifatik, siklik, dan aromatik. Alifatik terbagi lagi menjadi jenuh (alkana) dan tak jenuh (alkena, alkuna). Alkana memiliki ikatan tunggal, alkena ikatan rangkap dua, alkuna ikatan rangkap tiga. Hidrokarbon digunakan sebagai bahan bakar, pelarut, dan bahan baku senyawa organik l