เอกสารประกอบการประชุม
Controversial in Asthma (20-22 Mar 2016) Final
สำนักงานของสภาองค์กรโรคหืดแห่งประเทศไทย
แหล่งข้อมูล:
http://www.tac.or.th/2011/sites/tac.or.th/files/%E0%B9%80%E0%B8%AD%E0%B8%81%E0%B8%AA%E0%B8%B2%E0%B8%A3%E0%B8%9B%E0%B8%A3%E0%B8%B0%E0%B8%81%E0%B8%AD%E0%B8%9A%E0%B8%81%E0%B8%B2%E0%B8%A3%E0%B8%9B%E0%B8%A3%E0%B8%B0%E0%B8%8A%E0%B8%B8%E0%B8%A1%20%20Controversial%20in%20Asthma%20(20-22%20Mar%202016)%20Final.pdf






























![27
เอกสารประกอบการประชุมวิชาการประจาปี 2559 สมาคมสภาองค์กรโรคหืดแห่งประเทศไทย
Controversial Issues in Asthma 2016
ภาคผนวก 1
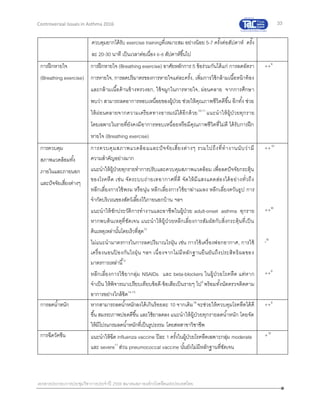
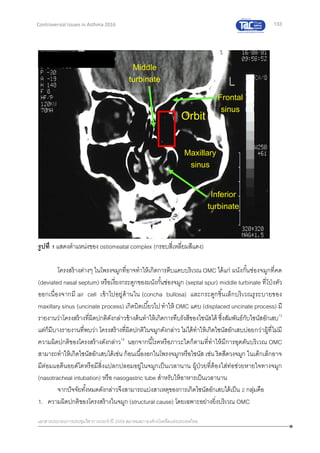
การวัดค่า PEFR variability เนื่องจาก Peak flow variability ถือเป็นหนึ่งในการวินิจฉัยและประเมินผลการ
ตอบสนองต่อการรักษาในผู้ป่วยหืด นอกเหนือจากการทดสอบสมรรถภาพปอด วิธีที่นิยมวัดและคานวณและ
ใช้บ่อยๆ คือ
1) ส่วนต่างของค่า PEFR สูงสุดกับค่าต่าสุด หารด้วยค่าเฉลี่ย ซึ่งเป็นค่าเฉลี่ยในรอบ 7-14 วัน วัดก่อน
พ่นยา pre-bronchodilator PEFR ทาการวัด 3 ครั้งในแต่ละเวลาที่วัด และเลือกค่าที่ดีสุด และใช้อุปกรณ์วัด
PEFR ชนิดเดิมทุกครั้งในการวัด วิธีนี้บ่งบอกถึงความผันแปรของ PEF ในวันเดียวกันในผู้ป่วยหืด การบันทึก
PEF วันละ 2 ครั้งพบว่า ค่าในประชากรมาตรฐานอยู่ที่ร้อยละ 986, 87
อย่างไรก็ตาม GINA แนะนาว่า สาหรับ
เกณฑ์ในการตัดแยก หากค่า PFER variability > ร้อยละ 10 ในผู้ใหญ่และ > ร้อยละ 13 ในเด็ก จากการวัดค่า
2 ครั้งต่อวัน ถือว่ามีความผิดปกติ1
และสาหรับการวินิจฉัย asthma การจาแนกว่าเป็น persistent asthma คือ
ร้อยละ 2088
PEF variability = average [PEFR highest –PEFR lowest]
Mean daily PEF
PEFR (L/min)
Time
(days)
D1 D2 D 3 D 4 D5 D6 D7
a.m.
p.m
a.m
p.m
a.m.
p.m.
a.m.
p.m
a.m.
p.m.
a.m.
p.m.
a.m.
p.m
600
500
400
300
200
100
0](https://image.slidesharecdn.com/controversialinasthma20-22mar2016final-160506101203/85/Controversial-in-asthma-20-22-mar-2016-final-31-320.jpg)








![37
เอกสารประกอบการประชุมวิชาการประจาปี 2559 สมาคมสภาองค์กรโรคหืดแห่งประเทศไทย
Controversial Issues in Asthma 2016
เอกสารอ้างอิง
1. GINA. Global strategy for asthma management and prevention 2014. Global Initiative for Asthma 2014 [cited 2014 June 2014];
Available from: http://www.ginasthma.org/guidelines-gina-report-global-strategy-for-asthma.html.
2. Worldwide variations in the prevalence of asthma symptoms: the International Study of Asthma and Allergies in Childhood
(ISAAC). Eur Respir J. 1998;12(2):315-35.
3. Hanania NA, Celli BR, Donohue JF, Martin UJ. Bronchodilator reversibility in COPD. Chest. 2011;140(4):1055-63.
4. Crapo RO, Casaburi R, Coates AL, Enright PL, Hankinson JL, Irvin CG, et al. Guidelines for methacholine and exercise
challenge testing-1999. This official statement of the American Thoracic Society was adopted by the ATS Board of Directors,
July 1999. Am J Respir Crit Care Med. 2000;161(1):309-29.
5. Nathan RA, Sorkness CA, Kosinski M, Schatz M, Li JT, Marcus P, et al. Development of the asthma control test: a survey for
assessing asthma control. J Allergy Clin Immunol. 2004;113(1):59-65.
6. Juniper EF, O'Byrne PM, Guyatt GH, Ferrie PJ, King DR. Development and validation of a questionnaire to measure asthma
control. Eur Respir J. 1999;14(4):902-7.
7. O'Byrne PM, Bisgaard H, Godard PP, Pistolesi M, Palmqvist M, Zhu Y, et al. Budesonide/formoterol combination therapy as both
maintenance and reliever medication in asthma. Am J Respir Crit Care Med. [Clinical Trial Multicenter Study Randomized
Controlled Trial]. 2005;171(2):129-36.
8. Rau JL. The inhalation of drugs: advantages and problems. Respir Care. 2005;50(3):367-82.
9. Cazzola M, Page CP, Calzetta L, Matera MG. Pharmacology and therapeutics of bronchodilators. Pharmacol Rev.
2012;64(3):450-504.
10. Pauwels RA, Pedersen S, Busse WW, Tan WC, Chen YZ, Ohlsson SV, et al. Early intervention with budesonide in mild persistent
asthma: a randomised, double-blind trial. Lancet. 2003;361(9363):1071-6.
11. Boulet LP, Cowie RL, Negro RD, Brett W, Gold M, Marques A, et al. Comparison of once- with twice-daily dosing of fluticasone
propionate in mild and moderate asthma. Can Respir J. 2000;7(3):239-47.
12. Busse WW, Pedersen S, Pauwels RA, Tan WC, Chen YZ, Lamm CJ, et al. The Inhaled Steroid Treatment As Regular Therapy in
Early Asthma (START) study 5-year follow-up: effectiveness of early intervention with budesonide in mild persistent asthma. J
Allergy Clin Immunol. 2008;121(5):1167-74.
13. Wilson AM, Dempsey OJ, Sims EJ, Lipworth BJ. A comparison of topical budesonide and oral montelukast in seasonal allergic
rhinitis and asthma. Clin Exp Allergy. 2001;31(4):616-24.
14. Busse W, Raphael GD, Galant S, Kalberg C, Goode-Sellers S, Srebro S, et al. Low-dose fluticasone propionate compared with
montelukast for first-line treatment of persistent asthma: a randomized clinical trial. J Allergy Clin Immunol. 2001;107(3):461-8.
15. Dahl R, Larsen BB, Venge P. Effect of long-term treatment with inhaled budesonide or theophylline on lung function, airway
reactivity and asthma symptoms. Respir Med. 2002;96(6):432-8.
16. Yurdakul AS, Taci N, Eren A, Sipit T. Comparative efficacy of once-daily therapy with inhaled corticosteroid, leukotriene
antagonist or sustained-release theophylline in patients with mild persistent asthma. Respir Med. 2003;97(12):1313-9.
17. Bateman ED, Boushey HA, Bousquet J, Busse WW, Clark TJ, Pauwels RA, et al. Can guideline-defined asthma control be
achieved? The Gaining Optimal Asthma ControL study. Am J Respir Crit Care Med. 2004;170(8):836-44.](https://image.slidesharecdn.com/controversialinasthma20-22mar2016final-160506101203/85/Controversial-in-asthma-20-22-mar-2016-final-41-320.jpg)

![39
เอกสารประกอบการประชุมวิชาการประจาปี 2559 สมาคมสภาองค์กรโรคหืดแห่งประเทศไทย
Controversial Issues in Asthma 2016
35. Humbert M, Beasley R, Ayres J, Slavin R, Hebert J, Bousquet J, et al. Benefits of omalizumab as add-on therapy in patients with
severe persistent asthma who are inadequately controlled despite best available therapy (GINA 2002 step 4 treatment):
INNOVATE. Allergy. 2005;60(3):309-16.
36. Bousquet J, Cabrera P, Berkman N, Buhl R, Holgate S, Wenzel S, et al. The effect of treatment with omalizumab, an anti-IgE
antibody, on asthma exacerbations and emergency medical visits in patients with severe persistent asthma. Allergy.
2005;60(3):302-8.
37. Bousquet J, Rabe K, Humbert M, Chung KF, Berger W, Fox H, et al. Predicting and evaluating response to omalizumab in
patients with severe allergic asthma. Respir Med. 2007;101(7):1483-92.
38. Molimard M, Mala L, Bourdeix I, Le Gros V. Observational study in severe asthmatic patients after discontinuation of
omalizumab for good asthma control. Respir Med. 2014;108(4):571-6.
39. Ohta K, Miyamoto T, Amagasaki T, Yamamoto M. Efficacy and safety of omalizumab in an Asian population with moderate-to-
severe persistent asthma. Respirology. 2009;14(8):1156-65.
40. Braunstahl GJ, Leo J, Thirlwell J, Peachey G, Maykut R. Uncontrolled persistent allergic asthma in practice: eXpeRience registry
baseline characteristics. Curr Med Res Opin. [Evaluation Studies Multicenter Study Research Support, Non-U.S. Gov't].
2011;27(4):761-7.
41. Poachanukoon O, Kawamatawong T, Saengasapaviriya A, Sittipunt C, Chantaphakul H, Maneechotesuwan K, et al. Long-Term
Effectiveness Of Omalizumab Treatment In Thai Severe Asthmatic Patients: A Real-Life Experience. Journal of Allergy and
Clinical Immunology.133(2):AB2.
42. M. Beeh K. Which patients should be treated with anti-IgE? EUROPEAN RESPIRATORY REVIEW. 2007;16(104):85-7.
43. Dworski R, Fitzgerald GA, Oates JA, Sheller JR. Effect of oral prednisone on airway inflammatory mediators in atopic asthma.
Am J Respir Crit Care Med. 1994;149(4 Pt 1):953-9.
44. Walsh LJ, Wong CA, Oborne J, Cooper S, Lewis SA, Pringle M, et al. Adverse effects of oral corticosteroids in relation to dose in
patients with lung disease. Thorax. 2001;56(4):279-84.
45. Cox G, Thomson NC, Rubin AS, Niven RM, Corris PA, Siersted HC, et al. Asthma control during the year after bronchial
thermoplasty. N Engl J Med. 2007;356(13):1327-37.
46. Castro M, Rubin AS, Laviolette M, Fiterman J, De Andrade Lima M, Shah PL, et al. Effectiveness and safety of bronchial
thermoplasty in the treatment of severe asthma: a multicenter, randomized, double-blind, sham-controlled clinical trial. Am J
Respir Crit Care Med. 2010;181(2):116-24.
47. Pavord ID, Pizzichini MM, Pizzichini E, Hargreave FE. The use of induced sputum to investigate airway inflammation. Thorax.
1997;52(6):498-501.
48. Green RH, Brightling CE, McKenna S, Hargadon B, Parker D, Bradding P, et al. Asthma exacerbations and sputum eosinophil
counts: a randomised controlled trial. Lancet. 2002;360(9347):1715-21.
49. Woolcock AJ. What are the important questions in the treatment of asthma? Clinical & Experimental Allergy Reviews.
2001;1(2):62-4.
50. Rank MA, Hagan JB, Park MA, Podjasek JC, Samant SA, Volcheck GW, et al. The risk of asthma exacerbation after stopping
low-dose inhaled corticosteroids: a systematic review and meta-analysis of randomized controlled trials. J Allergy Clin Immunol.
2013;131(3):724-9.](https://image.slidesharecdn.com/controversialinasthma20-22mar2016final-160506101203/85/Controversial-in-asthma-20-22-mar-2016-final-43-320.jpg)
![40
เอกสารประกอบการประชุมวิชาการประจาปี 2559 สมาคมสภาองค์กรโรคหืดแห่งประเทศไทย
Controversial Issues in Asthma 2016
51. van der Palen J. Peak inspiratory flow through diskus and turbuhaler, measured by means of a peak inspiratory flow meter (In-
Check DIAL). Respir Med. 2003;97(3):285-9.
52. Chien JW, Ciufo R, Novak R, Skowronski M, Nelson J, Coreno A, et al. Uncontrolled oxygen administration and respiratory
failure in acute asthma. Chest. 2000;117(3):728-33.
53. Rodrigo GJ, Rodriquez Verde M, Peregalli V, Rodrigo C. Effects of short-term 28% and 100% oxygen on PaCO2 and peak
expiratory flow rate in acute asthma: a randomized trial. Chest. 2003;124(4):1312-7.
54. Perrin K, Wijesinghe M, Healy B, Wadsworth K, Bowditch R, Bibby S, et al. Randomised controlled trial of high concentration
versus titrated oxygen therapy in severe exacerbations of asthma. Thorax. 2011;66(11):937-41.
55. Cates CJ, Welsh EJ, Rowe BH. Holding chambers (spacers) versus nebulisers for beta-agonist treatment of acute asthma.
Cochrane Database Syst Rev. 2013;9:Cd000052.
56. Hasegawa T, Ishihara K, Takakura S, Fujii H, Nishimura T, Okazaki M, et al. Duration of systemic corticosteroids in the treatment
of asthma exacerbation; a randomized study. Intern Med. 2000;39(10):794-7.
57. Jones AM, Munavvar M, Vail A, Aldridge RE, Hopkinson L, Rayner C, et al. Prospective, placebo-controlled trial of 5 vs 10 days
of oral prednisolone in acute adult asthma. Respir Med. 2002;96(11):950-4.
58. Alangari AA. Corticosteroids in the treatment of acute asthma. Ann Thorac Med. 2014;9(4):187-92.
59. Chapman KR, Verbeek PR, White JG, Rebuck AS. Effect of a short course of prednisone in the prevention of early relapse after
the emergency room treatment of acute asthma. N Engl J Med. 1991;324(12):788-94.
60. Fiel SB, Swartz MA, Glanz K, Francis ME. Efficacy of short-term corticosteroid therapy in outpatient treatment of acute bronchial
asthma. Am J Med. 1983;75(2):259-62.
61. Nowak RM, Pensler MI, Sarkar DD, Anderson JA, Kvale PA, Ortiz AE, et al. Comparison of peak expiratory flow and FEV1
admission criteria for acute bronchial asthma. Ann Emerg Med. 1982;11(2):64-9.
62. Weber EJ, Silverman RA, Callaham ML, Pollack CV, Woodruff PG, Clark S, et al. A prospective multicenter study of factors
associated with hospital admission among adults with acute asthma. Am J Med. 2002;113(5):371-8.
63. Kawamatawong T, Boonsarngsuk V, Kiatboonsri S, Promajun P. Acute Asthma Treatment Guideline implementatin -
Ramathibodi experience. Respirology. 2007;12(suppl 4):P-1-007[A144].
64. Kew KM, Kirtchuk L, Michell CI. Intravenous magnesium sulfate for treating adults with acute asthma in the emergency
department. Cochrane Database Syst Rev. 2014;5:CD010909.
65. Goodacre S, Cohen J, Bradburn M, Stevens J, Gray A, Benger J, et al. The 3Mg trial: a randomised controlled trial of
intravenous or nebulised magnesium sulphate versus placebo in adults with acute severe asthma. Health Technol Assess.
2014;18(22):1-168.
66. Lim WJ, Mohammed Akram R, Carson KV, Mysore S, Labiszewski NA, Wedzicha JA, et al. Non-invasive positive pressure
ventilation for treatment of respiratory failure due to severe acute exacerbations of asthma. Cochrane Database Syst Rev.
2012;12:CD004360.
67. Schatz M, Harden K, Forsythe A, Chilingar L, Hoffman C, Sperling W, et al. The course of asthma during pregnancy, post
partum, and with successive pregnancies: a prospective analysis. J Allergy Clin Immunol. 1988;81(3):509-17.
68. Namazy JA, Schatz M. The safety of asthma medications during pregnancy: an update for clinicians. Ther Adv Respir Dis.
2014;8(4):103-10.
69. Gluck JC, Gluck PA. Asthma controller therapy during pregnancy. Am J Obstet Gynecol. 2005;192(2):369-80.](https://image.slidesharecdn.com/controversialinasthma20-22mar2016final-160506101203/85/Controversial-in-asthma-20-22-mar-2016-final-44-320.jpg)
![41
เอกสารประกอบการประชุมวิชาการประจาปี 2559 สมาคมสภาองค์กรโรคหืดแห่งประเทศไทย
Controversial Issues in Asthma 2016
70. Berges-Gimeno MP, Simon RA, Stevenson DD. The natural history and clinical characteristics of aspirin-exacerbated respiratory
disease. Ann Allergy Asthma Immunol. 2002;89(5):474-8.
71. Szczeklik A, Stevenson DD. Aspirin-induced asthma: advances in pathogenesis, diagnosis, and management. J Allergy Clin
Immunol. 2003;111(5):913-21; quiz 22.
72. Dahlen SE, Malmstrom K, Nizankowska E, Dahlen B, Kuna P, Kowalski M, et al. Improvement of aspirin-intolerant asthma by
montelukast, a leukotriene antagonist: a randomized, double-blind, placebo-controlled trial. Am J Respir Crit Care Med.
2002;165(1):9-14.
73. Drazen JM. Asthma therapy with agents preventing leukotriene synthesis or action. Proc Assoc Am Physicians.
1999;111(6):547-59.
74. Pleskow WW, Stevenson DD, Mathison DA, Simon RA, Schatz M, Zeiger RS. Aspirin desensitization in aspirin-sensitive
asthmatic patients: clinical manifestations and characterization of the refractory period. J Allergy Clin Immunol. 1982;69(1 Pt
1):11-9.
75. Lee RU, Stevenson DD. Aspirin-exacerbated respiratory disease: evaluation and management. Allergy Asthma Immunol Res.
2011;3(1):3-10.
76. Smetana GW, Conde MV. Preoperative pulmonary update. Clin Geriatr Med. 2008;24(4):607-24, vii.
77. Tirumalasetty J, Grammer LC. Asthma, surgery, and general anesthesia: a review. J Asthma. 2006;43(4):251-4.
78. Warner DO, Warner MA, Barnes RD, Offord KP, Schroeder DR, Gray DT, et al. Perioperative respiratory complications in
patients with asthma. Anesthesiology. 1996;85(3):460-7.
79. Woods BD, Sladen RN. Perioperative considerations for the patient with asthma and bronchospasm. Br J Anaesth. 2009;103
Suppl 1:i57-65.
80. Silvanus MT, Groeben H, Peters J. Corticosteroids and inhaled salbutamol in patients with reversible airway obstruction
markedly decrease the incidence of bronchospasm after tracheal intubation. Anesthesiology. 2004;100(5):1052-7.
81. Vichitvejpaisal P, Svastdi-Xuto O, Udompunturux S. The use of nebulized salbutamol in patients with bronchospasm during
anaesthesia: a clinical trial. J Med Assoc Thai. 1991;74(9):397-403.
82. Expert Panel Report 3 (EPR-3): Guidelines for the Diagnosis and Management of Asthma-Summary Report 2007. J Allergy Clin
Immunol. 2007;120(5 Suppl):S94-138.
83. Wakim JH, Sledge KC. Anesthetic implications for patients receiving exogenous corticosteroids. AANA J. 2006;74(2):133-9.
84. Louie S, Zeki AA, Schivo M, Chan AL, Yoneda KY, Avdalovic M, et al. The asthma-chronic obstructive pulmonary disease
overlap syndrome: pharmacotherapeutic considerations. Expert Rev Clin Pharmacol. [Review]. 2013;6(2):197-219.
85. Zeki AA, Schivo M, Chan A, Albertson TE, Louie S. The Asthma-COPD Overlap Syndrome: A Common Clinical Problem in the
Elderly. J Allergy (Cairo). 2011;2011:861926.
86. Boezen HM, Schouten JP, Postma DS, Rijcken B. Distribution of peak expiratory flow variability by age, gender and smoking
habits in a random population sample aged 20-70 yrs. Eur Respir J. 1994;7(10):1814-20.
87. Gannon PF, Newton DT, Pantin CF, Burge PS. Effect of the number of peak expiratory flow readings per day on the estimation of
diurnal variation. Thorax. 1998;53(9):790-2.
88. Hetzel MR, Clark TJ. Comparison of normal and asthmatic circadian rhythms in peak expiratory flow rate. Thorax.
1980;35(10):732-8.](https://image.slidesharecdn.com/controversialinasthma20-22mar2016final-160506101203/85/Controversial-in-asthma-20-22-mar-2016-final-45-320.jpg)






![48
เอกสารประกอบการประชุมวิชาการประจาปี 2559 สมาคมสภาองค์กรโรคหืดแห่งประเทศไทย
Controversial Issues in Asthma 2016
การคัดเลือกงานวิจัยคือ เป็นผู้ป่วยโรคหืดที่อาการคงที่ มีอายุมากกว่า 12 ปี มีความรุนแรงของโรคระดับใดก็ได้
มีการใช้ยา ICS หรือ ICS ร่วมกับ long-acting beta2 agonist (LABA) เป็นงานวิจัยในรูปแบบ randomized-
controlled (RCT) ที่มีระยะเวลาการวิจัยนานอย่างน้อย 4 สัปดาห์ มีการเปรียบเทียบยา tiotropium กับยาอื่น
และมีการรายงานผลลัพธ์การรักษาอย่างน้อย 1 อย่างได้แก่ สมรรถภาพปอด เป็น primary outcome ส่วน
secondary outcome ได้แก่ การใช้ยา rescuer, asthma symptom-free days/week, คุณภาพชีวิต (Mini-
Asthma Quality of Life Questionnaire [AQLQ] total score), asthma control (Asthma Control
Questionnaire 7 (ACQ-7) total score), ACQ-7 responder rate (ประเมินโดยร้อยละของผู้ป่วยที่มีการลดลง
ของ ACQ-7 score อย่างน้อย 0.5 คะแนน), การเกิดโรคกาเริบเฉียบพลัน และผลข้างเคียง
ผลการวิจัยมี RCT 13 ชิ้นจานวนผู้ป่วยรวม 4,966 คน สามารถแบ่งแนวทางการรักษาโรคออกได้เป็น
3 กลุ่ม กลุ่มที่ 1 คือ tiotropium เสริมกับ ICS ในผู้ป่วย mild-moderate asthma กลุ่มที่ 2 คือ tiotropium
ร่วมกับ ICS เปรียบเทียบกับ LABA+ICS ในผู้ป่วย moderate asthma กลุ่มที่ 3 คือ tiotropium เสริมกับ
LABA+ICS เปรียบเทียบกับ LABA+ICS ในผู้ป่วย severe asthma ระยะเวลาการวิจัยตั้งแต่ 4-52 สัปดาห์
ส่วนใหญ่ใช้ tiotropium ในรูปแบบ soft mist inhaler (respimat) ขนาดยา 5 ไมโครกรัม มีงานวิจัย 2 ฉบับที่ใช้
ในรูปแบบอื่นในขนาดยา 18 ไมโครกรัม
ผลการวิจัยพบดังนี้ในกลุ่มที่ 1 (tiotropium เสริม ICS) มี peak expiratory flow (PEF) ตอนเช้าและ
บ่ายดีขึ้นอย่างมีนัยสาคัญ (เพิ่มขึ้น 22-24 L/min, P<.00001) peak และ trough FEV1 ดีขึ้นอย่างมีนัยสาคัญ
(peak FEV1 เพิ่มขึ้น 150 mL; P<.00001) (trough FEV 1 เพิ่มขึ้น 140 mL; P<.00001) เมื่อเปรียบเทียบกับ
ICS เพียงตัวเดียว AQLQ และ ACQ-7 total scores ดีขึ้นอย่างมีนัยสาคัญถึงแม้จะไม่ถึง minimal clinically
important difference (MCID) นอกจากนี้ยังลดจานวนผู้ป่วยที่เกิดการกาเริบเฉียบพลันโดยมี number
needed to treat = 36 ส่วน asthma symptom-free days และผลข้างเคียไม่พบความแตกต่างจาก ICS
กลุ่มที่ 2 (tiotropium + ICS เปรียบเทียบกับ LABA+ICS) พบว่า ผลลัพธ์ที่ไม่แตกต่างกันได้แก่ค่า
FEV1 ทั้ง peak และ trough, PEF ช่วงบ่าย, asthma symptom-free day, ACQ-7, จานวนผู้ป่วยที่มีโรคกาเริบ
เฉียบพลัน และผลข้างเคียง tiotropium ดีกว่า LABA ในแง่ PEF ช่วงเช้า ส่วน LABA ดีกว่า tiotropium ในแง่
การใช้ rescuer, AQLQ total score แต่ก็ไม่ถึง MCID](https://image.slidesharecdn.com/controversialinasthma20-22mar2016final-160506101203/85/Controversial-in-asthma-20-22-mar-2016-final-52-320.jpg)




![54
เอกสารประกอบการประชุมวิชาการประจาปี 2559 สมาคมสภาองค์กรโรคหืดแห่งประเทศไทย
Controversial Issues in Asthma 2016
หลักในการเลือกผู้ป่วยเพื่อรับการรักษาด้วยยา omalizumab
เนื่องจาก omalizumab ได้รับการรับรองจากองค์การอาหารและยาในสหภาพยุโรป หรือ EU ในการใช้
เป็น added on therapy ในการรักษาผู้ป่วยหืด ที่อายุมากกว่า 6 ปี ที่มี severe persistent allergic asthma ที่
มีลักษณะดังต่อไปนี้คือ8
รูป แสดงแนวทางการเลือกผู้ป่วยหืดที่สมควรได้รับการรักษาด้วยยา omalizumab8
1) เป็น atopic asthma จากผลการตรวจ allergen skin test ให้ผลบวก หรือ serum specific IgE จาก in
vitro reactivity (วิธี radioallergosorbent test [RAST] หรือ) ต่อ perennial respiratory aeroallergen ให้
ผลบวก
2) มีค่าผลการทดสอบสมรรถภาพปอดที่ได้จากวิธิสไปโรเมตรีย์มีค่าต่า (FEV1 < 80%)](https://image.slidesharecdn.com/controversialinasthma20-22mar2016final-160506101203/85/Controversial-in-asthma-20-22-mar-2016-final-58-320.jpg)








![63
เอกสารประกอบการประชุมวิชาการประจาปี 2559 สมาคมสภาองค์กรโรคหืดแห่งประเทศไทย
Controversial Issues in Asthma 2016
และแก้ไขปัจจัยที่ทาให้คุมโรคไม่ได้ เช่น patient compliance หรือ device technique หรือการรักษาโรคพบ
ร่วมของโรคหืดเช่น allergic rhinitis อย่งเต็มที่ก่อน และการประเมินผลการตอบสนองที่ 16 สัปดาห์ ด้วย
objective measurement นั้นมีความสาคัญอย่างยิ่ง เพื่อพิจารณา ในการใช้ยา ดังกล่าวที่ราคาแพง อย่าง
ต่อเนื่องในระยะยาว สาหรับผู้ป่วยหืด ในบริบทของประเทศไทย ที่มีข้อจากัดเรื่องงบประมาณ และการเข้าถึง
ยาดังกล่าวจากระบบบริการสุขภาพ รวมทั้งการกาหนดแนวทางการใช้ยาที่เหมาะสมในระดับประเทศ เพื่อให้
เป็นไปในแนวทางปฏิบัติที่สอดคล้องกัน อันจะทาให้การรักษาผู้ป่วยด้วยยาดังกล่าวเกิดประสิทธิผลสูงสุด
เอกสารอ้างอิง
3) Presta LG, Lahr SJ, Shields RL, Porter JP, Gorman CM, Fendly BM, et al. Humanization of an antibody
directed against IgE. J Immunol. 1993;151(5):2623-32.
4) Pelaia G, Gallelli L, Renda T, Romeo P, Busceti MT, Grembiale RD, et al. Update on optimal use of
omalizumab in management of asthma. J Asthma Allergy. 2011;4:49-59.
5) Presta L, Shields R, O'Connell L, Lahr S, Porter J, Gorman C, et al. The binding site on human
immunoglobulin E for its high affinity receptor. J Biol Chem. 1994;269(42):26368-73.
6) Spector S. Omalizumab: efficacy in allergic disease. Panminerva Med. 2004;46(2):141-8.
7) Holgate S, Casale T, Wenzel S, Bousquet J, Deniz Y, Reisner C. The anti-inflammatory effects of omalizumab
confirm the central role of IgE in allergic inflammation. J Allergy Clin Immunol. 2005;115(3):459-65.
8) Price D. The use of omalizumab in asthma. Prim Care Respir J. 2008;17(2):62-72.
9) GINA. Global strategy for asthma management and prevention 2011. Global Initiative for Asthma 2011 [cited
2012 Jan 2012]; Available from: http://www.ginasthma.org/guidelines-gina-report-global-strategy-for-
asthma.html.
10) Holgate S, Buhl R, Bousquet J, Smith N, Panahloo Z, Jimenez P. The use of omalizumab in the treatment of
severe allergic asthma: A clinical experience update. Respir Med. 2009;103(8):1098-113.
11) Hochhaus G, Brookman L, Fox H, Johnson C, Matthews J, Ren S, et al. Pharmacodynamics of omalizumab:
implications for optimised dosing strategies and clinical efficacy in the treatment of allergic asthma. Curr Med
Res Opin. 2003;19(6):491-8.
12) Ledford DK. Omalizumab: overview of pharmacology and efficacy in asthma. Expert Opin Biol Ther.
2009;9(7):933-43.](https://image.slidesharecdn.com/controversialinasthma20-22mar2016final-160506101203/85/Controversial-in-asthma-20-22-mar-2016-final-67-320.jpg)

















![84
เอกสารประกอบการประชุมวิชาการประจาปี 2559 สมาคมสภาองค์กรโรคหืดแห่งประเทศไทย
Controversial Issues in Asthma 2016
เอกสารอ้างอิง
1. GINA. Global strategy for asthma management and prevention 2014. Global Initiative for Asthma 2014 [cited
2014 June 2014]; Available from: http://www.ginasthma.org/guidelines-gina-report-global-strategy-for-
asthma.html.
2. Salvi SS, Barnes PJ. Chronic obstructive pulmonary disease in non-smokers. Lancet 2009;374(9691):733-43.
3. Global Strategy for Diagnosis, Management, and Prevention of COPD 2013. Global Initiative for Chronic
Obstructive Lung Disease (GOLD) 2013; 2013 [cited 2013 September 2013]; Available from:
http://www.goldcopd.org/guidelines-global-strategy-for-diagnosis-management.html.
4. Antoniu SA. UPLIFT Study: the effects of long-term therapy with inhaled tiotropium in chronic obstructive
pulmonary disease. Evaluation of: Tashkin DP, Celli B, Senn S et al.: a 4-year trial of tiotropium in chronic
obstructive pulmonary disease. N Engl J Med (2008) 359(15):1543-1554. Expert Opin Pharmacother.
2009;10(4):719-22.
5. Louie S, Zeki AA, Schivo M, Chan AL, Yoneda KY, Avdalovic M, et al. The asthma-chronic obstructive
pulmonary disease overlap syndrome: pharmacotherapeutic considerations. Expert Rev Clin Pharmacol.
2013;6(2):197-219.
6. Zeki AA, Schivo M, Chan A, Albertson TE, Louie S. The Asthma-COPD Overlap Syndrome: A Common
Clinical Problem in the Elderly. J Allergy (Cairo). 2011;2011:861926.
7. Soler-Cataluna JJ, Cosio B, Izquierdo JL, Lopez-Campos JL, Marin JM, Aguero R, et al. Consensus
document on the overlap phenotype COPD-asthma in COPD. Arch Bronconeumol. 2012;48(9):331-7.
8. Gibson PG, Simpson JL. The overlap syndrome of asthma and COPD: what are its features and how
important is it? Thorax. 2009;64(8):728-35.
9. Kauppi P, Kupiainen H, Lindqvist A, Tammilehto L, Kilpelainen M, Kinnula VL, et al. Overlap syndrome of
asthma and COPD predicts low quality of life. J Asthma. 2011;48(3):279-85.
10. Contoli M, Baraldo S, Marku B, Casolari P, Marwick JA, Turato G, et al. Fixed airflow obstruction due to
asthma or chronic obstructive pulmonary disease: 5-year follow-up. J Allergy Clin Immunol. 2010;125(4):830-
7.
11. Hardin M, Silverman EK, Barr RG, Hansel NN, Schroeder JD, Make BJ, et al. The clinical features of the
overlap between COPD and asthma. Respir Res. 2011;12:127.
12. Blanchette CM, Gutierrez B, Ory C, Chang E, Akazawa M. Economic burden in direct costs of concomitant
chronic obstructive pulmonary disease and asthma in a Medicare Advantage population. J Manag Care
Pharm. 2008;14(2):176-85.](https://image.slidesharecdn.com/controversialinasthma20-22mar2016final-160506101203/85/Controversial-in-asthma-20-22-mar-2016-final-88-320.jpg)











![97
เอกสารประกอบการประชุมวิชาการประจาปี 2559 สมาคมสภาองค์กรโรคหืดแห่งประเทศไทย
Controversial Issues in Asthma 2016
เอกสารอ้างอิง
1. Martinez FD, Wright AL, Taussig LM, Holberg CJ, Halonen M, Morgan WJ. Asthma and wheezing in the first
six years of life. The Group Health Medical Associates. N Engl J Med. 1995;332(3):133-8.
2. Morgan WJ, Stern DA, Sherrill DL, Guerra S, Holberg CJ, Guilbert TW, et al. Outcome of asthma and
wheezing in the first 6 years of life: follow-up through adolescence. Am J Respir Crit Care Med.
2005;172(10):1253-8.
3. Grad R, Morgan WJ. Long-term outcomes of early-onset wheeze and asthma. J Allergy Clin Immunol.
2012;130(2):299-307.
4. Castro-Rodriguez JA, Holberg CJ, Wright AL, Martinez FD. A clinical index to define risk of asthma in young
children with recurrent wheezing. Am J Respir Crit Care Med. 2000;162(4 Pt 1):1403-6.
5. Leonardi NA, Spycher BD, Strippoli MP, Frey U, Silverman M, Kuehni CE. Validation of the Asthma Predictive
Index and comparison with simpler clinical prediction rules. J Allergy Clin Immunol. 2011;127(6):1466-72 e6.
6. Guilbert TW, Morgan WJ, Krawiec M, Lemanske RF, Jr., Sorkness C, Szefler SJ, et al. The Prevention of Early
Asthma in Kids study: design, rationale and methods for the Childhood Asthma Research and Education
network. Control Clin Trials. 2004;25(3):286-310.
7. Chang TS, Lemanske RF, Jr., Guilbert TW, Gern JE, Coen MH, Evans MD, et al. Evaluation of the modified
asthma predictive index in high-risk preschool children. J Allergy Clin Immunol Pract. 2013;1(2):152-6.
8. Amin P, Levin L, Epstein T, Ryan P, LeMasters G, Khurana Hershey G, et al. Optimum predictors of childhood
asthma: persistent wheeze or the Asthma Predictive Index? J Allergy Clin Immunol Pract. 2014;2(6):709-15.
9. Bacharier LB. The recurrently wheezing preschool child-benign or asthma in the making? Ann Allergy Asthma
Immunol 2015;115(6):463-70.
10. Kurukulaaratchy RJ, Matthews S, Holgate ST, Arshad SH. Predicting persistent disease among children who
wheeze during early life. Eur Respir J. 2003;22(5):767-71.
11. Caudri D, Wijga A, CM AS, Hoekstra M, Postma DS, Koppelman GH, et al. Predicting the long-term prognosis
of children with symptoms suggestive of asthma at preschool age. J Allergy Clin Immunol. 2009;124(5):903-
10 e1-7.
12. Pescatore AM, Dogaru CM, Duembgen L, Silverman M, Gaillard EA, Spycher BD, et al. A simple asthma
prediction tool for preschool children with wheeze or cough. J Allergy Clin Immunol. 2014;133(1):111-8 e1-13.
13. Klaassen EM, van de Kant KD, Jobsis Q, van Schayck OC, Smolinska A, Dallinga JW, et al. Exhaled
biomarkers and gene expression at preschool age improve asthma prediction at 6 years of age. Am J Respir
Crit Care Med. 2015;191(2):201-7.
14. Global initiative for asthma. Global strategy for asthma management and prevention (2015 update). 2015
[updated April 1, 2015]; Available from: http://www.ginasthma.org.](https://image.slidesharecdn.com/controversialinasthma20-22mar2016final-160506101203/85/Controversial-in-asthma-20-22-mar-2016-final-101-320.jpg)






![104
เอกสารประกอบการประชุมวิชาการประจาปี 2559 สมาคมสภาองค์กรโรคหืดแห่งประเทศไทย
Controversial Issues in Asthma 2016
airway obstruction มากกว่า43
นอกจากนั้นยังอาจนามาใช้ประเมินประสิทธิภาพของยาขยายหลอดลมแต่
ละชนิดเช่น salmeterol กับ tiotropium ในกรณีที่มีค่า FEV1 ใกล้เคียงกัน44
รวมทั้ง bronchodilation
effect ที่มีต่อผู้ป่วยโรคหืดหลังพ่นยาขยายหลอดลม45
ค่า IOS parameters ที่ได้จากการวัดระหว่างการ
กระตุ้นหลอดลมของผู้ป่วยโรคหืดด้วย methacholine จะสัมพันธ์กับอาการ chest tightness และ
dyspnea ที่เกิดขึ้นระหว่างการกระตุ้นมากกว่า spirometry ยกเว้นอาการ wheeze46
2. Lung clearance index (LCI)
ได้มาจาก concentration curve ของ multiple-breath N2 washout มีการนามาใช้เป็น early
small airway marker การศึกษาเร็วๆนี้ศึกษากับผู้ป่วยโรคหืดที่ได้รับการทา bronchoprovocation พบว่า
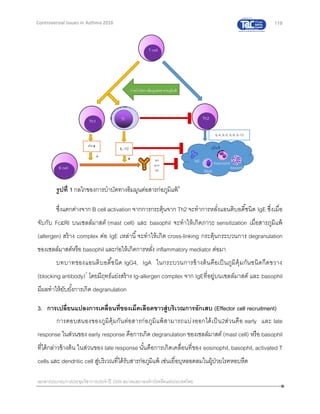
ค่า LCI มีความสัมพันธ์โดยตรงกับ convection (Scond) และ diffusion-dependent ventilation
heterogeneity (Sacin)47
ดังนั้นการใช้ markers ทั้งสามอย่างร่วมกัน จะช่วยบอกว่าผู้ป่วยโรคหืดมี
ventilation heterogeneity (เป็นการบอก degree of small airway obstruction) ได้ดีกว่าการใช้ markers
อย่างใดอย่างหนึ่ง เพราะ LCI, Scond , Sacin อย่างใดอย่างหนึ่ง อาจ detect ventilation heterogeneity ได้
ไม่สมบูรณ์
3. Ventilation heterogeneity
อาศัยวิธีการตรวจ multiple-breath N2 washout (MBW) ทาให้สามารถวัด ventilation
distribution ใน conductive และ acinar spaces ขั้นตอนการตรวจ MBW ทาโดยให้ผู้ตรวจหายใจ
สม่าเสมอให้ได้ tidal volume 1 L โดยเริ่มหายใจเข้าตั้งต้นจาก functional residual capacity (FRC)
ผู้ตรวจจะหายใจเข้าเอา 100% oxygen จาก inspiratory bag เมื่อหายใจเข้าออกประมาณ 20-25 ครั้ง
หลังจากนั้นจะให้ผู้ตรวจหายใจออกเต็มที่จนถึง residual volume อากาศหายใจออกมาแต่ละครั้งจนถึง
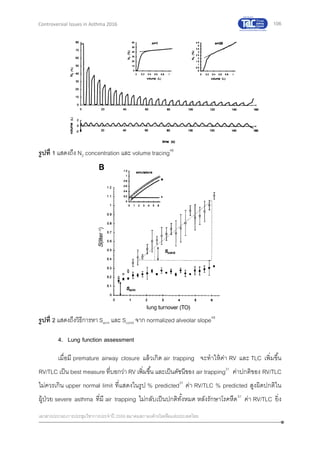
เหลือปริมาตรปอดที่ FRC จะทาให้มี progressive N2 dilution เมื่อนา N2 concentration tracing (รูปที่ 1)
มา plot graph ให้อยู่ในรูป semi- logarithmic scale เราเรียกว่า N2-washout curve ค่าที่นามาสร้าง
graph คือ % ของ mean expired N2 concentration ของแต่ละ breath เทียบกับ initial N2 concentration
ในปอด N2-washout curve จะมี y-axis แสดงค่า log[N2] เทียบกับ x-axis แสดงค่า lung turnover
(expired volume/FRC) การใช้ค่า lung turnover เพื่อเป็นการตัดปัญหาของ different lung volume และ
dilution ของผู้ตรวจแต่ละราย การตรวจ MBW ทาให้ทราบ normalized alveolar slope (S) (คาณวนจาก](https://image.slidesharecdn.com/controversialinasthma20-22mar2016final-160506101203/85/Controversial-in-asthma-20-22-mar-2016-final-108-320.jpg)














































![156
เอกสารประกอบการประชุมวิชาการประจาปี 2559 สมาคมสภาองค์กรโรคหืดแห่งประเทศไทย
Controversial Issues in Asthma 2016
1. แนะนาให้ทาสไปโรเมตรีย์ (spirometry) ในรายที่สงสัยโรคหลอดลม2
เพื่อค้นหาภาวะหลอดลมตีบ (airway
obstruction)3
(Level of evidence 2, Grade of recommendation ++) [รายละเอียดในภาคผนวก]
2. การวัดค่า peak expiratory flow rate (PEFR) ก่อนและภายหลังการให้สูดยาขยายหลอดลมชนิดออกฤทธิ์
สั้น เพียงครั้งเดียวไม่แนะนาให้ทาเนื่องจากไม่แน่นอนเที่ยงตรงเมื่อเทียบกับค่า forced expiratory volume ใน
เวลา 1 วินาที (FEV1) ในการวินิจฉัยภาวะหลอดลมตีบ12
(Level of evidence 2, Grade of recommendation
+/-) แต่การใช้ serial PEFR ในกรณีที่สงสัยโรคหืด ยังไม่มีการศึกษาเพียงพอที่จะแนะนาให้ทาในผู้ป่วยที่มี
อาการไอเรื้อรัง (Level of evidence 4, Grade of recommendation +/-) [ดูจากแนวทางปฏิบัติโรคหืด พ.ศ.
2550]
3.3.2 ระดับทุติยภูมิ (Secondary care) แนะนาให้ทาในกรณีที่มีผู้เชี่ยวชาญ ได้แก่
3.3.2.1 Bronchoprovocative test เป็นการทดสอบความไวหลอดลม (airway hyperresponsiveness, AHR)
แนะนาให้ทาในกรณีที่ผลการตรวจสไปโรเมตรีย์ปกติและสงสัยภาวะหลอดลมไวเกิน เนื่องจากผลสไปโรเมตรีย์
ที่ปกติยังไม่สามารถตัดสาเหตุอาการไอที่เกิดจาก asthma ได้2,13
การทดสอบความไวหลอดลม ทาได้โดยวิธี
methacholine challenge test หากผลการตรวจ methacholine challenge test เป็นผลลบ สามารถตัดการ
วินิจฉัยโรคหืดออกไปได้ถ้าผู้ป่วยไม่เคยได้รับยาสูดคอร์ติโคสเตียรอยด์มาก่อน14
(Level of evidence 2,
Grade of recommendation +)
3.3.2.2 เอกซเรย์คอมพิวเตอร์ปอด (High-resolution computed tomography, HRCT) ในกรณีที่สงสัยโรค
หลอดลมโป่งพอง (bronchiectasis), โรค interstitial lung diseases หรือหลอดลมขนากเล็กอักเสบ
(bronchiolitis) ที่ผลการตรวจภาพรังสีทรวงอกปกติ3
(Level of evidence 3, Grade of recommendation+)
3.3.2.3 Indirect laryngoscopy เพื่อค้นหาหลักฐานของ laryngopharyngeal reflux แนะนาให้ทาในกรณีที่มี
ผู้เชี่ยวชาญทางหู คอ จมูก (ENT)3
(Level of evidence 1, Grade of recommendation ++)
3.3.2.4 เอกซเรย์คอมพิวเตอร์ไซนัส (computerized tomography paranasal sinus) ไม่แนะนาให้ส่งตรวจ
เอกซเรย์คอมพิวเตอร์ไซนัส ในการตรวจเบื้องต้น9
(Level of evidence 2, Grade of recommendation -)
แนะนาให้ทาเฉพาะในรายที่จะได้ทาการผ่าตัดไซนัส หรือมีภาวะแทรกซ้อนชนิดร้ายแรง เช่นภาวะแทรกซ้อน
ทางตา และสมอง และในผู้ที่ไม่ตอบสนองต่อการรักษาด้วยยา4
(Level of evidence 3, Grade of
recommendation ++)](https://image.slidesharecdn.com/controversialinasthma20-22mar2016final-160506101203/85/Controversial-in-asthma-20-22-mar-2016-final-160-320.jpg)








































![197
เอกสารประกอบการประชุมวิชาการประจาปี 2559 สมาคมสภาองค์กรโรคหืดแห่งประเทศไทย
Controversial Issues in Asthma 2016
ประสิทธิภาพ47
และอาจช่วยป้ องกันการเกิดโรคหืดได้ในเด็กที่เป็นโรคเยื่อบุจมูกอักเสบจากภูมิแพ้ (allergic
rhinitis, AR) โดยข้อมูลการศึกษาของ Jacobsen L และคณะ (the PAT study) ที่ทาการศึกษาในเด็กที่เป็น
AR อายุ 6-14 ปี จานวน 205 คน ที่ได้รับการทา SCIT (birch และ/หรือ grass pollen) เป็นเวลาต่อเนื่อง 3 ปี
แล้วติดตามผู้ป่วยกลุ่มดังกล่าวไปอีก 7 ปี หลังหยุด SCIT เปรียบเทียบกับกลุ่มควบคุม พบว่ากลุ่มที่ได้รับการ
รักษาด้วย SIT เกิดเป็นโรคหืดน้อยกว่าอย่างมีนัยสาคัญทางสถิติ โดยมีค่า odds ratio ในการป้ องกันการเกิด
โรคหืดเท่ากับ 4.6 ดังนั้น SCIT จึงเป็นวิธีการป้ องกันการเกิดโรคหืดอีกวิธีหนึ่งในผู้ป่วยที่เป็นกลุ่มเสี่ยงหรือกลุ่ม
ที่มีอาการแสดงของ AR แล้ว
โดยสรุป การป้ องกันการเกิดโรคหืดด้วยวิธีการต่างๆ จนถึงปัจจุบัน ยังไม่มีวิธีใดเป็นวิธีที่ดีที่สุด
เนื่องจากยังไม่มีหลักฐานข้อมูลเชิงลึกที่มากเพียงพอในการนามาประยุกต์ใช้ทั่วไปทางคลินิก แต่จากข้อมูล
การศึกษาที่ผ่านมาบ่งชี้ให้เห็นว่า การป้ องกันการเกิดโรคหืดนั้นเป็นไปได้ เพียงแต่ยังคงต้องการความรู้ความ
เข้าใจถึงความสัมพันธ์ของปัจจัยทางด้านพันธุกรรมและปัจจัยทางด้านสิ่งแวดล้อมที่ส่งผลต่อการเกิดโรคหืด
ตลอดจนกระบวนการการเกิดโรคหืดและ biomarkers ของโรคหืดอย่างละเอียด เพื่อนาไปสู่การศึกษาค้นคว้า
ถึงวิธีการป้ องกันการเกิดโรคหืดได้อย่างมีประสิทธิภาพในอนาคต
เอกสารอ้างอิง
1. Masoli M, Fabian D, Holt S, Beasley R. The global burden of asthma: executive summary of the GINA
Dissemination Committee report. Allergy. 2004;59(5):469-78.
2. Global initiative for asthma. Global strategy for asthma management and prevention (updated 2010). 2010
[updated Febuary 1, 2016]; Available from: http://www.ginasthma.org.
3. Asher MI, Montefort S, Bjorksten B, Lai CK, Strachan DP, Weiland SK, et al. Worldwide time trends in the
prevalence of symptoms of asthma, allergic rhinoconjunctivitis, and eczema in childhood: ISAAC Phases One
and Three repeat multicountry cross-sectional surveys. Lancet. 2006;368(9537):733-43.
4. Jackson DJ, Hartert TV, Martinez FD, Weiss ST, Fahy JV. Asthma: NHLBI Workshop on the Primary Prevention
of Chronic Lung Diseases. Ann Am Thorac Soc. 2014;11 Suppl 3:S139-45.
5. Moffatt MF, Gut IG, Demenais F, Strachan DP, Bouzigon E, Heath S, et al. A large-scale, consortium-based
genomewide association study of asthma. N Engl J Med. 2010;363(13):1211-21.](https://image.slidesharecdn.com/controversialinasthma20-22mar2016final-160506101203/85/Controversial-in-asthma-20-22-mar-2016-final-201-320.jpg)











![210
เอกสารประกอบการประชุมวิชาการประจาปี 2559 สมาคมสภาองค์กรโรคหืดแห่งประเทศไทย
Controversial Issues in Asthma 2016
2. Omalizumab มีรายงานของผู้ป่วยที่ได้รับการรักษาด้วย omalizumab แล้วตอบสนองต่อการ
รักษาที่ดี ซึ่งในรายงานผู้ป่วยมีโรคหืด (asthma)ร่วมด้วยและมี skin test เป็นบวกต่อ specific allergen
ร่วมกับได้รับ oral corticocorticoid เป็นเวลานาน64-66
สรุป
Chronic eosinophilic pneumonia เป็นโรคที่พบน้อยซึ่งผู้ป่วยมักมีโรคหืด (asthma) หรือ atopic
disease นามาก่อน และพบในช่วงอายุ 30-40 ปี การวินิจฉัยอาศัยประวัติ ตรวจร่างกายและผลตรวจทาง
ห้องปฏิบัติการ การพบภาพถ่ายรังสีทรวงอกที่มีลักษณะของ peripheral infiltration หรือ photonegative of
pulmonary edema ร่วมกับ blood eosinophilia ซึ่ง ผล bronchoalveolar lavage มีสัดส่วนของ eosinophils
สูงมากขึ้นโดยมากกว่าร้อยละ 25 ของเม็ดเลือดขาวทั้งหมด โดยต้องวินิจฉัยแยกภาวะอื่นที่ทาให้มี
eosinophilic pneumonia กรณีที่ผลตรวจมีการขัดแย้งดังกล่าวมาแล้ว การวินิจฉัยจาเป็นต้องใช้
histopathology ซึ่งส่วนใหญ่จะได้จาก open lung biopsy การรักษาที่สาคัญคือ systemic corticosteroid
และค่อยๆลดขนาดลงในระยะเวลา 6-12 เดือนและหลังจากหยุด systemic corticosteroid ต้องเฝ้ าระวังการ
กลับมาเป็นซ้า(relapse) ของโรค
เอกสารอ้างอิง
1. Wechsler ME. Pulmonary eosinophilic syndromes. Immunol Allergy Clin North Am. 2007;27(3):477-92.
2. Bhatt NY, Allen JN. Update on eosinophilic lung diseases. Semin Respir Crit Care Med. 2012;33(5):555-71.
3. Allen JN, Davis WB. Eosinophilic lung diseases. Am J Respir Crit Care Med. 1994;150(5):1423-38.
4. Sveinsson OA, Isaksson HJ, Gudmundsson G. [Chronic eosinophilic pneumonia in Iceland: clinical features,
epidemiology and review]. Laeknabladid. 2007;93(2):111-6.
5. Jederlinic PJ, Sicilian L, Gaensler EA. Chronic eosinophilic pneumonia. A report of 19 cases and a review of
the literature. Medicine (Baltimore). 1988;67(3):154-62.
6. Marchand E, Reynaud-Gaubert M, Lauque D, Durieu J, Tonnel AB, Cordier JF. Idiopathic chronic eosinophilic
pneumonia. A clinical and follow-up study of 62 cases. The Groupe d'Etudes et de Recherche sur les
Maladies "Orphelines" Pulmonaires (GERM"O"P). Medicine (Baltimore). 1998;77(5):299-312.
7. Fox B, Seed WA. Chronic eosinophilic pneumonia. Thorax. 1980;35(8):570-80.
8. Naughton M, Fahy J, FitzGerald MX. Chronic eosinophilic pneumonia. A long-term follow-up of 12 patients.
Chest. 1993;103(1):162-5.](https://image.slidesharecdn.com/controversialinasthma20-22mar2016final-160506101203/85/Controversial-in-asthma-20-22-mar-2016-final-214-320.jpg)
![211
เอกสารประกอบการประชุมวิชาการประจาปี 2559 สมาคมสภาองค์กรโรคหืดแห่งประเทศไทย
Controversial Issues in Asthma 2016
9. Marchand E, Etienne-Mastroianni B, Chanez P, Lauque D, Leclerc P, Cordier JF. Idiopathic chronic
eosinophilic pneumonia and asthma: how do they influence each other? Eur Respir J. 2003;22(1):8-13.
10. Ivanick MJ, Donohue JF. Chronic eosinophilic pneumonia: a cause of adult respiratory distress syndrome.
South Med J. 1986;79(6):686-90.
11. Libby DM, Murphy TF, Edwards A, Gray G, King TK. Chronic eosinophilic pneumonia: an unusual cause of
acute respiratory failure. Am Rev Respir Dis. 1980;122(3):497-500.
12. Jeong YJ, Kim KI, Seo IJ, Lee CH, Lee KN, Kim KN, et al. Eosinophilic lung diseases: a clinical, radiologic,
and pathologic overview. Radiographics. 2007;27(3):617-37; discussion 37-9.
13. Bartter T, Irwin RS, Nash G, Balikian JP, Hollingsworth HH. Idiopathic bronchiolitis obliterans organizing
pneumonia with peripheral infiltrates on chest roentgenogram. Arch Intern Med. 1989;149(2):273-9.
14. Glazer HS, Levitt RG, Shackelford GD. Peripheral pulmonary infiltrates in sarcoidosis. Chest. 1984;86(5):741-
4.
15. Mayo JR, Muller NL, Road J, Sisler J, Lillington G. Chronic eosinophilic pneumonia: CT findings in six cases.
AJR Am J Roentgenol. 1989;153(4):727-30.
16. Carrington CB, Addington WW, Goff AM, Madoff IM, Marks A, Schwaber JR, et al. Chronic Eosinophilic
Pneumonia. New England Journal of Medicine. 1969;280(15):787-98.
17. Samman YS, Wali SO, Abdelaal MA, Gangi MT, Krayem AB. Chronic eosinophilic pneumonia presenting with
recurrent massive bilateral pleural effusion : case report. Chest. 2001;119(3):968-70.
18. Marchand E, Cordier J. Idiopathic chronic eosinophilic pneumonia. Orphanet J Rare Dis. 2006;1:11.
19. Olopade CO, Crotty TB, Douglas WW, Colby TV, Sur S. Chronic eosinophilic pneumonia and idiopathic
bronchiolitis obliterans organizing pneumonia: comparison of eosinophil number and degranulation by
immunofluorescence staining for eosinophil-derived major basic protein. Mayo Clin Proc. 1995;70(2):137-42.
20. d'Amours P, Leblanc P, Boulet LP. Chronic eosinophilic pneumonia associated with thrombocytosis and
pleural effusion. CMAJ. 1990;142(8):837-9.
21. Nishimori M, Tsunemine H, Maruoka H, Itoh K, Kodaka T, Matsuoka H, et al. Marked Thrombocytosis in
Chronic Eosinophilic Pneumonia and Analysis of Cytokine Mechanism. J Clin Exp Hematop. 2015;55(2):97-
102.
22. Brezis M, Lafair J. Thrombocytosis in chronic eosinophilic pneumonia. Chest. 1979;76(2):231-2.
23. Taniguchi H, Kadota J, Abe K, Matsubara Y, Kaseda M, Kawamoto S, et al. [Eosinophilic pneumonia without
eosinophilia in BALF or peripheral blood and diagnosed by open lung biopsy]. Nihon Kokyuki Gakkai Zasshi.
1999;37(10):796-801.
24. Matsuse H, Shimoda T, Fukushima C, Matsuo N, Sakai H, Takao A, et al. Diagnostic problems in chronic
eosinophilic pneumonia. J Int Med Res. 1997;25(4):196-201.](https://image.slidesharecdn.com/controversialinasthma20-22mar2016final-160506101203/85/Controversial-in-asthma-20-22-mar-2016-final-215-320.jpg)

![213
เอกสารประกอบการประชุมวิชาการประจาปี 2559 สมาคมสภาองค์กรโรคหืดแห่งประเทศไทย
Controversial Issues in Asthma 2016
41. Silva CI, Muller NL, Fujimoto K, Johkoh T, Ajzen SA, Churg A. Churg-Strauss syndrome: high resolution CT
and pathologic findings. J Thorac Imaging. 2005;20(2):74-80.
42. Choi YH, Im J-G, Han BK, Kim J-H, Lee KY, Myoung NH. Thoracic Manifestation of Churg-Strauss Syndrome:
Radiologic and Clinical Findings. Chest. 2000;117(1):117-24.
43. Talmadge E King J, Flaherty KR, Glassock RJ, Bochner BS, Hollingsworth H. Clinical features and diagnosis
of eosinophilic granulomatosis with polyangiitis (Churg-Strauss). [updated Oct 15, 2015]; Available from:
http://www.uptodate.com/contents/clinical-features-and-diagnosis-of-eosinophilic-granulomatosis-with-
polyangiitis-churg-strauss.
44. Guillevin L, Cohen P, Gayraud M, Lhote F, Jarrousse B, Casassus P. Churg-Strauss syndrome. Clinical study
and long-term follow-up of 96 patients. Medicine (Baltimore). 1999;78(1):26-37.
45. Katzenstein AL. Diagnostic features and differential diagnosis of Churg-Strauss syndrome in the lung. A
review. Am J Clin Pathol. 2000;114(5):767-72.
46. Churg A. Recent advances in the diagnosis of Churg-Strauss syndrome. Mod Pathol. 2001;14(12):1284-93.
47. Lie JT. Illustrated histopathologic classification criteria for selected vasculitis syndromes. American College of
Rheumatology Subcommittee on Classification of Vasculitis. Arthritis Rheum. 1990;33(8):1074-87.
48. Durieu J, Wallaert B, Tonnel AB. [Chronic eosinophilic pneumonia or Carrington's disease]. Rev Mal Respir.
1993;10(6):499-507.
49. Shah A, Panjabi C. Allergic aspergillosis of the respiratory tract. Eur Respir Rev. 2014;23(131):8-29.
50. Patterson K, Strek ME. Allergic Bronchopulmonary Aspergillosis. Proceedings of the American Thoracic
Society. 2010;7(3):237-44.
51. Kim PW, Sorbello AF, Wassel RT, Pham TM, Tonning JM, Nambiar S. Eosinophilic pneumonia in patients
treated with daptomycin: review of the literature and US FDA adverse event reporting system reports. Drug
Saf. 2012;35(6):447-57.
52. Klion AD, Baltimore, Weller PF, Bochner BS, Hollingsworth H. Causes of pulmonary eosinophilia. [updated
Apr 03, 2014]; Available from: http://www.uptodate.com/contents/causes-of-pulmonary-eosinophilia.
53. Jeong YJ, Kim K-I, Seo IJ, Lee CH, Lee KN, Kim KN, et al. Eosinophilic Lung Diseases: A Clinical, Radiologic,
and Pathologic Overview. Radiographics. 2007;27(3):617-37.
54. Singh P, Saggar K, Kalia V, Sandhu P, Galhotra RD. Thoracic imaging findings in a case of disseminated
cysticercosis. Postgrad Med J. 2011;87(1024):158-9.
55. Fauci AS, Harley JB, Roberts WC, Ferrans VJ, Gralnick HR, Bjornson BH. NIH conference. The idiopathic
hypereosinophilic syndrome. Clinical, pathophysiologic, and therapeutic considerations. Ann Intern Med.
1982;97(1):78-92.
56. Weller P, Bubley G. The idiopathic hypereosinophilic syndrome. Blood. 1994;83(10):2759-79.](https://image.slidesharecdn.com/controversialinasthma20-22mar2016final-160506101203/85/Controversial-in-asthma-20-22-mar-2016-final-217-320.jpg)
![214
เอกสารประกอบการประชุมวิชาการประจาปี 2559 สมาคมสภาองค์กรโรคหืดแห่งประเทศไทย
Controversial Issues in Asthma 2016
57. Slabbynck H, Impens N, Naegels S, Dewaele M, Schandevyl W. Idiopathic hypereosinophilic syndrome-
related pulmonary involvement diagnosed by bronchoalveolar lavage. Chest. 1992;101(4):1178-80.
58. Spry CJ, Davies J, Tai PC, Olsen EG, Oakley CM, Goodwin JF. Clinical features of fifteen patients with the
hypereosinophilic syndrome. Q J Med. 1983;52(205):1-22.
59. Brown KK, Talmadge E King J, Flaherty KR, Hollingsworth H. Chronic eosinophilic pneumonia. [updated
April 14, 2015]; Available from: http://www.uptodate.com/contents/chronic-eosinophilic-pneumonia.
60. Ebara H, Ikezoe J, Johkoh T, Kohno N, Takeuchi N, Kozuka T, et al. Chronic eosinophilic pneumonia:
evolution of chest radiograms and CT features. J Comput Assist Tomogr. 1994;18(5):737-44.
61. Lavandier M, Carre P. Effectiveness of inhaled high-dose corticosteroid therapy in chronic eosinophilic
pneumonia. Chest. 1994;105(6):1913-4.
62. Fujimori K, Shimatsu Y, Suzuki E, Arakawa M, Gejyo F. [Chronic eosinophilic pneumonia complicated by
bronchial asthma and diabetes mellitus successfully treated with suplatast tosilate and high-dose inhaled
corticosteroid therapy]. Nihon Kokyuki Gakkai Zasshi. 1999;37(11):903-8.
63. Minakuchi M, Niimi A, Matsumoto H, Amitani R, Mishima M. Chronic eosinophilic pneumonia: treatment with
inhaled corticosteroids. Respiration. 2003;70(4):362-6.
64. Shin YS, Jin HJ, Yoo HS, Hwang EK, Nam YH, Ye YM, et al. Successful treatment of chronic eosinophilic
pneumonia with anti-IgE therapy. J Korean Med Sci. 2012;27(10):1261-4.
65. Kaya H, Gumus S, Ucar E, Aydogan M, Musabak U, Tozkoparan E, et al. Omalizumab as a steroid-sparing
agent in chronic eosinophilic pneumonia. Chest. 2012;142(2):513-6.
66. Domingo C, Pomares X. Can omalizumab be effective in chronic eosinophilic pneumonia? Chest.
2013;143(1):274.](https://image.slidesharecdn.com/controversialinasthma20-22mar2016final-160506101203/85/Controversial-in-asthma-20-22-mar-2016-final-218-320.jpg)































![253
เอกสารประกอบการประชุมวิชาการประจาปี 2559 สมาคมสภาองค์กรโรคหืดแห่งประเทศไทย
Controversial Issues in Asthma 2016
เอกสารอ้างอิง
1. GINA. Global strategy for asthma management and prevention 2014 [online]. Available at:
http://www.ginasthma.org/guidelines-gina-report-global-strategy-for-asthma.html. Accessed June 2014.
2. Reddel HK, Taylor DR, Bateman ED, Boulet LP, Boushey HA, Busse WW, et al. An official American Thoracic
Society/European Respiratory Society statement: asthma control and exacerbations: standardizing endpoints
for clinical asthma trials and clinical practice. Am J Respir Crit Care Med. 2009;180:59-99.
3. Taylor DR, Bateman ED, Boulet LP, Boushey HA, Busse WW, Casale TB, et al. A new perspective on
concepts of asthma severity and control. Eur Respir J. 2008;32:545-54.
4. Levy ML, Thomas M, Small I, Pearce L, Pinnock H, Stephenson P. Summary of the 2008 BTS/SIGN British
Guideline on the management of asthma. Prim Care Respir J. 2009;18 Suppl 1:S1-16.
5. NICE. National Institute for Health and Care Excellence (NICE) Guideline. Quality Standard for asthma
[online]. Available at: http://www.nice.org.uk/guidance/qs25/chapter/quality-statement-11-difficult-asthma.
Accessed June 2014.
6. Proceedings of the ATS workshop on refractory asthma: current understanding, recommendations, and
unanswered questions. American Thoracic Society. Am J Respir Crit Care Med. 2000;162:2341-51.
7. Bousquet J, Mantzouranis E, Cruz AA, Aït-Khaled N, Baena-Cagnani CE, Bleecker ER, et al. Uniform
definition of asthma severity, control, and exacerbations: document presented for the World Health
Organization Consultation on Severe Asthma. J Allergy Clin Immunol. 2010;126:926-38.
8. Bel EH, Sousa A, Fleming L, Bush A, Chung KF, Versnel J et al. Diagnosis and definition of severe refractory
asthma: an international consensus statement from the Innovative Medicine Initiative (IMI). Thorax.
2011;66:910-7.
9. Chung KF, Wenzel SE, Brozek JL, Bush A, Castro M, Sterk PJ, et al. International ERS/ATS guidelines on
definition, evaluation and treatment of severe asthma. Eur Respir J. 2014;43:343-73.
10. Wenzel SE. Asthma phenotypes: the evolution from clinical to molecular approaches. Nat Med 2012;18:716-
25.
11. Bourdin A, Halimi L, Vachier I, Paganin F, Lamouroux A, Gouitaa M, et al. Adherence in severe asthma. Clin
Exp Allergy. 2012;42:1566-74.
12. Difficult-to-Treat Severe Asthma, 2011.
13. Burgess SW, Wilson SSI, Cooper DM, Sly PD, Devadason SG. In vitro evaluation of an asthma dosing device:
The smart-inhaler. Respir Med 2006;100:841-5.
14. Patel M1, Pilcher J, Travers J, Perrin K, Shaw D, Black P, et al. Use of Metered-Dose Inhaler Electronic
Monitoring in a Real-World Asthma Randomized Controlled Trial. J Allergy Clin Immunol Pract. 2013;1:83-91.](https://image.slidesharecdn.com/controversialinasthma20-22mar2016final-160506101203/85/Controversial-in-asthma-20-22-mar-2016-final-257-320.jpg)




